تحضير أفلام عينية للبريمونيدين طرطرات وتقييمها في الزجاج
2023-01-01 | المجلد السابع العدد الأول - المجلد السابع | مقالات بحثيةميشيل الحداد | محمد عثمان
الملخص
يعتمد العلاج الدوائي للزرق على الأدوية التي تقلل من الضغط داخل المقلة لإبقائه ضمن الحدود الطبيعية، حيث يُعد الضغط العالي داخل المقلة من أهم الأسباب التي تسبب تفاقم الحالة. تعد الأشكال معدلة التحرر ذات أهمية في هذا المجال ومنها الأفلام العينية التي تعمل على تحسين مطاوعة المريض مقارنةً بالقطرات العينية متعددة الجرعات. البريمونيدين طرطرات دواء ناهض لمستقبلات α2 مما يجعله فعالا في علاج الزرق. تهدف الدراسة الحالية إلى تحضير أفلام عينية للبريمونيدين طرطرات بهدف تحسين الكفاءة العلاجية. تمّ التحضير باستخدام تقنية صب المذيب وذلك بالبلمرات HPMC k15m و PVP-k30 بنسب مختلفة، استُخدم PEG 400 كملدّن. قُيّمت الأفلام بإجراء اختبارات فيزيوكيميائية، ودراسات تحرر الدواء باستخدام خلايا فرانز، أعطت الصيغة A6 أطول زمن تحرراً مقارنةً ببقية الصيغ المحضّرة.
كلمات مفتاحية : بريمونيندين طرطرات Brimonidine Tartrate، أفلام عينية Ophthalmic films،PVP-k30 ،HPMC k15m ، PEG 400 ، خلية فرانز.
المقدمة Introduction:
يعد الزرق من أشيع الأمراض التي تصيب العين كما أنها المسبب الرئيسي للإصابة بالعمى في العالم (1)، إنّ البريمونيدين طرطرات من المواد الفعالة المستخدمة بشكل كبير في خفض الضغط داخل المقلة لضمان عدم تدهور الحالة (2). الأفلام العينية أشكال عقيمة، ورقيقة يتمّ تصميم حجمها وشكلها بحيث يتناسب مع تطبيقها في كيس الملتحمة (cul de sac) في العين. تؤمن الأفلام العينية العديد من المزايا مثل زيادة زمن البقاء في العين، وتحرير الدواء ببطء، ودقة الجرعة، وتقليل الامتصاص الجهازي للدواء، وزيادة مطاوعة المريض بسبب انخفاض تواتر الإعطاء وقلة حدوث الآثار الجانبية الموضعية والجهازية وزيادة عمر الدواء على الرف shelf-life مقارنةً بالمحاليل المائية، واستبعاد المواد الحافظة، وبالتالي تقليل مخاطر تفاعلات الحساسية (3). صُنّفت الأفلام وفقًا لقابليتها للذوبان إلى أفلام قابلة للذوبان أو غير قابلة للذوبان أو دروكة حيوياً.(4) تمّ في هذا البحث العمل على صياغة أفلام عينية من مادة البريمونيدين طرطرات المستخدمة في علاج الزرق وهي مادة قابلة للذوبان في الماء وتوجد على شكل قطرات عينية (Alphagan Z®).
المواد والطرائق Materials and methods
المواد المستخدمة
بريمونيدين طرطرات(Brimonidine Tartrate) (Medichem SA, Spain)، هيدروكسي بروبيل ميتيل سيللوز (HPMC K15M) (Shreeji chemical, India)، بوفيدون PVP-k30 (Poly Vinyl Pyrrolidine) (Shreeji chemical, India)، بولي ايتيلين غليكول PEG 400 (Poly ethylene glycol) (Sigma-Aldrich, Germany).
بريمونيدين طرطرات Brimonidine Tartrate
يظهر الشكل 1 الصيغة الكيميائية للبريمونيدين طرطرات وهو 5-Bromo-6-(2-imidazolin-2-ylamino)quinoxaline D-tartrate . يتواجد على شكل مسحوق ذي لون أبيض أو أصفر شاحب، عديم الرائحة، ذواب في الماء والميتانول (5).

اسـتخدم فـي البحـث الأجهزة التاليـة:
خلية فرنز محلية الصنع Franz cell، جهاز التحليل الطيفي في مجال الأشعة المرئية وفوق البنفسجية (PG Instruments T80+, UK)، جهاز طيف الأشعة تحت الحمراءFTIR، Germany) ,(Bruker IR-10049361، فرن تجفيف (Carbolite PF30, Germany)، جهاز قياس درجة باهاء الوسط , Romania) (Hanna Instruments pH 211 Microprocessor pH Meter، جهاز الأمواج فوق الصوتية (Digital ultrasonic cleaner, Italy)، جهاز قياس الثخانة (Digital caliper DigiMax, Germany).
معايرة البريمونيدين طرطرات بمقياس الطيف الضوئي
أُجري مسح طيفي على جهاز الطيف الضوئي ضمن مجال الأشعة فوق البنفسجية لتحديد طول موجة الامتصاص الأعظمي، مع تكرار كل قياس ثلاث مرات (n=3). وتمّ اعتماد وقاء الفوسفات ذو pH 7.4 كوسط انحلال مناسب وفقاً لـSajeev وزملاؤه (6). وتم تحضير سلسلة عيارية تراوحت التراكيز بين (2-18 مكغ/مل)، وذلك انطلاقاً من محلول أم stock solution 20 مكغ/مل.
تحضير الأفلام العينية
استُخدم هيدروكسي بروبيل ميتيل سيللوز HPMC K15M، بولي فينيل بيروليدين pvp-k30 كعوامل مشكّلة لمطرس الفلم وتمّت إضافة PEG400 كعامل ملدّن للفلم. تم تحضير عدة صيغ تتضمن نسباً مختلفة من HPMC k15m و PVP-k30، مع ملاحظة اختلاف الخصائص الفيزيوكيميائية للأفلام المتشكلة وتحرر المادة الدوائية منها في الزجاج. ويتأثر معدل تحرر الدواء من المطارس البملرية التي تحتوي HPMC بعدة عوامل مثل كمية البلمر وتركيز الداوء ونسب(بلمر: دواء)، والوزن الجزئي للبلمر واللزوجة وخواص الدواء ونوع القالب المستخدم. حيث إنه عند تماس البلمر مع وسط الذوبان، ينفذ الوسط عبر مسامات ميكروية ويتشكل هلام بسبب إماهة سلاسل البلمرات، وبالتالي يتأثّر معدل تحرر الدواء.(7) أما العامل الملدّن PEG 400 فقد أُضيف في جميع الصيغ المحضّرة بنسبة 20% (و/و) من وزن البلمرات الجافة، حيث أن التراكيز الأعلى من 20% أعطت لدونة شديدة مما جعل الأفلام غير مقبولة، بينما التراكيز الأقل من 20% أعطت أفلام قاسية مما جعل الأفلام سهلة الكسر وقابلية الطي لها غير مقبولة. (8). تمّ الحصول على مطرس الفلم باستخدام تقنية صب المحل (Solvent Casting). أضيفت المادة الدوائية والبلمرات الداخلة في الصيغة تدريجياً، ومن ثم الملدن وذلك في 10 مل من المحل في بيشر مع استخدام التحريك المغناطيسي لمدة 3 ساعات، ومن ثم وُضعت في حمام مائي مع Ultrasound لمدة 30 دقيقة لضمان الانحلال والحصول على محلول رائق خالٍ من فقاعات الهواء. تمّ صب محلول المطرس في طبق بتري بلاستيكي مساحته (19.65) سم2 ووُضِع قمع مقلوب فوقها مع سد فتحة القمع باستخدام القطن لضمان عدم التبخر السريع للمحل، ثم وُضعت العينات في فرن التجفيف بدرجة حرارة °37م لمدة 48 ساعة.

الفحوص الفيزيوكيميائية المطبقة
اختبار تجانس المحتوى Content uniformity (9)
تمّ الاختبار على ثلاثة أفلام متساوين في الوزن من كل صيغة محضرة، وقياس تركيز المادة الفعالة في كل فلم، عند طول موجة الامتصاص الأعظمي للمادة الدوائية باستخدام جهاز المطياف الضوئي، بالمقارنة مع معادلة السلسلة العيارية المحضرة مسبقاً، حيث تمّ حل المادة الفعالة من الفلم في بالون معايرة سعة 10 مل، في 10 مل من محلول وقاء الفوسفات (pH 7.4) ثم باستخدام Ultrasound لمدة 3 ساعات، تمّ ترشيح المحلول باستخدام مرشحة قبل القياس((chrompure PTFE syringe filter, 0.45 µm. قيس امتصاص المحلول الناتج عند طول موجة الامتصاص الأعظمي مقابل محلول شاهد blank محضر بنفس الطريقة وغير متضمن المادة الفعالة(سواغات فقط).
اختبار قابلية الطي Folding endurance (9)
تمّ العمل على 3 أفلام في كل صيغة، حيث تمّ طي الفلم من منطقة محددة عدة مرات حتى يحدث تشققاً. حُدّدت قيمة قابلية الطي بعدد المرات التي تمّ فيها طي الفلم دون أن يتشقق.
اختبار قبط الرطوبة Moisture uptake (10)
تم التحقّق من نسبة امتصاص الرطوبة من الأفلام، لتأثيرها على الثبات الفيزيائي. تمّ العمل على ثلاثة أفلام، حيث تمّ تسجيل الوزن البدئي قبل إجراء الاختبار، ثم وُضعت الأفلام في مجفف (desiccator)، والذي يحوي 100 مل من محلول مشبع لكلور البوتاسيوم ثم وُضع في فرن التجفيف بدرجة حرارة الغرفة º25م. قيس الوزن بعد 3 أيام وحُسبت النسبة المئوية لامتصاص الرطوبة من خلال المعادلة:

كما حُسب المتوسط والانحراف المعياري SD.
اختبار فقدان الرطوبة moisture loss (10)
لهذا الاختبار أهمية في التحقق من سلامة الأفلام في الظروف الجافة، تم العمل على ثلاثة أفلام، وأخذ الوزن البدئي ثم وُضعت الأفلام في مجفف (desiccator)، مع وجود ملح كلور الكالسيوم اللامائي (anhydrous calcium chloride) وتم وضع المجفف بدرجة حرارة الغرفة º25 م.
تمّ أخذ الوزن بعد 3 أيام وتمّ حساب النسبة المئوية لفقد الرطوبة من خلال المعادلة:
كما تمّ حساب المتوسط والانحراف المعياري SD.
درجة باهاء السطح pH of the surface(11)
تم إجراء اختبار pH السطح للتحقق من إمكانية حدوث أي تهيج محتمل للعين. تُرِكت الأفلام بالانتباج في طبق بتري مغلقة عند درجة حرارة الغرفة لمدة 30 دقيقة، في 10. مل من الماء المقطر. تم وضع الأفلام المنتبجة تحت أقطاب مقياس الـpH الرقمي(وتم إجراء الاختبار أيضاً باستخدام أوراق الـpH) لتحديد درجة باهاء السطح.
موحودية الثخانةthickness uniformity (12)
حُدّد متوسط ثخانة الافلام باستخدام جهاز digiMax، بأخذ قياس كل فلم 3 مرات وحساب المتوسط والانحراف المعياري
اختبار التحرر في الزجاج In vitro drug release rate (13)
تمّ اختبار تحرر البريمونيدين طرطرات في الزجاج من الصيغ، باستخدام خلية محلية الصنع محاكية لعمل خلية فرانز (الشكل 2)، والتي تتكون من الأجزاء التالية:
حجرة مستقبلة حجم 12 مل، تحتوي على محلول دارئة الفوسفات (pH 7.4) كوسط ذوبان. حجرة معطية يّثبّت فوقها الفلم العيني على غشاء صنعي من نترات السيللوز أبعاد المسام 0.45 ميكرومتر. تمّ استخدام هذا الغشاء في محاولة لمحاكاة ظروف العين في الزجاج مثل الحاجز الظهاري للقرنية. سخّان مع حمام مائي مزوّد بحساس(Thermocouple) للحفاظ على درجة حرارة 37o ±1 درجة مئوية. محرك مغناطيسي لتحريك محلول الوقاء في الحجرة المستقبلة بسرعة 50 دورة بالدقيقة. تمّ سحب أحجام من العينات(2 مل) واستبدالها بحجم مساوٍ من محلول وقاء الفوسفات pH 7.4. تمّت مقايسة كمية الدواء المتحرر، باستخدام مقياس الطيف الضوئي عند موجة امتصاص 248 نانومتر مقابل شاهد من محلول (pH=7.4).

دراسة حرائك تحرر الدواء kinetic analysis of drug release(14)
تمّت دراسة أنماط رياضية لتحرر البريمونيدين طرطرات من مختلف صيغ الأفلام العينية المحضرة، وفق عدة نماذج للتحرر، تمّ تحليل النتائج والتحقق من الأنماط المناسبة من خلال استخدام برنامج مايكروسوفت Excel 2019، تمّ حساب قيم معاملات الارتباط (R²) وفق الأنماط التالية:
- نمط التحرر من الرتبة صفر (Zero order release model)
- نمط التحرر من الرتبة الأولى (First order release model)
- نمط التحرر وفق هيكسون-كرول (Hixson-Crowell)
- 4. نمط التحرر وفق هيغوشي (Higuchi release)
- 5. نمط التحرر وفق كورسماير-بيباس (Korsmeyer-Peppas)
يعتبر النمط الذي يمتاز بقيمة معامل ارتباط أعلى مقارنةً مع بقية الأنماط هو النمط الأكثر مواءمة.
تقييم التآثرات بين البريمونيدين طرطرات والسواغات
تمّ قياس عينات نقية من المواد بمفردها، أو بشكل مزائج فيزيائية ثنائية، باستخدام جهاز الطيف بالأشعة تحت الحمراء من نوع (Bruker IR 10049361, Germany) وذلك ضمن المجال (400-4000) سم-1. إذ تمّ المسح بالأشعة تحت الحمراء لكل من البريمونيدين طرطرات للتأكد من هوية المادة والمزائج الفيزيائية لكل من السواغات الداخلة في تحضير الأفلام والدواء (50:50)%، بهدف دراسة تحرّي إمكانية حدوث تآثرات بين الدواء والسواغات المستخدمة في صياغة الأفلام.
النتائج Results
معايرة البريمونيدين طرطرات بمقياس الطيف الضوئي:
تبين من إجراء المسح الطيفي لمحلول المادة الفعالة في المجال 200-400 نانومتر أن طول موجة الامتصاص الأعظمي 248 نانومتر، وهذا وافق ما وجده لـSajeev وزملاؤه (6). ويبين الشكل طول موجة الامتصاص الأعظمي لمادة البريمونيدين طرطرات في المجال المدروس.
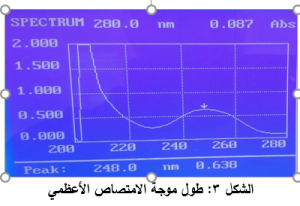
اختبار تجانس المحتوىcontent uniformity
أظهرت النتائج في الجدول 2، أن المحتوى الدوائي للأفلام الناتجة تراوح بين (94 – 98)%
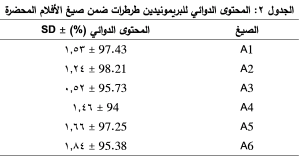
قابلية الطي folding endurance
تراوحت قيم قابلية الطي للأفلام بين (350-150) كما هو واضح في الجدول 3، واختلف وفقاً لنسبة البلمرات الداخلة في الصيغة والملدّن. وهذا يبين أن إضافة PEG400 كعامل ملدن قد ساهم في إعطاء أفلام مرنة مناسبة تتحمل شروط التحضير والنقل والتخزين والتطبيق العيني، وحركة الأجفان.

قبط الرطوبة moisture uptake
بينت نتائج الفحص بعد الحفظ لثلاثة أيام، أن الصيغة A6 المتضمنة النسبة الأكبر من البلمرات المحبة للماء HPMC k15m، PVP-k30 كانت الأكثر قبطاً للرطوبة. الجدول (4)، حيث كانت نسبة قبط الرطوبة بعد ثلاثة أيام (5.3%) بينما كانت الصيغة A1 أقل قبطاً للرطوبة (0.75%). حيث ازدادت قدرة الأفلام على قبط الرطوبة بازدياد نسب البلمرات المحبة للماء المشكّلة لها .
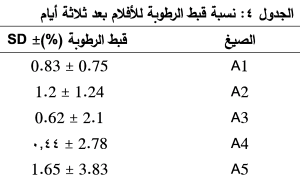
فقد الرطوبة moisture loss من الأفلام
بينت نتائج الفحص بعد الحفظ لثلاثة أيام، أن الصيغة A6 المتضمنة النسبة الأكبر من البلمرات المحبة للماء كانت الأكثر فقداً للرطوبة، الجدول (5)، حيث كانت تلك النسبة بعد ثلاثة أيام (10.9%)، بينما كانت الصيغة A1 الأقل فقداً للرطوبة (1.29%)، حيث ازداد فقدان الفلم للرطوبة مع زيادة نسبة البلمرات المحبة للماء المشكّلة لها.

درجة باهاء السطح (pH of the surface)للأفلام
يوضح الجدول 6 أن درجة باهاء الأفلام المحضرة تراوحت من 5.1 حتى 5.8، وهي تُعد محتملة وغير مخرشة للعين نظراً لأنها تقع ضمن مجال الـ pH {4-10} للأشكال التي تناسب التطبيق العيني. (15)
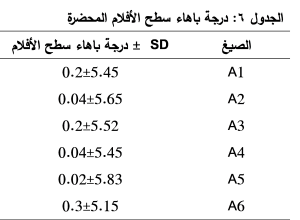
ثخانة الأفلام (Thickness of films)
تُظهر النتائج في الجدول 7 بأن ثخانة الأفلام المحضرة تراوحت بين (0.4-0.1) ملم.

تحرر الدواء في الزجاج In vitro drug release
يُظهر الجدول 8 معدلات تحرر البريمونيدين طرطرات من الأفلام العينية المحضّرة. كانت الصيغة A6 الأبطأ تحرراً من بين صيغ الأفلام المحضّرة، حيث استمر تحرر البريمونيدين طرطرات منها حتى 6 ساعات بينما استمر التحرر في الصيغة A5 المتضمنة نسب أقل من البلمرات المشكلة للفلم أربع ساعات، أما في الصيغتين A4 و A3 فقد استمر التحرر لمدة ساعتين، بينما تحررت كامل كمية البريمونيدين طرطرات من الصيغتين A2 و A1 خلال ساعة واحدة فقط. حيث إنّ ازدياد تركيز PVP-k30 يزيد من زمن تحرر الدواء، وهذا يوافق ما توصل إليه Khan وزملاؤه(2021) حيث يحدث إماهة للفلم عند ملامسته وسط الذوبان (16).
دراسة حرائك تحرر البريمونيدين طرطرات kinetic analysis of drug release من الأفلام
يوضح الجدول 9 قيم معاملات الارتباط R2، بالنسبة لأنماط التحرر من الرتبة صفر، الرتبة الأولى، هكسون-كرول، هيغوتشي، كورسماير بيباس للأفلام المحضرة. تُظهر النتائج أن الصيغ A1،A2، A3، A4، A5، A6 تتوافق مع الرتبة صفر للتحرر، حيث كانت قيم معاملات الارتباط أعلى بالمقارنة مع بقية الأنماط، أي أنّ تحرر الدواء من المطرس ثابت خلال الزمن، وهذا يتوافق مع التحرر المضبوط. بينما كان التحرر من الصيغة A2 يتوافق أيضاً مع نمط Korsmeyer-Peppas للتحرر وتم حساب معامل التحرر الأسي n والذي كان بين (0.7-0.83) وهذا يدل على أن انتشار الدواء شاذ ولا يتبع قانون فيك للانتشار (Non-Fickan transport) ويتحكم به نفوذية الفلم وانتشار الدواء عبر سلاسل البلمرات وانتباج وتآكل البلمرات معاً (17) حيث يشرح نمط كورسماير- بيباس(Korsmeyer-Peppas) علاقة تحرر الدواء بآلية تحرره ويُعطى وفق العلاقة الآتية:
Qt =a.tn
حيث إنَّ Qt النسبة المئوية المتحررة من الدواء عند الزمن t، و a ثابتة تعبر عن الخواص الهندسية geometric للشكل الصيدلاني، بينما n أس التحرر أو الانتشار والتي تدل على نمط التحرر، و t الزمن(ساعة). تُحسب قيمة n من الخط البياني المرسوم بين log(Qt) و log(t).
التآثرات بين البريمونيدين طرطرات والسواغات
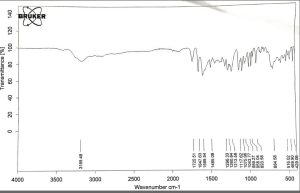
يُظهر الشكل 4 طيف الأشعة تحت الحمراء للبريمونيدين طرطرات، كما يُبين الشكل 5 طيف الأشعة تحت الحمراء للمزيج الفيزيائي لـ (HPMC k15m) والبريمونيدين طرطرات. كما يُظهر الشكل 6 طيف IR للمزيج الفيزيائي لـ (PVP-k30) والبريمونيدين طرطرات، ويُظهر الشكل 7 طيف IR للمزيج الفيزيائي لـ (PEG 400) والبريمونيدين طرطرات.
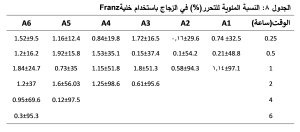

يُبيّن الجدول 10 أهم القمم الوصفيّة في طيف IR والمجموعات الوظيفية المتوقعة الموافقة لها.
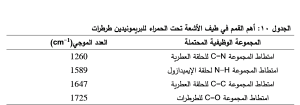
بُظهر طيف FTIR للبريمونيدين قمّة مميزة عند 1589 سم-1 تقابل اهتزاز المجموعات –NH للإيميدازول. وعُثر على قمّة قد تُعزى لاهتزازات الامتطاط للمجموعات C = N و C = C عند 1260 سم-1 و 1647 سم-1 على التوالي. كما ظهرت اهتزازات للمجموعة C = O عند 1725 سم-1. وهذا يتوافق مع نتائج Abu Rahma وزملائه (18) وSharma وزملائه (19).
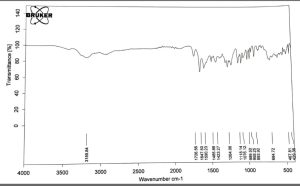

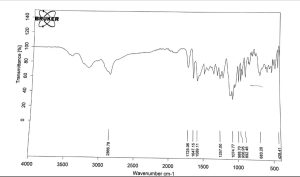
يُلاحظ في المخططات السابقة للأمزجة الفيزيائية للبريمونيدين طرطرات مع السواغات بقاء العُصابات الدالة على المجموعات الوظيفية المميزة في صيغة الدواء وهذا قد يشير إلى محدودية التآثرات بين البلمرات المستخدمة والبريمونيدين. تم في هذه الدراسة تحضير صيغ أفلام ذوابة في الماء ودراسة تحرر البريمونيدين طرطرات منها، وتحديد خواصها الفيزيوكيميائية وأنماط تحرر الدواء منها، وأظهرت النتائج أن ازدياد نسبة HPMC k15m و PVP-k30 المستخدمة في الصيغ يُمكن أن يزيد من زمن تحرر البريمونيدين طرطرات.
الاستنتاجات Conclusions
جرى تحضير 6 صيغ مختلفة من الأفلام العينية الذوابة، للبريمونيدين طرطرات، باستخدام بلمرات محبة للماء (HPMC k15m،PVP-k30) وذلك بإضافتها بنسب مختلفة وتمّت إضافة PEG 400 بنسبة ثابتة. كان تحرر البريمونيدين من الصيغة A6 الأطول تحررا ًحيث استمر لمدة 6 ساعات بينما استمر لمدة 4 ساعات من الصيغة A5 أما من الصيغتين A3 و A4 فقد تحرر البريمونيدين خلال ساعتين، وتحرر الدواء الصيغتين A1 و A2 خلال ساعة واحدة. إنّ زيادة نسبة البلمرات المائية المستخدمة في تحضير الأفلام زاد من زمن تحرر البريمونيدين طرطرات من الأفلام كما اختلفت نسب فقد الرطوبة وقبطها وثخانة الأفلام. كان تحرر البريمونيدين من الصيغ المحضرة وفقاً للرتبة صفر، أي أن التحرر ثابت خلال الزمن وهو يعد نمطاً مفضلاً لتحرر الأدوية العينية.
المراجع :- 1. Shalaby WS, Shankar V, Razeghinejad R, Katz LJ. Current and new pharmacotherapeutic approaches for glaucoma, Expert Opinion on Pharmacotherapy, 21, 16, 2027-2040, 2020.
- 2. Oh DJ, Chen JL, Vajaranant TS, Dikopf MS. Brimonidine tartrate for the treatment of glaucoma. Expert Opinion on Pharmacotherapy, 20, 1, 115–122. 2019.
- 3. Kumari, A, Sharma, PK, Garg VK, Garg, G. Ocular inserts Advancement in therapy of eye diseases, Journal of Advanced Pharmaceutical Technology and Research, 1, 3, 291–296, 2010.
- 4. Parveen N, Joshi H. Ocuserts: A Novel Formulation Approach in Drug Delivery System, Saudi Journal of Medical and Pharmaceutical Sciences, 6, 5, 420–425, 2020.
- FDA, S-, N. D. A. Alphagan, Doctissimo, 1.2013.
- Bhagav P, Deshpande P, Pandey S, Chandran S. Development and validation of stability indicating UV spectrophotometric method for the estimation of brimonidine tartrate in pure form, formulations and preformulation studies. Der Pharmacia Lettre, 2, 3, 106-22, 2010
- Mohamed FAA, Roberts M, Seton L, Ford JL, Levina M. Rajabi-Siahboomi AR, The effect of HPMC particle size on the drug release rate and the percolation threshold in extended-release mini-tablets. Drug Development and Industrial Pharmacy, 41, 1, 70–78, 2015.
- Baranowski P, Karolewicz B, Gajda M, Pluta J. Ophthalmic Drug Dosage Forms: Characterisation and Research Methods. The Scientific World Journal.. vol:2014. 2014.
- Devi U, Gupta T, Kumari P. Ophthalmic Insert : A Controlled Drug Delivery System for Eye Diseases, International Journal of Emerging Technologies and Innovative Research, 8, 1, 1120–1127, 2021.
- Taghe S, Mirzaeei S, Alany RG, Nokhodchi A. Polymeric inserts containing eudragit® L100 nanoparticle for improved ocular delivery of azithromycin, Biomedicines, 8, 11, 1–21, 2020.
- Noori MM, Al-Shohani ADH, Yousif NZ. Fabrication and characterization of new combination ocular insert for the combined delivery of tinidazole and levofloxacin, Materials Today: Proceedings, 2021.
- Shah, SNH, Nawaz A, Javed H, Rafiq M, Riaz R, Sadaquat H, Akhtar M. Preparation and In Vitro/In Vivo Evaluation of Antihistaminic Ocular Inserts, Pharmaceutical Chemistry Journal, 52, 7, 615–622, 2018.
- Khurana G, Arora S, Pawar PK. Ocular insert for sustained delivery of gatifloxacin sesquihydrate: Preparation and evaluations, International journal of pharmaceutical investigation, 2, 2, 70, 2012.
- Costa P, Lobo MS. Modeling and comparison of dissolution profiles, European Journal of Pharmaceutical Sciences, 123, 123-133, 2001.
- Lim LT, Ah-Kee EY, Collins CE. Common eye drops and their implications for pH measurements in the management of chemical eye injuries, International Journal of Ophthalmology, 7, 6, 1067–1068, 2014.
- Ali B, Khan A, Alyami HS, Ullah M, Wahab A, Badshah M, Naz A. Evaluation of the effect of carrier material on modification of release characteristics of poor water soluble drug from liquisolid compacts, PLoS ONE, 16, 8, 2021.
- Lobo M.S. and Costa P. Modeling and comparison of dissolution profiles, European Journal of pharmaceutical sciences. 123, 123-133. 2001.
- Aburahma MH، Mahmoud AA. Biodegradable ocular inserts for sustained delivery of brimonidine tartrate: preparation and in vitro/in vivo evaluation, AAPS PharmSciTech, 12, 4, 1335–1347, 2011.
- Sharma, PK, Chauhan MK. Optimization and Characterization of Brimonidine Tartrate Nanoparticles-loaded In Situ Gel for the Treatment of Glaucoma, Current Eye Research, 46, 11, 1703–1716, 2021.