تحضير أنظمة إيتاء فموية للأسيكلوفير بشكل مستحلبات ميكروية لتدبير الإنتانات الفيروسية وتقييمها في الزجاج
2023-07-01 | المجلد السابع العدد الثاني - المجلد السابع | مقالات بحثيةإيمان العلي | محمد عثمان
الملخص
الهدف من هذه الدراسة تطوير مستحلبات ميكروية من الأسيكلوفير والتي يمكن إيتاؤها فموياً وتطبيقها موضعياً، تمت دراسة انحلالية (solubility) الأسيكلوفير في عدد من السواغات، التي استُخدمت في تحضير المستحلبات الدقيقة، ثمّ تمّ دراسة تأثير نسبة العوامل الاستحلابية على حجم قطيرات الطور الداخلي وتحديد النسب الفُضلى منها للوصول إلى الأبعاد الميكروية، ثمّ تمّ تحميل الأسيكلوفير على الصيغ المحضرة ودراسة قدرة كل صيغة على حل الأسيكلوفير. تم تحديد حجم قطيرات الطور الداخلي باستخدام جهاز Mastersizer وجهاز Nanosizer ودراسة نفاذية ودرجة باهاء الصيغ المحضرة وثباتيتها تحت الطرد المركزي، حيث تم التّوصل إلى صيغة بأبعاد حوالي 14 نانومتر وتحرر ما يزيد عن 90% من الدواء وذلك بدراسة التحرر باستخدام خلية فرانز. تبين أن قطيرات الطور الداخلي كروية باستخدام المجهر الالكتروني الماسح SEM. كما ثبُت باستخدام المسح بالأشعة تحت الحمراء FTIR والمسح الحراي التفاضلي DSC قلّة التداخلات بين الأسيكلوفير والسواغات المستخدمة.
كلمات مفتاحية : المستحلبات الميكروية، الأسيكلوفير، فيروسات الحلأ، العوامل الفعالة على السطح.
المقدمة Introduction
من بين أكثر من مئة فيروس من فيروسات الهربس المعروفة، فقط ثمانية فيروسات تصيب الإنسان، وهي: فيروس الهربس البسيط بنمطيه الأول والثاني (herpes simplex types 1 and 2)، فيروس الحماق النطاقي (varicella-zoster)، الفيروس المضخم للخلايا (cytomegalovirus)، فيروس إبشتاين بار (Epstein-Barr)، فيروس الهربس البشري 6 (human herpes 6)، فيروس الهربس البشري7(human herpes 7)، وفيروس كابوزي ساركوما أو فيروس الهربس البشري 8 (Kaposi’s sarcoma virus). يمكن لجميع فيروسات الهربس أن تشكّل عدوى كامنة داخل أنسجة معينة، والتي تعتبر مميزة لكل فيروس. من أهم الأدوية المضادة للفيروسات والتي تؤثر في فيروسات الهربس الأسيكلوفير حيث يعتبر فعالاً ضد فيروس الحلأ البسيط بنمطيه الأول، والثاني، وفيروس الحماق النطاقي. هذه الفعالية تتطلب تحويل الأسيكلوفير بواسطة الأنزيم الفيروسي تيميدين كيناز إلى الشكل أحادي الفوسفات، مما يؤمن الفعالية تجاه الخلايا المصابة فقط، ثم يتحول بعد ذلك بواسطة الأنزيمات الخلوية إلى ثنائي الفوسفات ثم إلى الشكل ثلاثي الفوسفات (الشكل الفعّال)، هذا الشكل الفعّال يثبط تركيب DNA الفيروسي ويثبط التضاعف عن طريق تثبيط أنزيم DNA بوليميراز الفيروسي. يمتص الأسيكلوفير بشكل سيئ من القناة الهضمية بعد الجرعات الفموية، إذ يبلغ التوافر الحيوي للأسيكلوفير الفموي حوالي 10 إلى 20٪، يرتبط بالبروتين حوالي (9-33%)، يتم اطراح الأسيكلوفير في البول بدون تغيير بشكل كبير عن طريق الترشيح الكبيبي والافرازات الأنبوبية، مع حوالي (14%) من المستقلبات غير الفعّالة التي تظهر في البول. عند المرضى الذين لديهم وظائف الكلية طبيعية، يكون نصف العمر الحيوي حوالي 2 إلى 3 ساعات. صنف نظام التصنيف الصيدلاني الحيوي(BCS) الأسيكلوفير تحت الصف الثالث Class III وذلك في الجرع الفموية التي تصل لحد 400 ملغ وكذلك تم تصنيفه تحت الصف الرابع Class IV وذلك عندما يعطى بجرعة 800 ملغ، وُجِد أن امتصاص الأسيكلوفير بطيء ومتغير وغير مكتمل مع انخفاض التوافر الحيوي عن الطريق الفموي1،2،3، مع ذلك فإن العلاج عن طريق الفم لهذا الدواء يتطلب تناول جرعات عالية وتكرارها، مما يؤدي إلى آثار ضارة جهازية محتملة مثل الفشل الكلوي الحاد والسمية العصبية 4. يعود ضعف كفاءة الأسيكلوفير في العلاج عن طريق الفم بشكل أساسي إلى قابلية ذوبانه المائية المحدودة ونفاذه المنخفض2،6،7،8. كذلك العلاج الموضعي بالأسيكلوفير قليل الفعالية بسبب النفاذية الجلدية المنخفضة 8.
دُرِسَت المستحلبات الدقيقة على نطاق واسع لتعزيز التوافر الحيوي للأدوية ضعيفة الذوبان، حيث أنّ للمستحلبات الدقيقة توتر سطحي منخفض جدًا وحجم قطيرات صغير مما يؤدي إلى امتصاص واختراق عاليين. يتزايد الاهتمام بهذه النواقل متعددة الاستخدامات، وتنوعت تطبيقاتها إلى طرائق إعطاء مختلفة بالإضافة إلى الطريق الفموي. يمكن أن يعزى ذلك إلى خصائصها الفريدة في الذوبان والثبات الترموديناميكي الذي لفت الانتباه لاستخدامها كوسيلة جديدة لإيتاء الأدوية، إذ كانت النتائج التي تم الحصول عليها واعدة للغاية.
إنّ صياغة مستحلبات ميكروية للأسيكلوفير قد تحسّن التوافر الحيوي وتؤدي إلى إنقاص الجرعة المعطاة فموياً.
المواد والطرائق Materials and Methods
جرى الحصول على الأسيكلوفير من مختبرات ميديكو للصناعات الدوائية (AMRI،India)، التوين 80 والتوين 60 والسبان 80 من Riedel-De haen (Germany)، البروبيلين غليكول والبولي ايتيلين غليكول 200 والغليسيرين من Hutong Global (China)، زيت الخروع وحمض الزيت من Panreac corp (Spain)، زيت دوار الشمس من Croda (India).
- دراسة ذوبانية الأسيكلوفير في سواغات نقية:
تم ذلك أولاً من خلال تحضير سلاسل عيارية في (الميتانول، الماء المقطر، الغليسيرين،PEG200، البروبلين غليكول)، وذلك للتأكد من عدم تداخل قمم الامتصاص العظمى، ثم ثانياً تمّ دراسة ذوبانية الأسيكلوفير في السواغات بطريقة الدورق الهزاز (Shake flask method) حيث أضيف مقدار25 ملغ من الأسيكلوفير إلى (2 مل) من الطور الزيتي (حمض الزيت، زيت الخروع، زيت دوار الشمس)، أوالعوامل الاستحلابية (توين 80، توين 60)، أوالمذيبات المشاركة (غليسيرين، بروبلين غليكول، بولي ايتيلين غليكول 200) في أنابيب تثفيل ومزج بالأمواج فوق الصوتية لمدة 30 دقيقة بالدرجة 37° درجة مئوية لتسريع الانحلال، ثم تم إخضاع العينات للاهتزاز ضمن جهاز مازج (Shaker) لمدة 48 ساعة بدرجة حرارة 25 م° للوصول إلى التوازن، ثفلت بعدها بسرعة (3000) دورة بالدقيقة بواسطة مثفلة (Hermle Z200A،Germany) لمدة 10 دقائق 9.أُخذ عينة (1مل) من الطافي ومُدّد بالميتانول في بالون معايرة سعة 10 مل إلى خط العيار، وتم مقايسة الامتصاص بجهاز الطيف الضوئي (Genove Life science 6300، Jenway،China) عند طول موجة 253 نانومتر، وتمّ التمديد بالميتانول عند اللزوم. استُخدِمَ الميتانول كناصع، تم تكرار التجربة ثلاث مرات وحساب الانحراف المعياري. ووفقاً للنتائج تم اختيار زيت دوار الشمس وزيت الخروع كأطوار زيتية، التوين 80 كعامل استحلابي رئيسي، PEG200 كمذيب مساعد، وتم إضافة السبان 80 كعامل استحلابي مثبت معاكس.
- تحضير المستحلبات الأولية (ز/م) ودراسة تأثيرات نسب العوامل الاستحلابية على أبعاد قطيرات الطور الداخلي:
تم تحضير 18 صيغة بنمط استحلابي (ز/م) منها (9) صيغ بأساس من زيت دوار الشمس و (9) صيغ بأساس من زيت الخروع بالاضافة إلى التوين 80 والسبان80 (عوامل استحلابية) والماء المقطر. في جميع الصيغ، تم تثبيت كميات الزيت والماء PEG200 وتغيير نسب السبان80 والتوين 80 وفق الجدولين (1،2) التاليين:
|
الجدول (1): المستحلبات الأولية بأساس من زيت دوار الشمس |
||||||
| زيت دوار الشمس
(غ) |
ماء مقطر
(غ) |
PEG200
(غ) |
التوين 80
(غ) |
السبان 80
(غ) |
نسبة العوامل الاستحلابية %(وزن/وزن) | |
| FS1 | 10 | 110 | 10 | 0.75 | 0.25 | 0.76 |
| FS2 | 10 | 110 | 10 | 3.75 | 1.25 | 3.7 |
| FS3 | 10 | 110 | 10 | 7.5 | 2.5 | 7.1 |
| FS4 | 10 | 110 | 10 | 11.25 | 3.75 | 10.3 |
| FS5 | 10 | 110 | 10 | 15 | 5 | 13.3 |
| FS6 | 10 | 110 | 10 | 45 | 15 | 31.5 |
| FS7 | 10 | 110 | 10 | 52.5 | 17.5 | 35 |
| FS8 | 10 | 110 | 10 | 60 | 20 | 38 |
| FS9 | 10 | 110 | 10 | 67.5 | 22.5 | 40.9 |
|
الجدول (2): المستحلبات الأولية بأساس من زيت الخروع |
||||||
| زيت الخروع
(غ) |
ماء مقطر
(غ) |
PEG200
(غ) |
التوين 80
(غ) |
السبان 80
(غ) |
نسبة العوامل الاستحلابية %(وزن/وزن) | |
| FC1 | 10 | 110 | 10 | 0.9 | 0.1 | 0.76 |
| FC2 | 10 | 110 | 10 | 4.5 | 0.5 | 3.7 |
| FC3 | 10 | 110 | 10 | 9 | 1 | 7.1 |
| FC4 | 10 | 110 | 10 | 13.5 | 1.5 | 10.3 |
| FC5 | 10 | 110 | 10 | 18 | 2 | 13.3 |
| FC6 | 10 | 110 | 10 | 54 | 6 | 31.5 |
| FC7 | 10 | 110 | 10 | 63 | 7 | 35 |
| FC8 | 10 | 110 | 10 | 72 | 8 | 38 |
| FC9 | 10 | 110 | 10 | 81 | 9 | 40.9 |
في البداية تم وزن الكميات بدقة باستخدام ميزان حساس، تمّ إضافة العوامل الاستحلابية إلى الزيت وتم المزج باستخدام مازج مغناطيسي على سخان كهربائي لمدة 15 دقيقة بدرجة حرارة 40° م درجة مئوية، بعد ذلك نٌقِلَ المزيج إلى حمّام الأمواج فوق الصوتية وتم تستيل الماء قطرة فقطرة مع التحريك بدرجة حرارة 40° م درجة مئوية لمدة 15 دقيقة ثانية.
تم تقييم أنماط المستحلبات الناتجة وتقييم تأثير نسب العوامل الاستحلابية على حجم القطيرات باستخدام المجهر الاستقطابي و المجهر الضوئي مع التمديدات اللازمة للعينات وتلوينها بأزرق الميتيلين وباستعمال عدادة نيوبار. تم اختيارالصيغ متماثلة الخواص isotropic التي اختفت فيها قطيرات الطور الداخلي تحت المجهرالاستقطابي.
دراسة تحميل الأسيكلوفير في الصيغ المقترحة:
حققت الصيغ من F6 إلى F9 بأساس من زيت دوار الشمس أو زيت الخروع، الخواص المنشودة، وهي التي تم اختيارها لتحميل الأسيكلوفير وتحديد عتبة الإشباع في الصيغة، تم تحميل الصيغ المقترحة بالأسيكلوفير، حيث تراوحت تراكيز الأسيكلوفير بين 3ملغ/غ مستحلب إلى 20ملغ/ غ مستحلب، حضرت جميع الصيغ بمزج الدواء (بتراكيز مختلفة) مع الطور المائي بدرجة حرارة 40° م لمدة 15 دقيقة بالاستعانة بجهاز الأمواج فوق الصوتية، ومُزِجَت العوامل الاستحلابية ضمن الطور الزيتي بدرجة حرارة 40°م ثم تمّ إضافة الطور الخارجي إلى الطور الداخلي بالتدريج وذلك في حمّام الأمواج فوق الصوتية، ثمّ تمّ إخضاع الصيغ إلى عملية الرج باستخدام جهازهز (shaker) لمدة 72 ساعة بدرجة حرارة 25م° وتم تقييم الخواص الفيزيوكيميائية.
- تحري بلورات في الصيغ المحضرة باستعمال المجهر الاستقطابي:
تم تحري بلورات الدواء في الصيغ المحضرة:
من FS6 إلى FS9 بأساس من زيت دوار الشمس
من FC6 إلى FC9 بأساس من زيت الخروع
وذلك للتأكد من تمام انحلال الأسيكلوفير في المستحلبات.
دراسة خصائص المستحلبات:
- تعيين النفاذية الضوئية Transmittance عند طول موجة 650 نانومتر:
هناك ارتباط بين أبعاد القطيرات وشفافية ونفاذية الضوء عبر المستحلبات، حيث تتجاوز نفاذية الضوء المرئي للمستحلبات الرائقة 98%، لاحتوائها على أبعاد ميكروية ونانوية، في حين أن المستحلبات العكرة تمتص وتبعثر كمية أكبر من الضوء، مما يؤدي إلى الحصول على قيم نفاذية أقل10.
- تحديد درجة حموضة المستحلبات (pH):
تم تحديد درجة الحموضة باستخدام جهاز pH 211، HANNA،Italy)) عند الدرجة 25°م مع اجراء القياس ثلاث مرات وحساب الانحراف المعياري.
- دراسة توزع أبعاد القطيرات باستخدام الـ MasterSizer:
حُدّد حجم القطيرات ذوات الأبعاد أكبر من 0.1 ميكرومتر، من خلال تشتت الضوء الديناميكي، باستخدام جهاز الــ Master sizer (Master-sizer 3000، Malvern instruments Corp، UK)، أجري التحليل عند زاوية تشتت 90، درجة الحرارة 25° م، حيث تم القياس بعد التمديد بالماء المقطر. ثم حُدِّدَ متوسط حجم القطيرات mean particle size D (3.2)، وتوزع الحجم size distribution ، وتجانس توزع الحجم من خلال size uniformity، إذ أنّه كلّما انخفضت قيم توزع الحجم هذين المعاملين يكون المستحلب ذو أبعاد قطيرات متقاربة الحجم و معامل تشتت منخفض 11،12
- تحديد حجم القطيرات (Determination of droplet size) باستخدام الـ Nanosizer:
قِيسَ حجم القطيرات باستخدام مقياس تشتت الضوء الديناميكي (Dynamic Light Scattering)، بعد تمديد المستحلب باستخدام (Nanosizer، Malvern،UK) ضمن المجال 0.3 نانومتر -5 ميكرومتر.
- دراسات ثبات المستحلبات الدقيقة تحت تأثير الطرد المركزي Stability studies of microemulsion by centrifugation
تمّ باستخدام المثفلة (HERMLE Z 200A, Germany) بأخذ 10 مل من الصيغ المدروسة، 3500 دورة في الدقيقة لمدة نصف ساعة 14.
- دراسات التحرر في الزجاج In vitro drug realease)):
أجريت دراسات التحرر في الزجاج من خلال أغشية نصف نفوذة
من أسيتات السيللوز(0.45 مكم)، باستخدام خلايا فرانز Franz cell محلية الصنع، تم استخدام دارئة الفوسفات (PH=6.4) كوسط استقبال
- المجهر الالكتروني الماسح:
تم استخدام SEM، TESCAN، VEGA، Czech Republic)) لفحص شكل وخواص سطح وحجم قطيرات الطور الداخلي، وذلك بالنسبة للصيغ الأمثل (FS8،FS9).
- دراسة التآثرات بين الأسيكلوفير والسواغات المستخدمة Drug – excipient interactions
8-1- المسح الحراري التفاضلي Differential Scanning Calorimetry:
تم اجراء المسح الحراري التفاضلي باستخدام جهاز (DSC131، SETARAM) حيث تم وزن عينات (4-5 ميلي غرام) بشكل دقيق مع وضعها ضمن بوتقة خاصة من الألمنيوم وتم احكام اغلاقها جيدا بواسطة مكبس خاص. أجري الاختبار مع استخدام بوتقة ثانية فارغة من الالمنيوم كشاهد، وذلك بتعريض العينات إلى حرارة بمعدل متزايد 10°م درجة مئوية / دقيقة. تم اجراء الاختبار على المساحيق النقيّة للأسيكلوفير والسواغات، من ثم على المزائج الفيزيائية للمادة الفعالة مع كل سواغ وذلك بنسب (1:1) 15،16
8-2- المسح الطيفي بالأشعة تحت الحمراء FTIR Spectroscopy:
تم القيام بالمسح بالأشعة تحت الحمراء لكل من الأسيكلوفير ومن ثمّ على المزيج الفيزيائي للمادة الفعالة مع كل سواغ مُستخدَم، بنسب (1:1). وذلك بهدف التحري عن إمكانية حدوث أي تداخل بين الدواء والسواغات افي الصيغ. 17
النتائج والمناقشة Results and Discussion
ذوبانية (solubility) الأسيكلوفير في السواغات:
بعد الحصول على السلاسل العيارية للأسيكلوفير، ومقايسة تراكيز الاشباع للدواء ضمن المُحلّات تم الحصول على القيم المدرجة في الجدول (3).
| الجدول (3): ذوبانية الأسيكلوفير في مكونات الصيغ النقيّة (زيوت، العوامل الاستحلابية، المذيبات المساعدة) | |
| السواغ | الذوبانية ± SD (ملغ/مل) |
| زيت دوار الشمس | 8.5 ±2.15 |
| زيت الخروع | 3.5 ±1.3 |
| حمض الزيت | 1.5 ±0.34 |
| التوين 80 | 6.2 ±2.07 |
| التوين 60 | 1.4 ±0.56 |
| الغليسيرين | 2.5 ±1.65 |
| البروبيلين غليكول | 1.5 ± 0.91 |
| البولي ايتيلين غليكول 200 | 6.5 ±1.98 |
تم اختيار السواغات التي أبدت قدرة أكبر على حل الأسيكلوفير (زيت الخروع، زيت دوار اشمس، البولي ايتيلين غليكول 200، التوين 80) وتمّ إضافة السبان 80 كعامل استحلابي مثبّت معاكس.
نتائج تحضير المستحلبات الأولية وتأثير زيادة نسبة العوامل الاستحلابية على حجم القطيرات:
دُرٍست الصيغ باستخدام المجهر الاستقطابي والمجهر الضوئي، حيث تمّ الفحص باستخدام عدّادة نيوبار. لوحِظَ صِغَر أبعاد القطيرات عند زيادة نسب العوامل الاستحلابية في الصيغ، وكذلك تجانس أكبر في الأبعاد، حيث أبدتFS4+FS5 وFC4+FC5 أصغر أبعاد للقطيرات الملاحظة بالمجهر الضوئي. في الصيغ من (FS6-FS9) وكذلك من (FC6-FC9) اختفى ظهور القطيرات بشكل كامل من ساحات المجهر الضوئي، وبفحصها بالمجهر الاستقطابي كانت المستحلبات متماثلة الخواص isotropic، هذا يدل على الحصول على بنية مستحلبات دقيقة أبعادها أقل من 500 نم، حيث احتوت هذه الصيغ على نسب عوامل استحلابية تتجاوز 30%. بناء عليه تم اختيارFS6-FS9 و FC6-FC9 لمتابعة الدراسة حيث أن F6s+F6c تحويان على العوامل الاستحلابية بنسبة 31.5% والصيغ FS7+F7c بنسبة 35% والصيغ Fs8+Fc8 بنسبة 38% والصيغ FS9+FC9 بنسبة 40.9%، مع كميات ثابتة لبقية المكونات.
نتائج دراسة ذوبان الأسيكلوفير في المستحلبات:
من خلال تحضير كل صيغة من الصيغ الثمانية السابقة، واستخدام تراكيز من الأسيكلوفيربين 3ملغ/غ-20ملغ/غ مستحلب، وحضنها في جهاز هزاز (shaker)، تمّ مراقبة الخواص البصرية Optical properties، وقياس النفاذية transmittance بمقياس الطيف الضوئي، إن استخدام تراكيزتتراوح بين 3-4 ملغ /غ مستحلب لم يؤثر على النفاذية الضوئية للمستحلبات الدقيقة حيث كانت مشابهه لنفاذية المستحلبات الدقيقة دون إضافة الأسيكلوفير، وذلك وفقاً لنوع الزيت المستخدم ونسبة العوامل الفعالة على السطح، حيث تم تحميل الصيغة (FS9) ب 4 ملغ / مستحلب دون تغير في نفاذيتها، وكذلك الصيغ (FS8، FC9،FC8،FS7) تم تحميلها بــــ 3 ملغ/ غ مستحلب دون تغير في نفاذيتها، أما بالنسبة للصيغتين (FC6،FC7) قد تم تحميلهما بــ 2ملغ\غ دون تغير في النفاذية. كان المقدار الذي يمكن تحميله من الأسيكلوفير في كل صيغة مختلفاً باختلاف نوع الزيت ونسبة العوامل الاستحلابية، حيث كانت أفضل النتائج مع زيت دوار الشمس والنسبة الأعلى من مزيج العوامل الاستحلابية(43% تقريباً) كما في الصيغة FS9، حيث يتوزع الأسيكلوفير بين الطورين المائي والزيتي بصورة أفضل بارتفاع نسبة العوامل الاستحلابية، وبوجود زيت دوار الشمس حيث كانت الانحلالية البدئية للأسيكلوفير فيه أعلى من زيت الخروع، لوحظ الترسّب عيانياً ضمن الصيغ عند زيادة كمية الدواء.
تحري بلورات الأسيكلوفير في المستحلبات الدقيقة باستعمال المجهر الاستقطابي
تبين بدراسة الصيغ السابقة :
اختفاء بلورات الأسيكلوفير من الساحات المجهرية، مما يتوافق مع نتائج فحص النفاذية، حيث حافظت هذه الصيغ الحاوية على الأسيكلوفير على نفاذيتها مقارنة مع الصيغ الشاهدة.
يبين الشكلين التاليين (1-2) بلورات الأسيكلوفير في صيغ زيت دوار الشمس وزيت الخروع وذلك عند تراكيز لم يكن الدواء منحل فيها بشكل كامل.

الشكل (2): بلورات مادة الأسيكلوفير ضمن الصيغة FS7 بالمجهر الاستقطابي بتكبير 20
نتائج دراسة خصائص المستحلبات الدقيقة:
النفاذية الضوئية عند طول موجة 650 نم:
تراوحت قيم النفاذية للصيغ المحضرة بين 85.3 إلى 98.9%، حيث كانت أعلاها في FS9. يبين الجدول (4) التالي قيم النفاذية لبعض الصيغ.
| الجدول (4): قيم النفاذية للصيغ المحضرة | |
| Transmittance% | Formulation |
| 98.9 | FS9 |
| 98.1 | FS8 |
| 95.2 | FC9 |
| 94.7 | FC8 |
| 93.5 | FS7 |
| 91.9 | FS6 |
| 91.6 | FC7 |
| 90.1 | FC6 |
يبين الشكل التالي مظهر الصيغة FS9 والتي كانت الأعلى نفاذية للضوء:

درجة الحموضةPH :
باستخدام جهاز قياس درجة الحموضة (PH 211، HANNA، Italy) في درجة حرارة 25 درجة مئوية أبدت الصيغ قيمة درجات حموضة من (5.5) إلى (6.3) كما هو مبين في الجدول (5)، وهي مقبولة من الناحية الفيزيولوجية ومناسبة للتطبيق الموضعي وللتطبيق عبر الجلد وذك لأن قيمة PH الجلد تكون ضمن المجال التالي (5.5-7.0) (11)، وكذلك ملائمة للإعطاء الفموي حيث تتراوح درجة ال PH المناسبة للإعطاء الفموي من 5 إلى8. 18
دراسة أبعاد قطيرات المستحلبات بالــــ Mastersizer :
يعتبر حجم الجسيمات من أهم الاختبارات في تقييم المستحلبات الدقيقة, حيث أنه يؤثر بشكل مباشر على ثبات و تحرر الدواء. تم تحليل الصيغ الثمانية.
| الجدول (5): قيم درجات الحموضة للصيغ المحضرة | |
| PH | Formulation |
| 5.8±0.2 | FS9 |
| 5.6±0.6 | FS8 |
| 5.5± 0.2 | FS7 |
| 6.2±0.12 | FS6 |
| 6.3±0.5 | FC9 |
| 5.9±0.6 | FC8 |
| 6.1±0.2 | FC7 |
| 5.8±0.4 | FC6 |
تم تحديد متوسط حجم القطيرات Mean particle size، وتوزع الحجم Size distribution، وتجانس توزع الحجم Uniformity كما هو مبين في الجدول (6). تراوحت أبعاد القطيرات (Mean particle size(µm بين 1-3 مكم بتجانس توزع Uniformity تراوح بين 0،2-0،7، حيث بينت النتائج عبر Mastersizer أن الصيغ FS9 و FS8 كانت الأصغر من حيث الابعاد. لذلك تم قياس أبعاد القطيرات بجهاز Nanosizer.
| الجدول (6): نتائج قياس حجم قطيرات المستحلبات بـــ Mastersizer | |||||||
| SPAN | Specific surface area(m2/g) | Uniformity | Mean particle size (µm) | d
(0.9µm) |
D
(0.5µm) |
d
(0.1 µm) |
|
| 1.7 | 0.6 | 0.4 | 9.23 | 152.8 | 88.6 | 1.9 | FC6 |
| 2.4 | 4.2 | 0.7 | 1.4 | 14.8 | 5.8 | 0.4 | FC7 |
| 1.3 | 1.5 | 0.4 | 3.3 | 6.8 | 3.4 | 1.9 | FC8 |
| 1.8 | 1.5 | 0.5 | 3.7 | 10.6 | 4.2 | 1.9 | FC9 |
| 1.3 | 2 | 0.4 | 3.0 | 6.3 | 3.3 | 1.7 | FS6 |
| 2.4 | 1.9 | 0.7 | 1.0 | 8.4 | 3.3 | 0.2 | FS7 |
| 1.2 | 1.6 | 0.4 | 1.6 | 2.3 | 1.3 | 0.6 | FS8 |
| 1.0 | 1.8 | 0.2 | 1.0 | 2.6 | 1.7 | 1.1 | FS9 |
دراسة أبعاد قطيرات المستحلبات بـ Nanosizer:
يقيس جهاز mastersizer أبعاد القطيرات بأبعاد أكبر من(0.1) مكم، تم استخدام جهاز Nanosizer لقياس أبعاد القطيرات الأصغر من (100) نانومتر. يشير مقياس التشتت (Pdi<1) إلى تقارب حجم القطيرات، حيث أنه كلما قل التشتت كانت القطيرات أكثر تجانساً.
أظهر قياس الكمون زيت للصيغ FS8 و FS9 قيم قريبة من الصفر وهذا يتوافق مع بنيتها المكونة من عوامل استحلابية غير متأينة (السبان والتوين) وأبعادها 175 – 14 نم على الترتيب. أما بقية الصيغ كانت كبيرة الحجم تتجاوز ال 5 مكم. الجدول (7).
| الجدول (7): نتائج قياس حجم قطيرات الصيغتين FS8 وFS9 باستخدام Nanosizer | |||
| رمز العينة | Size nm | PDI | Zeta potential mV |
| FS8 | 175 | 0.86 | 0.16 |
| FS9 | 14.6 | 0.27 | 1.4 |
دراسات الثبات لأنظمة المستحلبات الدقيقة تحت الطرد المركزي:
في نهاية عملية الطرد المركزي ب 3500 دورة في الدقيقة لمدة نصف ساعة باستعمال المثفلة (HERMLE Z 200A،Germany) لم يشاهد أي فصل في الأطوار ولا ترسب الدواء، مما يشير إلى ثبات المستحلبات الدقيقة فيزيائياً.
نتائج دراسات التحرر في الزجاج:
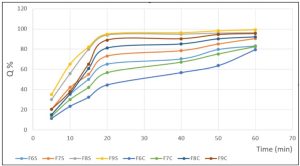
تمت دراسة التحرر في الزجاج باستخدام خلية فرانز على الصيغ السابقة.تبين أن الصيغتين FS9،FS8 هي أفضل الصيغ حيث تحرر أكثر من 90% من المادة الدوائية، تلاها الصيغتين FC8،FC9 حيث تحرر أكثر من 80% من المادة الدوائية بينما حررت FS7 ما يقارب 73% وحررت FS6 ما يقارب 65% وذلك خلال 20 دقيقة، ومن خلال الدراسة الاحصائية(ANOVA one way على الصيغ المشتركة بنوع الزيت والمختلفة بنسبة العوامل الاستحلابية تبين وجود وجود فرق جوهري(P<0.05، n=3) في التحرر عند كل نقطة زمنية من هذه الصيغ مما يبين أثر زيادة نسبة العوامل الاستحلابية في تحسين التحرر، وبالمقارنة بين الصيغ المشتركة بنسبة العوامل الاستحلابية والمختلفة بنوع الزيت باستدام اتبار Student’s t-test فأن التحرر أفضل بوجود زيت دوار الشمس مقارنة مع زيت الخروع وهذا يتوافق مع أبعاد قطيرات هذه الصيغ حيث بوجود زيت دوار الشمس كانت أبعاد القطيرات نانوية وكان التحرر أفضل. يبين الجدول (8) النسبة المئوية المتحررة من الأسيكلوفير من المستحلبات الدقيقة.
| الجدول (8): النسبة المئوية المتحررة للأسيكلوفير من المستحلبات الدقيقة لكل صيغة | ||||||||
| F6S | F7S | F8S | F9S | F6C | F7C | F8C | F9C | |
| Time (min) | Qave%±S.D. | Qave%±S.D. | Qave%±S.D. | Qave%±S.D. | Qave%±S.D. | Qave%±S.D. | Qave%±S.D. | Qave%±S.D. |
| 5 | 15،25±0،5 | 20،5± 0،1 | 30،21±1،3 | 35±0،3 | 11،5±0،2 | 13،5±0،2 | 15،21±0،5 | 20،5±1،2 |
| 10 | 35،26±0،5 | 42،1±0،3 | 55،85±1،2 | 65±0،9 | 23،5±0،2 | 30،2±0،2 | 36±1،4 | 38،22±0،3 |
| 15 | 50،25±0،8 | 55،2±0،1 | 79،75±0،5 | 82،21±0،4 | 32،4±0،1 | 42،2±1،1 | 60،8±0،2 | 65،26±0،8 |
| 20 | 65،25±0،6 | 73،3±0،5 | 93،95±1،2 | 95±1،7 | 44،6±0،1 | 56،7±1،5 | 81،12±0،3 | 88،95±0،1 |
| 40 | 70،36±0،6 | 78،6±0،9 | 94،58±1،6 | 96،33±1،5 | 56،8±0،2 | 67،1±1،5 | 85،19±1،4 | 90،25±0،2 |
| 50 | 79،69±1،3 | 85،2±0،6 | 95،86±1،1 | 98،22±0،1 | 63،7±0،1 | 75،2±0،1 | 90،21±1،5 | 94،35±0،5 |
| 60 | 83،22±1،6 | 90،6±0،9 | 96،21±0،9 | 99،23±0،1 | 79،5±0،2 | 82،4±0،2 | 92،15±0،2 | 95،36±0،3 |
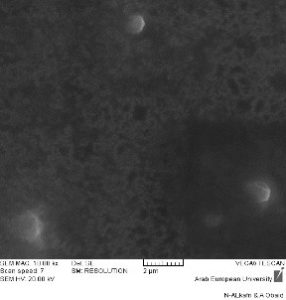
نتائج المجهر الالكتروني الماسح (SEM):
أظهر المجهر الالكتروني الماسح أن سطح قطيرات الطور الداخلي للصيغ الأمثل (FS8، FS9) أنها قطيرات كروية ملساء. الشكل (5)
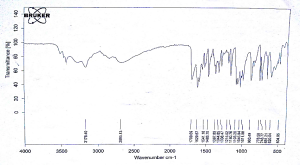
- دراسة مخططات طيف الأشعة تحت الحمراء IR:
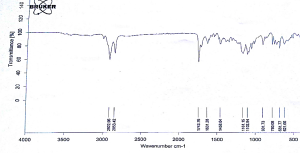
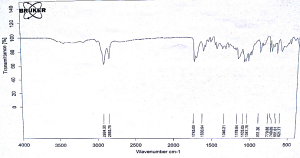
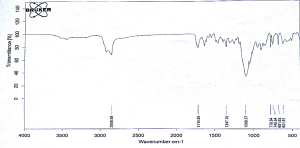
تم استخدام FTIR BUKER و فحص المواد النقية والأمزجة الفيزيائية لها وبنسبة وزنية تساوي (w/w)% 50/50، أبدى طيف الأشعة تحت الحمراء الناتج عن مزج الأسيكلوفير مع السواغ المدروس انخفاض في شدة بعض القمم المميزة للأسيكلوفير النقي بسبب التأثير الممدد للسواغ، ووجد بعض التأثيرات الخفيفة عند أعداد موجة 1000-1800 حيث لوحظ تآثر بين الأسيكلوفير وزيت الخروع، زيت دوار الشمس، السبان 80 والتوين 80 عند 1709، 1483 وعند 1180 سم -1 وفي المجال من 2900-3300 لوحظت التاثرات لذلك عند 3306، 2928 سم -1 وذلك قد يعزى إلى تشكل روابط هيدروجينية بين الأسيكلوفير وال PEG200، التوين 80 والسبان 80.
يبين الشكل(7) طيف الأشعة تحت الحمراء الأسيكلوفير حيث تظهر قمة عند (3500) سم-1 موافقة لامتطاط O-H))، وقمة عند (3400) تعود لامتطاط الأمين الأولي، وقمة عند (2937) توافق الامتطاط المتماثل لــ C-H الأليفاتية وعند(2854) توافق الامتطاط غير المتماثل لC-H الأليفاتية، وقمة عند (1709) تعود لامتطاط الكربونيل، وقمة (1103) تعود لامتطاط (C-O)، وقمة مميزة (1483) تعود لامتطاط الرابطة المضاعفة الكربونية في الحلقة العطرية.
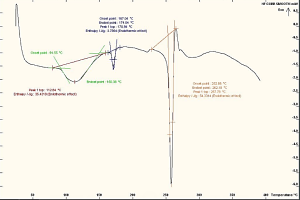
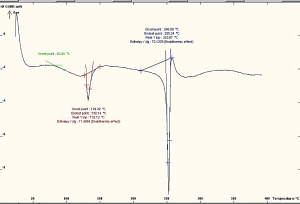
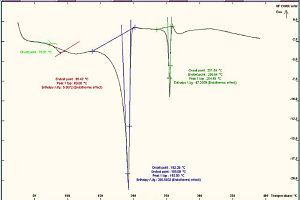
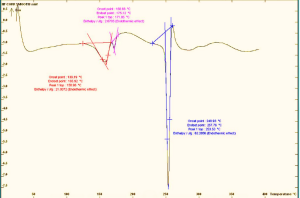
المسح الحراري التفاضلي DSC:
تم اجراء المسح الحراري التفاضلي باستخدام (DSC131، SETARAM)، توضح الأشكال التالية (11,12,13,14) مخطط المسح الحراري التفاضلي DSC (thermo gram) لكل من الأسيكلوفير وعينات من المزائج الفيزيائية لمادة الأسيكلوفير مع السواغات المدروسة بنسب (1:1)، حيث كانت متقاربة فيما بينها فقد أبدت جميعها قمة حادة ماصة للحرارة Endothermic تعزى الى انصهار الأسيكلوفير، والذي يظهر حالتها البلورية crystal structure، والتي ذروتها عند 257.78 م°، مما يؤكد هوية المادة. مع انزياحات بمقادير ضئيلة في بعض المزائج.
الاستنتاجات Conclusions
- تم الحصول على مستحلبات دقيقة ثابتة فيزيائيا و قادرة على على حل الاسكليوفير و تحريره.
- كانت الصيغة FS9 , FS8 ذوات أبعاد نانوية حررت الأسكليوفير أكثر من 90% خلال 20 دقيقة.
كان التركيز و نسبة العوامل الفعالة سطحياً وPEG200 تأثير واضح على الخواص الفيزيوكيميائية للمستحلبات، وعلى التحرر.
المراجع :- Arnal J. et al. Biowaiver monographs for immediate release solid oral dosage forms: aciclovir. J Pharm Sci 97:5061–73. 2008
- Fletcher C. and Bean B. Evaluation of oral acyclovir therapy. Drug Intell Clin Pharm 19:518–24.. 1985
- Laskin OL. Clinical pharmacokinetics of acyclovir. Clin Pharmacokinet 8:187–201. 1983
- Johnson GL. Limon L. Trikha G. and Wall H. Acute renal failure and neurotoxicity following oral acyclovir. Ann Pharmacother 28:460–3. 1994
- Wagstaff AJ. Faulds D. and Goa KL. Acyclovir: a reappraisal of its antiviral activity، pharmacokinetic properties and therapeutic efficacy. Drugs 47:153–205. 1994
- Friedrichsen GM. et al. Synthesis of analogs of L-valaciclovir and determination of their substrate activity for the oligopeptide transporter in Caco-2 cells. Eur J Pharm Sci 16: 1–13. 2002
- Bergstrom CA.et al. Absorption classification of oral drugs based on molecular surface properties.J Med Chem 46:558–70. 2003
- Spruance SL. et al. Acyclovir cream for treatment of herpes simplex labialis: results of two randomized، double- lind، vehicle-controlled، multicenter clinical trials.Antimicrob Agents Chemother 46:2238–43. 2002
- Prajapat MD. Patel NJ. Bariya A. and Patel SS. Formulation and evaluation of self-emulsifying drug delivery system for nimodipine, a BSC Class II drug. J Drug Deliv Sci Technol. 39:59-68. 2017
- Singh B. Bandopadhyay S. Kapil R. Singh R. and Katare O. Self Emulsifying Drug Delivery Systems (SEDDS): Formulation Development، Characterzation، And Applications. Crit Rev Ther Drug Carr Syst. 26(5):427-451. 2009
- Wang J. Lu C. Liu Y. Wang C. and Chu F. Preparation and characterization of natural rosin stabilized nanoparticles via miniemulsion polymerization and their pressure-sensitive adhesive applications. Industrial Crops and Products، 124، 244-253. 2018
- Du Y. Chen H. Chen R. and Xu N. Synthesis of p-aminophenol from p-nitrophenol over nano-sized nickel catalysts. Applied Catalysis A: General،277(1-2)، 259-264. 2004
- Ghosh P. K. Majithiya R. J. Umrethia M. L. and Murthy R. S. Design and development of microemulsion drug delivery system of acyclovir for improvement of oral bioavailability. 2006
- Roland I. Piel G. Delattre L. and Evrard B. Systematic characterization of oil-in-water emulsions for formulation design. International journal of pharmaceutics،263(1-2)، 85-94. 2003
- K et al. Evaluation and characterization of different polymers based drug theophylline in pulsatile drug delivery system. The pharma innovation. 1(7): 105-112. 2012
- M. and Srinivas.N. Preparation and evaluation of immediate release celecoxib tablets. International journal of innovative pharmaceutical sciences and research. 2(10): 2272-2282. 2014
- Pavithra R. Sangeetha M. Senthilnathan B. and RavichandiranV. Formulation and evaluation of chronopharmaceutical drug delivery system. Int.J.PharmTech Res; 6(3): 1124-1130. 2014
- Maleki Dizaj S. Preparation and study of vitamin A palmitate microemulsion drug delivery system and investigation of co-surfactant effect. Journal of nanostructure in chemistry، 3(1)، 1-6. 2013
- Kumar B. Jain S. K. Prajapati S. K. Mahor A. and Kumar ADevelopment and characterization of transdermal microemulsion gel for an antiviral drug. International Journal of Pharmaceutical Sciences and Research،1(6)، 57-74. 2010