تحسين معدل انحلال الاسيكلوفير المضاد الفيروسي باستخدام تقنية المبعثرات الصلبة المحضرة بطريقة الطحن
2023-07-01 | المجلد السابع العدد الثاني - المجلد السابع | مقالات بحثيةإيناس محمد أنيس دياربكرلي | هند الزين
الملخص
يهدف البحث إلى تحسين معدل انحلال الاسيكلوفير(ACV) المضاد الفيروسي باستخدام تقنية المبعثرات الصلبة المحضرة بطريقة الطحن، وتقييمها من خلال دراسة معدل الانحلال و السلوك الحراري والمسح الطيفي بالأشعة تحت الحمراء للمبعثر الصلب المحضر. تم تحضير المبعثرات الصلبة لمادة (ACV) مع كل من غليكولات النشاء الصودية (SSG) و بولي ايتلين غليكول 6000 (PEG6000) بنسبة (1:1) بطريقة الطحن باستخدام مطحنة الكرات، ثم تمت دراسة معدل تحرر الاسيكلوفير من المضغوطات الحاوية على المبعثرات المحضرة مقارنة مع المستحضر المحلي و المستحضر العالمي (®ZOVIRAX)، وانتقاء المبعثر الذي أعطى التحرر الأفضل، وإجراء مقارنة بين المادة النقية والمبعثر المحضر من خلال المسح الحراري التفاضلي (DSC) و المسح الطيفي بالأشعة تحت الحمراء (FTIR). أظهرت النتائج تشكل مبعثر صلب للاسيكلوفير (ACV) مع غليكولات النشاء الصودية (SSG) حيث ازداد معدل تحرر (ACV) من المضغوطات الحاوية على المبعثر المحضر مقارنة مع المستحضر المحلي وكان مماثلاً لتحرر الاسيكلوفير من المستحضر العالمي (®ZOVIRAX)، و لا يوجد بينهما فروق يعتد بها احصائياً باستخدام توزيع ستيودينت عند (P < 0.05), وبين فحص التحليل الحراري انخفاض قيمة ΔH للمبعثر مقارنة مع المادة النقية والذي قد يعود إلى تواجد جزء من مادة الاسيكلوفير بشكلها اللا بللوري وأظهر مخطط (FTIR) انزياح قمة امتطاط C-O)) للمبعثر المحضر.
كلمات مفتاحية : الاسيكلوفير، المبعثرات الصلبة، الطحن، معدل الانحلال.
المقدمة Introduction
واجهت الصناعة الدوائية وعلم تطوير الدواء العديد من التحديات ولعل أبرزها سوء انحلال المادة الدوائية الذي يشكل العائق الأساسي في الوصول إلى توافر حيوي جيد للدواء. ولمواجهة هذه التحديات الصيدلانية تم إيجاد العديد من الطرق التي من شأنها أن تساعد في تحسين انحلال المادة الدوائية منها تشكيل المبعثرات الصلبة, تحضير البللورات النانوية, استخدام معقدات السايكلوديكسترين وغيرها من الطرق الأخرى. 1 ومع الازدياد المتسارع لعدد المستحضرات الموافق عليها من قبل منظمة الدواء والغذاء (FDA) في السنوات الأخيرة تم ترسيخ المبعثرات الصلبةSolid Dispersions (SD) كتقنية أساسية لصياغة الأدوية ضعيفة الانحلال.2 ومن أهم مميزات المبعثرات الصلبة تخفيض حجم أجزاء الدواء وبالتالي زيادة سطح التماس النوعي له مما يؤدي إلى زيادة سرعة انحلال الدواء و زيادة التوافر الحيوي, كما تعمل على زيادة خواص التبلل للمادة الدوائية وبالتالي زيادة الذوبانية, كما لوحظ زيادة المسامية في أجزاء المبعثرات الصلبة مما حسن بدوره من تحرر الدواء, بالإضافة إلى تواجد الدواء غالباً بشكله اللابللوري في المبعثر الصلب مما يزيد من ذوبانية الدواء.3 إلا أن هناك بعض المشاكل التي تحد من تحضير المبعثرات الصلبة منها المشاكل المرافقة لصياغتها في أشكال جرعية مناسبة بالإضافة إلى مشاكل الثبات الفيزيائية والكيميائية لكل من الدواء والحامل. حيث أنه من الملاحظ عدم استخدام المبعثرات الصلبة بشكل كبير في المنتجات التجارية وهذا يعود بشكل أساسي إلى تحول المادة الدوائية في بعض الأحيان من الشكل اللابللوري إلى البللوري الأكثر ثباتاً سواءً بتأثير عمليات التصنيع اللاحقة نتيجة الطاقة المقدمة او أثناء التخزين بتأثير الرطوبة والتي تعمل على زيادة حركية الجزيئات وبالنتيجة التحول للشكل البللوري مما ينقص بالنهاية من سرعة تحرر الدواء.4 يتم تحضير المبعثرات الصلبة بالعديد من الطرق منها طريقة الصهر بحيث يصهر مزيج الدواء والحامل بشكل متزامن وبعد التبريد والمجانسة تتم القولبة على شكل مضغوطة، حثيرات، حبيبات أو بودرة. ممكن للأشكال المتوسطة أن تصنع فيما بعد لتحضير المضغوطات التقليدية, إنّ الميزة الأساسية لهذه الطريقة أنّ مزيج الدواء والحامل يتعرضان لحرارة متزايدة لمدة قصيرة من الزمن مما يجعل الأدوية غير المستقرة حرارياً سهلة التحضير باستخدام هذه الطريقة5 وقد استخدم Sekiguchi هذه الطريقة لتحضير مزيج أصهري بسيط للسلفاتيازول مع اليوريا.6 ومن الطرق أيضا طريقة تبخير المحل حيث يتم حلّ كل من الدواء و الحامل في محل شائع ثمّ تبخير هذا المحل لصناعة المبعثر الصلب, من المتطلبات الأساسية لتحضير المبعثرات الصلبة بهذه الطريقة أن يكون الدواء والحامل منحلان في المحلّ المستخدم, ومع اكتشاف طريقة المحلات تمّ حل العديد من المشكلات المرافقة لطريقة الصهر. حيث أصبح من الممكن تحضير مبعثرات صلبة من المواد الحساسة للحرارة, بالإضافة إلى القدرة على استخدام العديد من البلمرات التي كانت غير ملائمة لطريقة الصهر بسبب درجة انصهارها المرتفعة كالبوفيدون, إلا أنّه مع مرور الوقت وبسبب المشاكل البيئية والاقتصادية المترافقة مع استخدام المحلات والبلمرات العضوية أدى ذلك إلى جعل طريقة المحلات أكثر اشكالية.7وقد استخدم هذه الطريقة Mayersohn لتحضير مبعثر الغريزوفولفين ضمن البوفيدون.8 كما هناك طريقة الطحن وقد بدأ استخدام طريقة الطحن المشترك للمادة الدوائية والسواغ الحامل في تحضير المبعثرات الصلبة عندما لوحظ بأنها من أكثر الطرق أماناً, فعلى عكس الطرق السابقة لا تتضمن هذه الطريقة استخدام المحاليل السامة التي من الصعب التخلص منها بشكل نهائي من المبعثر المحضر, بالإضافة إلى التكلفة المنخفضة المرافقة لاستخدام هذه الطريقة مقارنة بالطرق السابقة, كما أنها تعد من الطرق البسيطة التي لا تحتاج لوقت طويل نسبياً أو أدوات معقدة, و لاتحتاج إلى الحرارة وبالتالي فهي تناسب المواد الدوائية الحساسة للحرارة. فغالباً ما يتم استخدام حوامل خاملة غير سامة وبنسب مختلفة, وبشكل عام يتم الطحن بالحالة الجافة لكل من الدواء والسواغ حيث تؤدي الطاقة الميكانيكية المقدمة إلى تآثرات بين الدواء والسواغ والارتباط بقوى من نمط فاندرفالس وروابط هيدروجينية, وتكون أجزاء المبعثرات الناتجة ثابتة وتبدي ميلاً قليلاً للتكتل, وتتم عملية الطحن باستخدام عدة طرق منها الطحن بالطاقة المتدفقة fluid energy milling عن طريق الهواء النافث air jet milling ومن الطرق أيضاً المستخدمة مطحنة الكرات وهي عبارة عن وعاء يمتلئ بالكرات ويتم وضع المواد المراد طحنها ضمنه حيث يدور أو يهتز بسرعة وبتواتر محدد. تؤدي حركة الوعاء إلى حركة الكرات بنمط محدد مصطدمة مع بعضها البعض وبالجدار الداخلي للوعاء. ويتأثر حجم الأجزاء الناتج بمقدار الصدم الذي تتلقاه المادة من الكرات كما يؤثر عدد الكرات الموضوعة وكمية المادة البدئية بشدة عملية الطحن المطبقة.7 ولقد تم استخدام مطحنة الكرات في العديد من المزائج لتحضير مبعثرات صلبة ساعدت على تحسين معدل انحلال العديد من الأدوية,1 من هذه المبعثرات مبعثر الغريزوفولفين مع كربوكسي ميتيل سيللوز, مبعثر الكاربامازبين مع الكروس بوفيدون 9والتي أوضحت تواجد الدواء بشكله اللابللوري وتحسن كل من سرعة تحرر الدواء وتوافره الحيوي, مبعثر كلور ديازيبوكسيد مع البوفيدون10 وكذلك مبعثر الايبوبروفن ضمن هيدروكسيد الألمنيوم حيث تم استخدم تقنية مطحنة الكرات في تحضير هذا المبعثر.11 يهدف البحث إلى تحسين معدل انحلال الاسيكلوفير(ACV) ذو الانحلال الضعيف من خلال تحضير مبعثرات صلبة باستخدام حوامل محبة للماء (غليكولات النشاء الصودية, البولي ايتلين غليكول 6000), وتحضير مضغوطات منها و دراسة معدل تحرر مادة الاسيكلوفير لدراسة تأثير الحامل المستخدم على مرتسم تحرر المادة الدوائية.
المواد والطرائق Materials and Methods
المواد Materials:
في هذه الدراسة تم الحصول على: الاسيكلوفير من شركة Rackshit الهندية, غليكولات النشاء الصودية من شركة JRS Pharma الهندية, البولي ايتلين غليكول 6000 من شركة JRS Pharma الهندية, هيدروكسي بروبيل ميتيل سيللوز من شركة JRS Pharma الهندية, شمعات المغنزيوم من شركة JRS Pharma الهندية, الكروس بوفيدون من شركة BASF الألمانية.
الأجهزة Instrumentation:
تم استخدام الأدوات التالية:ميزان حساس نموذج Sartorius GP2102ألمانيا, مناخل دستورية CISA-Sieve Shaker RP-09 اسبانيا, آلة ضغط مخبرية وحيدة المكبس ERWEKA الألمانية, مطحنة الكرات من شركةVEB Kombinat الألمانية, جهاز المسح الحراري التفاضلي DSC نموذج DSC131 فرنسا, وجهاز مقياس طيف الأشعة تحت الحمراءInfra-Red من شركة Bruker, جهاز فحص الذوبان Pharmatest نموذج PTWS610 ألمانيا, وجهاز مقياس الطيف الضوئي نموذجCary الأمريكي.
الطرائق Methods:
تم تحضير المبعثرات الصلبة ومن ثم تحضير مضغوطات منها بطريقة الضغط المباشر.
تحضير المبعثرات الصلبة:
تمت عملية التحضير باستخدام مطحنة الكرات وفق ما يلي, تم تحضير مزائج فيزيائية بنسب وزنية (1:1) لكل من الاسيكلوفير(ACV) مع غليكولات النشاء الصودية, والبولي ايتلين غليكول 6000, بالتسلسل حسب النسب السابقة, تم وضع كل مزيج في وعاء مطحنة الكرات المصنوع من البورسلان ذو السعة 6 ل بحيث كان يحوي 90 كرة من البورسلان ذات قطر يتراوح بين 2.5سم إلى 3 سم بحيث تم الطحن لمدة ساعة زمنية بتواتر 300دورة في الدقيقة. ثم تم النخل لمجانسة الأبعاد وتم حفظ المبعثر الناتج في المجفف الحاوي على كلور الكالسيوم لاجراء المراحل اللاحقة.
تحضير المضغوطات الحاوية على المبعثر الصلب بطريقة الضغط المباشر:
تم تحضير مضغوطات من المبعثرات الصلبة الناتجة الحاوية على الاسيكلوفير بجرعة 200ملغ بطريقة الضغط المباشر DCبحيث احتوت على هيدروكسي بروبيل ميتيل سيللوز كعامل رابط بنسبة 1% و الكروس بوفيدون كعامل مفتت بنسبة 2% بالرغم من وجود SSG في المبعثر الأول المستخدم وذلك لتوحيد الصيغة بين المضغوطتين المحضرتين وشمعات المغنزيوم كعامل مزلق بنسبة 0.25%, وذلك بوزن كلي للمضغوطة 415ملغ, يوضح الجدول (1) صيغة مضغوطات المبعثر الصلب.
| الجدول (1): صيغة مضغوطات المبعثر الصلب | |
| المادة | الكمية في المضغوطة (ملغ) |
| المبعثر الصلب (الاسيكلوفير:السواغ) (1:1) (وزن /وزن) | 400 |
| هيدروكسي بروبيل ميتييل سيللوز (عامل رابط 1%) | 4.15 |
| الكروس بوفيدون(عامل مفتت 2%) | 8.3 |
| شمعات المغنزيوم(عامل مزلق 0.25 %) | 1.03 |
| الوزن الكلي (total weight) | 415 |
دراسة تحرر المادة الفعالة في الزجاج In Vitro Dissolution Study:
تم دراسة معدل تحرر وانحلال المادة الفعالة لكل من المستحضر العالمي (Zovirax®) (تحوي 200 ملغ ACV بوزن كلي 500 ملغ) والمستحضر المحلي( تحوي 200 ملغ ACV بوزن كلي 300ملغ) ومضغوطات المبعثر الصلب. حيث تم اعتماد الطريقة الدستورية USP 43 NF 39 بحيث تم استخدام المجداف Apparatus IIووسط من حمض كلور الماء عشر نظامي بدرجة حرارة 37م وسرعة دوران (50) دورة / الدقيقة, و تم تحديد كمية الاسيكوفير المتحررة خلال الزمن بسحب عينات حجمها 5 مل عند فواصل زمنية مختلفة (5-10-15-20-30-45) دقيقة وترشيحها عبر مراشح ميكروية (0,45) ميكرون وتعويضها بكميات مساوية من وسط الانحلال, ثم تم حساب كمية مادة الاسيكلوفير المتحررة بقياس امتصاصها باستخدام جهاز مقياس الطيف لضوئي بالأشعة فوق البنفسجية عند طول موجة 256نانومتر. أجري الفحص على ستة مضغوطات من كل مستحضر للتأكد من تحقيقها للشرط الدستوري من حيث معدل الانحلال وتم أخذ نتيجة تحرر ثلاثة مضغوطات من كل مستحضر للمقارنة الاحصائية باستخدام توزيع ستيودينت لأنه أدق إحصائياً و تم حساب المتوسط الحسابي والانحراف المعياري.
المسح الطيفي بالأشعة تحت الحمراء (FTIR Spectroscopy):
تم إجراء مسح طيفي بالأشعة تحت الحمراء للمبعثر الذي أعطى معدل تحرر أفضل لمادة الاسيكلوفير في المضغوطات المحضرة وهو مبعثر الاسيكلوفير مع غليكولات النشاء الصودية بنسبة (1:1), كما أجري مسح طيفي لكل من مادة الاسيكلوفير وغليكولات النشاء الصودية بحيث تم القياس مباشرة دون الضغط مع بروميد البوتاسيوم وتم تسجيل الأطياف ضمن المجال (400 – 4000) سم -1.
التحليل الحراري باستخدام الماسح الحراري التفاضلي Differential Scanning Calorimetry:
تم إجراء الفحص لكل من الاسيكلوفير وغليكولات النشاء الصودية والمبعثر الصلب الناتج منهما بنسبة (1:1), حيث تم وزن (4-5) مغ من كل عينة ووضعها في بوتقة خاصة مصنوعة من الألمنيوم وتم إحكام إغلاقها جيداً بواسطة مكبس خاص وتم إجراء الاختبار مع استخدام بوتقة فارغة من الألمنيوم كشاهد وذلك بتعريض العينات إلى حرارة بمعدل متزايد قدره 10 °م/ دقيقة ضمن مجال مسح يتراوح بين (25-200 )ᵒم.
النتائج والمناقشة Results and Discussion
نتائج فحص الانحلال:
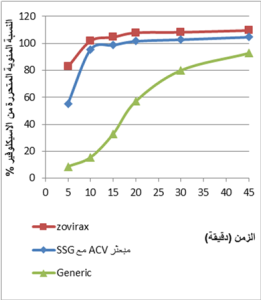
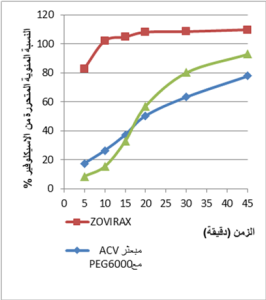
عند دراسة معدل انحلال الاسيكلوفير من المستحضر المحلي والمضغوطات المحضرة من المبعثر الصلب الحاوي على(ACV) و(SSG) بنسبة (1:1) (الشكل 1) لوحظ أن المضغوطات المحضرة من المبعثر الصلب تبدي معدل تحرر أفضل من المستحضر المحلي يعتد به احصائيا عند جميع النقاط المدروسة وذلك باستخدام توزيع ستيودينت ثنائي الذيل عند مستوى دلالة (P<0.05). كما أبدت معدل تحرر للاسيكلوفير مماثلة لمعدل تحرره من المستحضر العالمي(®ZOVIRAX) عند جميع النقاط الزمنية وهذا يعود إلى ما يتمتع به (SSG) من قبطه الشديد للماء والذي بدوره يؤدي إلى تبلل أفضل للمادة الدوائية في وسط الذوبان بالإضافة إلى خفض حجم أجزاء الدواء والناتج عن الطريقة المتبعة أثناء تحضير المبعثر الصلب بالإضافة إلى ما يتمتع به من قدرة عالية على التفتيت والتي تؤدي إلى تفتت المضغوطة بشكل سريع وبالتالي زيادة معدل الانحلال12. مع العلم أنه تم تحضير مبعثر من الاسيكلوفير مع غليكولات النشاء الصودية بنسبة (2:1) والمقارنة مع النسبة (1:1) ولم يكن هناك فروق يعتد بها احصائياً من حيث معدل تحرر مادة ااسيكلوفير لذلك تم انتقاء المبعثر بنسبة (1:1) للمقارنة مع المستحضر المحلي والعالمي بحيث تم استعمال نسبة أقل من السواغ المستخدم. أما عند دراسة معدل ذوبان الاسيكلوفير من المستحضر المحلي والمضغوطات المحضرة من المبعثر الصلب الحاوي على (ACV) و(PEG6000) بنسبة (1:1) ( الشكل 2) لوحظ تحسن معدل تحرر الاسيكلوفير عند 10 دقائق ثم تساوى معدل التحرر عند 15 دقيقة ثم كان أفضل للقرص المحلي مقارنة مع المضغوطات الحاوية على مبعثر ACV مع PEG6000 بحيث كانت الفروقات عند (20-30-45) دقيقة يعتد بها احصائياً وذلك وفق توريع ستيودينت ثنائي الذيل. أما عند المستحضر العالمي فقد تبين أن معدل تحرر الاسيكلوفير منه كان أعلى عند جميع النقاط الزمنية مما يشير إلى أن استخدام PEG6000 لم يؤدِ إلى تحسين معدل تحرر الاسيكلوفير وذلك قد يعود لتحسين فعالية المواد الرابطة في القرص وإطالة زمن التفتت عند استخدامها بتراكيز أكبر من 5% (و/و) في الصيغ.13
المسح الطيفي بالأشعة تحت الحمراء(FTIR Spectroscopy):
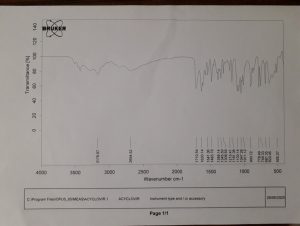
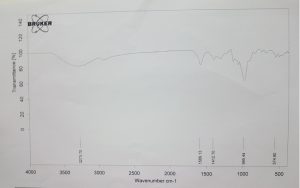
أظهر طيف امتصاص الأشعة تحت الحمراء لمادة الاسيكلوفير (الشكل 3) قمتي امتصاص مميزة عند (3439) سم-1 وعند (3178)سم-1 موافقة لامتطاط (N ̶ H) للأمين الأولي والثانوي، وقمة امتصاص مميزة عند (1710 ) سم-1 تعود إلى امتطاط مجموعة الكربونيل(C=O)، وقمة امتصاص مميزة عند (1630) سم-1 تعود إلى امتطاط مجموعة(C ̶ N) وقمة امتصاص مميزة (1388) سم-1 تعود إلى انحناء مجموعة(C ̶ OH).14 كما يبدي طيف امتصاص الأشعة تحت الحمراء لمادة غليكولات النشاء الصودية (الشكل 4) قمة امتصاص عند (3273) سم -1والموافقة لامتطاط مجموعة (( –OH وقمة امتصاص مميزة عند (2927)سم -1 والموافقة لاهتزاز مجموعة(C-H) وقمتي امتصاص عند (1618-1424) سم -1 والموافقة لاهتزاز (COO – ).15 يظهر طيف الأشعة تحت الحمراء للمبعثر الصلب لمادة الاسيكلوفير مع غليكولات النشاء الصودية وذلك بنسبة (1:1) (الشكل 5) عصابات الامتصاص الأساسية البارزة والمميزة لمادة الاسيكلوفير، بحيث يمكن اعتبار طيف امتصاص الأشعة تحت الحمراء للمبعثر الصلب هو ناتج اضافة طيف امتصاص الأشعة تحت الحمراء للاسيكلوفير إلى طيف امتصاص الأشعة تحت الحمراء لغليكولات النشاء الصودية مع انخفاض بسيط في شدتها بسبب التأثير الممدد للسواغ حيث حافظت قمم الامتصاص الخاصة بمادة الاسيكلوفير على موضعها مع ملاحظة انزياح قمة امتطاط (C-O) من (1103) سم -1إلى (1081) سم -1 مما قد يشير إلى تغير الشكل البللوري للاسيكلوفير .16

المسح التفاضلي الحراريDSC:
يظهر المسح الحراري التفاضلي لمادة الاسيكلوفير حالتها البلورية Crystal Structure كما هو واضح في الشكل (6) حيث يبين وجود قمة حادة ماصة للحرارة (endothermic peak) هي قمة انصهار المادة الدوائية وتبلغ ذروتها عند 249.23°م والتي توافق مجال الانصهار المرجعي للمادة الدوائية16 بالإضافة لوجود قمتي تحول (transition) ماصتين للحرارة الأولى تبلغ ذروتها عند درجة 110.94°م والثانية تبلغ ذروتها عند درجة 171.71°م.
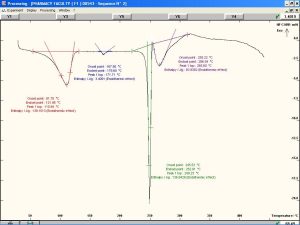
كما يبين مخطط المسح الحراري التفاضلي لغليكولات النشاء الصودية الشكل (7) ظهور قمة وحيدة ماصة للحرارة تبلغ ذروتها عند 82.30 °م وهي توافق تبخر الماء المُدمص بالإضافة إلى قمة ناشرة للحرارة تبلغ ذروتها عند درجة 279.30°م والتي توافق درجة تخرب المادة حيث أن مسحوق غليكولات النشاء الصودية هو مسحوق جاذب للرطوبة hygroscopic لا يبدي أية قمة انصهار وإنما يبدأ بالتفحم بعد الدرجة 200°م .17
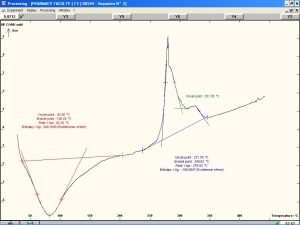
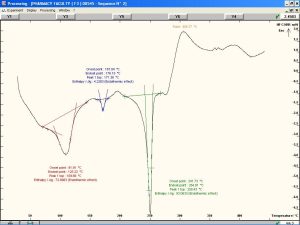
ويوضح الشكل(8) منحني المسح الحراري التفاضلي للمبعثر الصلب الحاوي على الاسيكلوفير وغليكولات النشاء الصودية بنسبة 1:1 حيث نلاحظ انخفاض قيمة ΔH من 136.84إلى 83.06 مع اتساع عرض قمة الانصهار والذي قد يعود إلى تواجد جزء من مادة الاسيكلوفير بشكلها غير البللوري وبالتالي تشكل المبعثر الصلب حيث يؤدي تواجد جزء من المادة بشكلها غير البللوري إلى انخفاض قيمة الطاقة المطلوبة لتحطيم البنية البللورية.18
الاستنتاجات Conclusions
ناقشت هذه الدراسة تحضير مبعثر صلب لمادة الاسيكلوفير بالاعتماد على طريقة الطحن باستخدام مطحنة الكرات وأظهرت تشكل مبعثر صلب للاسيكلوفير مع غليكولات النشاء الصودية و تبين ذلك من خلال ازدياد معدل انحلال الاسيكلوفير من المضغوطات الحاوية على هذا المبعثر بالاضافة إلى التغيرات الحاصلة في مخطط المسح الحراري التفاضلي للمبعثر الصلب مقارنة مع المادة النقية والمسح الطيفي بالأشعة تحت الحمراء, في حين لم يظهر المبعثر المحضر من الاسيكلوفير مع بولي ايتلين غليكول 6000 تحسن في معدل انحلال الاسيكلوفير من المضغوطات الحاوية على المبعثر السابق. ومنه يمكن اعتبار مضغوطات المبعثرات الصلبة للاسيكلوفير مع غليكولات النشاء الصودية بديل واعد عن المستحضر العالمي.
المراجع :- Loh, Z. H., Samanta, A. K. & Sia Heng, P. W. Overview of milling techniques for improving the solubility of poorly water-soluble drugs. Asian J. Pharm. Sci. 10, 255–274 (2015).
- Mohapatra, D., Agrawal, A. K. & Sahu, A. N. Exploring the potential of solid dispersion for improving solubility, dissolution & bioavailability of herbal extracts, enriched fractions, and bioactives. J. Microencapsul. 38, 594–612 (2021).
- Bhowmik, D. et al. Solid Dispersion-A approach to enhance the dissolution rate of poorly water soluble drugs. Pharma Innov. 1, 24–38 (2012).
- Cid, A. G., Simonazzi, A., Palma, S. D. & Bermúdez, J. M. Solid dispersion technology as a strategy to improve the bioavailability of poorly soluble drugs. Ther. Deliv. 10, 363–382 (2019).
- Williams, H. D. et al. Strategies to address low drug solubility in discovery and development. Pharmacological Reviews vol. 65 315–499 (2013).
- Saffoon, N., Uddin, R., Huda, N. H. & Sutradhar, K. B. Enhancement of oral bioavailability and solid dispersion: A review. J. Appl. Pharm. Sci. 1, 13–20 (2011).
- Zhang, X., Xing, H., Zhao, Y. & Ma, Z. Pharmaceutical dispersion techniques for dissolution and bioavailability enhancement of poorly water-soluble drugs. Pharmaceutics vol. 10 (2018).
- Leuner, C. & Dressman, J. Improving drug solubility for oral delivery using solid dispersions. Eur. J. Pharm. Biopharm. 50, 47–60 (2000).
- Iqbal, B. et al. Recent Advances and Patents in Solid Dispersion Technology. Recent Pat. Drug Deliv. Formul. 5, 244–264 (2011).
- Nokhodchi, A., Talari, R., Valizadeh, H. & Jalali, M. B. An investigation on the solid dispersions of chlordiazepoxide. Int. J. Biomed. Sci. 3, 211–6 (2007).
- Mallick, S. et al. Physicochemical characterization of interaction of ibuprofen by solid-state milling with aluminum hydroxide. Drug Dev. Ind. Pharm. 34, 726–734 (2008).
- Li, J. Sodium starch glycolate. in Handbook of Pharmaceutical Excipients 757–760 (2012).
- Row, R. C. Polyethylene Glycol. in Handbook of Pharmaceutical Excipients (ed. Row, R. C.) 517–522 (2009).
- Bruni, G. et al. Preparation and physicochemical characterization of acyclovir cocrystals with improved dissolution properties. J. Pharm. Sci. 102, 4079–4086 (2013).
- Panwar, V. et al. In-vitro and in-vivo evaluation of modified sodium starch glycolate for exploring its haemostatic potential. Carbohydr. Polym. 235, (2020).
- Lutker, K. M., Quiñones, R., Xu, J., Ramamoorthy, A. & Matzger, A. J. Polymorphs and hydrates of acyclovir. J. Pharm. Sci. 100, 949–963 (2011).
- Young, P. M., Edge, S., Staniforth, J. N., Steele, D. F. & Price, R. Dynamic Vapor Sorption Properties of Sodium Starch Glycolate Disintegrants. Pharm. Dev. Technol. 10, 249–259 (2005).
- Al-Obaidi, H. et al. Effect of drug-polymer interactions on the aqueous solubility of milled solid dispersions. Int. J. Pharm. 446, 100–105 (2013).