دراسة ارتباط بين انخفاض الوزن والخضاب الغلوكوزي عند مرضى معالَجين بالغليفلوزين
2022-04-01 | المجلد السادس العدد العاشر - المجلد السادس | مقالات بحثيةنهاد خراط حلو | أ. د. عبد الحكيم نتوف
الملخص
خلفيّة البحث وهدفه: يُعدّ داء السكّري النمط الثاني داءً استقلابياً يترافق بشكل شائع مع البدانة, وتُعتبر مثبّطات الناقل المشارك صوديوم-غلوكوز النمط2 من الزمر الدوائية الحديثة نسبياً التي أثبتت دوراً فعالاً في خفض الخضاب الغلوكوزي (HbA1C) عن طريق زيادة طرح الغلوكوز في البول, تشير الدراسات إلى ازدياد هذه الكمية المطروحة بازدياد مستويات الغلوكوز الدموية. يسبب هذا الإدرار التناضحي خسارة في الحريرات مما ينتج عنه فقدان للوزن. ومن هنا كان من المقتَرح أن يرتبط تأثير الغليفلوزين الخافض للخضاب الغلوكوزي بانخفاض الوزن.
مواد البحث وطرائقه: جرت دراسة تصالبية لمدّة24 أسبوعاً, مُعشَّاة, ثلاثيّة التعمية, وحيدة المركز على مرضى سوريّين سكّريين من النمط2 T2DM(37 مريضاً). أوتي خلالها المرضى الميتفورمين بجرعة 1000 ملغ مرتين يومياً مع الجرعة العظمى للغليفلوزين( الذراع الأولى: الايمباغليفلوزين 25 mgجرعة وحيدة يومياً (19 مريضاً), الذراع الثانية: الداباغليفلوزين 10 mg جرعة وحيدة يومياً (18 مريضاً) ) لمدة 12 أسبوعاً ثمّ جرت المصالبة أي المبادلة بين الدواءين وإيتائهما لمدة 12 أسبوعاً بعد فترة washout period لإزالة أي أثر للدواء من الجسم (7-10 أيام). قُيّمت المشعرات في لحظة البدء, الأسبوع 12 والأسبوع 24. في نهاية الدراسة دُرست علاقة الارتباط بين انخفاض الوزن وHBA1C لمستخدمي كل من الايمباغليفلوزين الداباغليفلوزين.
النتائج: أظهرت دراستنا عدم وجود علاقة ارتباط جوهرية بين انخفاض الوزن وHBA1C عند مستخدمي ايمباغليفلوزين (R=-0.208; p=0.216). في حين تبيّن وجود علاقة ارتباط جوهريّة طرديّة متوسّطة بين انخفاض الوزن وHBA1C عند مستخدمي داباغليفلوزين (R=;0.575; p=0.000 ).
الاستنتاج: أشارت دراستنا إلى وجود اختلاف في علاقة الارتباط المدروسة بين دواءي داباغليفلوزين وايمباغليفلوزين المستخدَمين عند ذات المرضى مما يلقي الضوء على وجود اختلافات فارماكوديناميكية بين هذين الدواءين على الرغم من انتمائهما لذات الزمرة العلاجية وامتلاكهما ذات الآلية الفارماكولوجية مما قد يفضي إلى اختلافات في الحصائل العلاجية وهذا ما يؤكد ضرورة إجراء أبحاث تستقصي هذه الاختلافات للوصول إلى خطّة علاجيّة أفضل عند المرضى.
كلمات مفتاحية : تصالبيّة, سكّري نمط2, مثبّطات نواقل صوديوم-غلوكوز, ايمباغليفلوزين, داباغليفلوزين, خضاب غلوكوزي.
المقدمة Introduction:
يصيب داء السكّري النمط الثاني Type 2 Diabetes Mellitus(T2DM) أكثر من 350 مليون شخص عالمياً كما يزداد انتشاراً, وعلى الرغم من توفّر مجموعة واسعة من الزمر العلاجية الخافضة للغلوكوز إلا أنها غير قادرة على ضبط الغلوكوز الدموي لمدّة طويلة ضبطاً كافياً عند غالبية المرضى حتى وإن اشتركت أكثر من زمرة دوائية معاً1. كما ترتبط معظم الأدوية الخافضة للغلوكوز الدموي بتأثيرات ضائرة تنعكس سلباً على المعالجة الدوائية كنوبات انخفاض الغلوكوز الدموي hypoglycemia واكتساب الوزن2. الأمر الذي يضعنا في حاجة مستمرّة لمزيد من الزمر العلاجية الجديدة التي قد تسهم في ضبط أفضل لهذا الداء (T2DM). تُعتبر مثبّطات الناقل المشارك صوديوم-غلوكوز النمط2 Sodium Glucose co-transporter Type 2 inhibitors (SGLT2is) زمرة علاجية جديدة نسبياً تخفض الغلوكوز الدموي بآلية عمل مستقلة عن الانسولين3,4 حيث تستهدف هذه المركّبات مستقبلات ( (SGLT2الموجودة في القطعة S1 الموجودة في الأنابيب القريبة في الكلى مثبّطةً عودة امتصاص الغلوكوز من الكلية, الأمر الذي يسبب زيادة إطراح الغلوكوز في البولUrine Glucose Excretion (UGE) 5,6 . كما تشير الدراسات إلى ازدياد هذه الكميّة المطروحة في البول مع ازدياد تراكيز الغلوكوز الدموية7,8. تمتلك هذه الزمرة الدوائية ميزة إضافية عن كونها تضبط الغلوكوز الدموي وهي أنّها تنقص الوزن بسبب خسارة الحريرات الناتجة عن زيادة طرح الغلوكوز في البول إضافة إلى الإدرار التناضحي5,6. كما تشير الدراسات إلى كون نقصان الوزن يحصل نتيجة لنقصان الكتلة الشحمية, الأنسجة الدهنية الحشوية والأنسجة الدهنية تحت الجلد9. حديثاً دخل صنفان من هذه الزمرة الصناعة الدوائية السورية وهما ايمباغليفلوزينEmpagliflozin بجرعتيه 10 و25 ملغ وداباغليفلوزين Dapagliflozin بجرعتيه 5 و10 ملغ. ونظراً لكلّ ما ورد ذكره سابقاً إضافةً إلى انعدام البيانات والدراسات في سوريا حول هذه الزمرة الدوائية كان من المقترح أن تُدرس علاقة الارتباط بين تأثير الغليفلوزينات الخافض للغلوكوز وانخفاض الوزن.
طرائق وأدوات البحث Methods and Materials
جمهرة البحثStudy population
شملت الدراسة مرضى سكريين من النمط2 (T2DM) تتراوح أعمارهم بين 18-75 عاماً ممن لديهم خضاب غلوكوزي HbA1C أكبر أو يساوي 7.5% قبل البدء بالدراسة. كما استُبعد مرضى السكري ذات الأنماط الأخرى أو المعالَجين بالانسولين, الحوامل والمرضعات, واستبعاد مرضى الاعتلال الكلوي الذين لديهم معدل الرشح الكبيبي eGFR أقل من 45 مل. دقيقة1-.1.73م2-, كما استبعدنا المرضى الذين يستخدمون الأدوية المنحّفة سواء نباتية أو كيميائية والذين يعانون من إنتانات بولية عند البدء بالدراسة. وبعد عرض الموافقات المستنيرة على المرضى قبل البدء بالدراسة حصلنا على موافقة كامل المرضى الذين انضمّوا إلى الدراسة.
تصميم الدراسة Study Design
أُجريت دراسة تصالبية crossover, معشّاة randomized, ثلاثيّة التعمية triple-blind, ثنائيّة الذراع, وحيدة المركز mono-center لمدة 24 أسبوعاً على المرضى الخارجيين الذين راجعوا العيادات الغدية للعيادات الطبية المجانية في عربين في الفترة الممتدة بين تشرين الأول 2019 وتشرين الأول 2020. تمّ سحب عيّنات دموية ( بعد صيام 8 ساعات). تمّ التعامل مع مرضى سكريين (T2DM) غير مضبوطي الغلوكوز الدموي((HbA1c>7.5, بداية خضع المشاركون لفترة washout period لإزالة أي أثر لخافضات السكّر الفمويّة الأخرى من الجسم والتي كان المرضى معالَجين بها قبل البدء بالدراسة (مدّة 10 أيام) مع وضعهم على الميتفورمين فقط بجرعة 1000 ملغ مرتين يومياً ثم انقسم المشاركون في الدراسة عشوائياً إلى مجموعتين, أُخذت القياسات المدروسة في اللحظة القاعدية (البدئية) Baseline, أُعطي مرضى الذراع الأولى دواء ايمباغليفلوزين (ايمبا) المرموز له بالرمز( (Aأثناء الدراسة ( تقدمة شركة سيتي فارما للصناعات الدوائية, رقم الطبخة4277 , تاريخ إنتاج 2019 م) جرعة وحيدة يومياً 25 ملغ بالمشاركة مع الميتفورمين بجرعة 1000 ملغ مرتين يومياً, وأُعطي مرضى الذراع الثانية دواء داباغليفلوزين (دابا) المرموز له بالرمز( (Bأثناء الدراسة (تقدمة شركة الفارس للصناعات الدوائية, رقم الطبخة 006, تاريخ إنتاج 2019 م) جرعة وحيدة 10 ملغ بالمشاركة مع الميتفورمين بجرعة 1000 ملغ مرتين يومياً لمدّة ثلاثة أشهر, في نهاية الثلاثة أشهر أُخذت القياسات المدروسة مّرة أخرى(نهاية الفترة الأولى) first period ومن ثمّ خضع المرضى لفترة غسيل مرة أخرى مدّتها 7-10أيام أي حوالي العشرة أعمار نصفية للدواء المدروس (بإيقاف الغليفلوزين والإبقاء على الميتفورمين فقط) ومن ثمّ بادلنا بين الذراعين بأن أعطينا مرضى الذراع الأولى (الميتفورمين مع الداباغليفلوزين) ومرضى الذراع الثانية (الميتفورمين مع الايمباغليفلوزين) بذات الجرعات العلاجية واستمرينا في الدراسة لثلاثة أشهر أخرى في نهايتها أعدنا أخذ القياسات المدروسة للمرة الأخيرة ( نهاية الفترة الثانية) second period. تمّ قياس HbA1c وفق معايرة التألّق المناعي Immunofluorescence Assay باستخدام جهاز I-chroma HbA1c analyzer (Boditech MED., INC., Korea). والتأكّد من مطاوعة المرضى والتزامهم ببروتوكول الدراسة عبر اتصالات هاتفية دورية مع المرضى إضافة إلى عدّ المضغوطات المتبقية في العبوات الدوائية. ومن الجدير بالذكر أنّ العبوات الدوائية كانت متماثلة جميعاً بالشكل وعدد المضغوطات مما يضمن تعمية الدواء المدروس عن المريض والطبيب والمحلّل الإحصائي.
الدراسة التحليلية والإحصائية للبيانات Statistical Analyses
اعتماداً على الحزمة الإحصائية للعلوم الاجتماعية (SPSS) النسخة 25 لتحليل البيانات SPSS version 25.0 (IBM Corp., Armonk, NY, USA) جرى توصيف البيانات المستمرة لمتغيرات الدراسة كـ متوسط حسابي ± الانحراف المعياري أما البيانات الفئوية فقد جرى توصيفها كنسبة مئوية. استخدم اختبار paired T-test لدراسة الفرق في الخصائص السريرية عند لحظة البدء بين مجموعتي الدراسة كما دُرست علاقة الارتباط بين انخفاض الوزن وHBA1C عن طريق ارتباط بيرسون Pearson correlation coefficient للمتغيرات التي تتبع التوزع الطبيعي، وارتباط سبيرمان Spearman correlation coefficient عند رفض فرضية التوزع الطبيعي (وذلك اعتماداً على اختبار Shapiro-Wilk المطبّق لدراسة فرضية التوزع الطبيعي) وذلك لدراسة قوة وجهة العلاقة بين متغيرين عند مجموعة مستخدمي ايمبا ((A (n=37, كامل المرضى بعد نهاية الدراسة أي مرضى الذراع الأولى خلال الفترة الأولى first period ومرضى الذراع الثانية خلال الفترة الثانية ( second period ومجموعة مستخدمي دابا ((B (n=37, مرضى الذراع الأولى خلال الفترة الثانية second period ومرضى الذراع الثانية خلال الفترة الأولىfirst period (. أُجريت الدراسة الإحصائية على المرضى الذين أكملوا بروتوكول الدراسة حتى النهاية فقط وفق مبدأ per-protocol principle اعتُمدت قيمة p-value=0.05 لتحديد الفروق الجوهرية عند مستوى ثقة قدره 95%.
النتائج Results:
عيّنة الدراسة Patients characteristics
بين الفترة الممتدة بين تشرين الأول من عام 2019م وتشرين الثاني من عام 2020م دُرست بيانات 85 مريضاً, 47 منهم حقّقوا معايير الاشتمال وقبلوا المشاركة في الدراسة, 37 مريضاً فقط مَن أكملوا الدراسة وهم الذين خضعوا للدراسة الإحصائية (مخطط 1). تضمّنت عيّنة بحثنا 24.3% من الذكور و75.7% من الإناث وقد كان العمر الوسطي± الانحراف المعياري 55±8 سنة, والوزن الوسطي± الانحراف المعياري 72.81±10.84 كغ, كما لم توجد أي فروق جوهريّة إحصائيّة في الخصائص السريرية عند لحظة البدء بين مجموعتي ايمبا Aودابا B (جدول 1). كما وردت الخصائص السريرية لمجموعتي الذراعين الأولى والثانية عند لحظة البدء baseline في الجدول (2).



3-2 المحصّلات الأوليّة Primary endpoint
دُرست علاقة الارتباط بين انخفاض الوزن وHBA1C في كل من مجموعة مستخدمي ايمبا ومجموعة مستخدمي دابا شملت الدراسة كامل المرضى الذين استخدموا كلاً من الدواءين أي 37 مريضاً في كل مجموعة وذلك باستخدام ارتباط سبيرمان البديل اللا معلمي نتيجة لعدم تحقق فرضية التوزع الطبيعي لمتغيرات الدراسة. أظهرت دراستنا عدم وجود علاقة ارتباط جوهرية بين انخفاض الوزن وHBA1C عند مستخدمي ايمبا حيث كانت (r=-0.208; p-value=0.216) عند مستوى ثقة .95% كما تبين وجود علاقة ارتباط جوهرية طردية متوسطة بين انخفاض الوزن وHBA1C عند مستخدمي دابا حيث كانت (r=0.575; p-value=0.000) عند مستوى ثقة 95% جدول (3), مخطط (2).

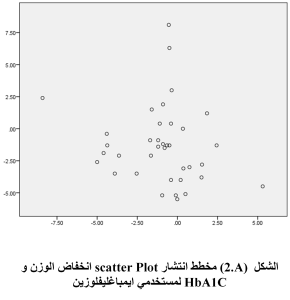

المناقشة Discussion:
تهدف معالجة داء السكريT2DM)) إلى تأخير مضاعفات المرض وتحقيق جودة حياة أمثل للمريض10, وتقترح الدلائل الإرشادية لمعالجة داء السكريT2DM) ) التركيز على خصائص المريض ذاته بدلاً من التركيز على المرض patient-centered strategy 10 وذلك بالأخذ بعين الاعتبار التأثيرات الضائرة الوارد حدوثها أثناء المعالجة كانخفاض غلوكوز الدم واكتساب الوزن واحتباس السوائل. ومع ارتفاع انتشار السكري عالمياً نظراً لازدياد معدلات البدانة11 كان لتأثير SGLT2is الخافض للوزن أهمية واضحة في معالجةT2DM 9,12–15. ومن المعروف أن SGLT2is تنقص مستويات الغلوكوز البلاسمية عبر زيادة طرح الغلوكوز في البول (تزداد هذه الكمية المطروحة بازدياد مستويات الغلوكوز البلاسمية) كما تنقص الوزن بشكل جوهري لدى المرضى16–18. وتشير الدراسات إلى كون الغليفلوزينات تنقص الوزن بإنقاص الكتلة الشحمية, الأنسجة الدهنية الحشوية والأنسجة الدهنية تحت الجلد9. ومن هنا كان من المقترح أن يرتبط تأثير الغليفلوزين الخافض للغلوكوز مع انخفاض الوزن. أوضحت دراستان رصديتان كوريتان عدم وجود علاقة ارتباط بين انخفاض الوزن وانخفاض الخضاب الغلوكوزي عند مستخدمي ايمبا19 ومستخدمي دابا20 واقترحوا تفسيراً لنتائج عدم الارتباط بين انخفاض الوزن وHBA1C عند المرضى بزيادة فرط الطعام كآلية تعويضية compensatory hyperphagia التي قد تُشاهد عند المرضى البدينين21 وما يدعم هذا الاقتراح كون خسارة الوزن المسبّبة بالغليفلوزين أقل من تلك المحسوبة من كمية الحريرات المفقودة جراء طرح الغلوكوز في البول22 كما تشير بعض الدراسات إلى كون الأفراد البدينين يمتصون الغلوكوز من العفج بصورة أكبر عبر مستقبلات SGLT1 التي يزداد التعبير عنها عند هؤلاء المرضى23 إلا أنّ ذلك قد يختلف حسب العِرق وهو مالم يُدرس في الأدب الطبي حتى الآن. وأوصتا بإجراء دراسة تجريبية استباقية prospective تستقصي بوضوح أكبر هذه العلاقة. أظهرت دراستنا وجود علاقة ارتباط طردية جوهرية متوسطة بين انخفاض الوزن وHBA1C عند المرضى الذين استخدموا دواء دابا, مع عدم وجود علاقة ارتباط جوهرية بين انخفاض الوزن وHBA1C عند المرضى الذين استخدموا دواء ايمباغليفلوزين أي اتفقت نتائج دراستنا مع نتائج دراسةCho 2019 وزملائه على الايمبا 19 إلا أنها تعارضت مع نتائج دراسة Lee 2016 وزملائه على الدابا 20. أشار kosugi 2019 وزملاؤه إلى أن الدابا لا يحرّضcompensatory hyperphagia 24 كما أشارت دراسة SEASAW 2020 إلى أنّ الايمبا لايغيّر من شهية المريض للطعام إلا أنه يسبّب انخفاضاً في النشاط الفيزيائي لدى المرضى المعالَجين به25. الأمر الذي يوصي بإجراء دراسة تدرس هذا الأثر عند المرضى المعالَجين بالدابا. ومن الجدير بالذكر أنّ دراسة lee وزملائه قد درست العلاقة بين المتغيرين في فترة كانت وسطياً 203 يوماً ومما قد يفسّر الاختلاف في نتائجنا اختلاف الأثر العلاجي للدابا بين الأمد القصير short-term والأمد الطويل long-term للمعالجة26. يمتاز هذا البحث بكونه الأول الذي درس هذه الزمرة الدوائية الجديدة على مرضى سوريين كما يمتاز بتصميمه الذي لغى أي اختلاف في الخصائص السريرية لأفراد البحث على اعتبار أن المرضى هم ذاتهم في كلتا المجموعتين AوB مما يجعل المقارنة بين خصائص الدواءين تظهر بصورة أدق وأوضح. إلا أنه يمتلك بعض المحدوديات كعدم تقييم الاختلافات في نمط الحياة عند المرضى (رياضة أو نظام غذائي) كما لم يتم قياس كمية الغلوكوز المطروحة في البول في حين أن هذه الكمية قد تختلف باختلاف الخصائص السريرية للمريض, مما يوصي بإجراء أبحاث أخرى تدرس تأثير هذه العوامل ( نمط الحياة, النشاط الفيزيائي وكمية الغلوكوز المطروحة في البول) على المتغيّرات المدروسة عند مستخدمي ايمبا ومستخدمي دابا واستقصاء أي فروق بين الدواءين.
الاستنتاج Conclusion:
أشارت دراستنا إلى وجود اختلاف في علاقة الارتباط المدروسة بين دواءي داباغليفلوزين وايمباغليفلوزين المستخدَمين عند ذات المرضى يُعتقد أن يعود ذلك إلى اختلاف أثر الدواء المدروس على النشاط الفيزيائي مما يوصي بإجراء أبحاث أخرى ذات عدد مرضى أكبر ومدة دراسة أطول تدرس تأثير العوامل (الوارد الغذائي, النشاط الفيزيائي وكمية الغلوكوز المطروحة في البول) على المتغيّرات المدروسة عند مستخدمي ايمبا ومستخدمي دابا واستقصاء أي فروق بين الدواءين.
المراجع :- Inzucchi, S. E. et al. Management of hyperglycemia in type 2 diabetes: A patient-centered approach. Diabetes Care 35, 1364–1379 (2012).
- Tahrani, A. A., Bailey, C. J., Del Prato, S. & Barnett, A. H. Management of type 2 diabetes: New and future developments in treatment. Lancet 378, 182–197 (2011).
- Tahrani, A. A., Barnett, A. H. & Bailey, C. J. SGLT inhibitors in management of diabetes. Lancet Diabetes Endocrinol. 1, 140–151 (2013).
- Hasan, F. M., Alsahli, M. & Gerich, J. E. SGLT2 inhibitors in the treatment of type 2 diabetes. Diabetes Res. Clin. Pract. 104, 297–322 (2014).
- Bailey, C. J. Renal glucose reabsorption inhibitors to treat diabetes. Trends Pharmacol. Sci. 32, 63–71 (2011).
- Abdul-Ghani, M. A., Norton, L. & DeFronzo, R. A. Role of sodium-glucose cotransporter 2 (SGLT 2) inhibitors in the treatment of type 2 diabetes. Endocr. Rev. 32, 515–531 (2011).
- Abdul-Ghani, M. A., DeFronzo, R. A. & Norton, L. Novel hypothesis to explain why SGLT2 inhibitors inhibit only 30-50% of filtered glucose load in humans. Diabetes 62, 3324–3328 (2013).
- Yagi, S. et al. Predictors for the Treatment Effect of Sodium Glucose Co-transporter 2 Inhibitors in Patients with Type 2 Diabetes Mellitus. Adv. Ther. 35, 124–134 (2018).
- Bolinder, J. et al. Effects of Dapagliflozin on Body Weight, Total Fat Mass, and Regional Adipose Tissue Distribution in Patients with Type 2 Diabetes Mellitus with Inadequate Glycemic Control on Metformin. J. Clin. Endocrinol. Metab. 97, 1020–1031 (2012).
- Davies, M. J. et al. Management of Hyperglycemia in Type 2 Diabetes, 2018. A Consensus Report by the American Diabetes Association (ADA) and the European Association for the Study of Diabetes (EASD). Diabetes Care 2012, 1–33 (2018).
- Di Cesare, M. et al. Trends in adult body-mass index in 200 countries from 1975 to 2014: A pooled analysis of 1698 population-based measurement studies with 19.2 million participants. Lancet 387, 1377–1396 (2016).
- Bailey, C. J. et al. Dapagliflozin add-on to metformin in type 2 diabetes inadequately controlled with metformin: A randomized, double-blind, placebo-controlled 102-week trial. BMC Med. 11, 1–10 (2013).
- Ferrannini, E., Seman, L., Hantel, S., Pinnetti, S. & Woerle, H. J. A Phase IIb, randomized, placebo-controlled study of the SGLT2 inhibitor empagliflozin in patients with type 2 diabetes. 721–728 (2013).
- Zaccardi, F. et al. Efficacy and safety of sodium-glucose co-transporter-2 inhibitors in type 2 diabetes mellitus: systematic review and network meta-analysis. Diabetes, Obes. Metab. 18, 783–794 (2016).
- Rosenstock, J. et al. Efficacy and safety of empagliflozin, a sodium glucose cotransporter 2 (SGLT2) inhibitor, as add-on to metformin in type 2 diabetes with mild hyperglycaemia. Diabetes, Obes. Metab. 15, 1154–1160 (2013).
- Chao, E. C. & Henry, R. R. SGLT2 inhibition-A novel strategy for diabetes treatment. Nat. Rev. Drug Discov. 9, 551–559 (2010).
- Kato, K. et al. The effects of intermittent use of the SGLT-2 inhibitor, dapagliflozin, in overweight patients with type 2 diabetes in Japan: a randomized, crossover, controlled clinical trial. Expert Opin. Pharmacother. 18, 743–751 (2017).
- Bonora, B. M., Avogaro, A. & Fadini, G. P. Extraglycemic effects of SGLT2 inhibitors: A review of the evidence. Diabetes, Metab. Syndr. Obes. Targets Ther. 13, 161–174 (2020).
- Cho, Y. K. et al. Clinical parameters affecting the therapeutic efficacy of empagliflozin in patients with type 2 diabetes. 2, 1–12 (2019).
- Lee, J. Y. et al. Clinical parameters affecting dapagliflozin response in patients with type 2 diabetes. Diabetes Metab. 43, 191–194 (2017).
- Moran, T. H. Hypothalamic nutrient sensing and energy balance. Front. Eat. Weight Regul. 63, 94–101 (2009).
- Scheen, A. J. & Paquot, N. Metabolic effects of SGLT-2 inhibitors beyond increased glucosuria: A review of the clinical evidence. Diabetes Metab. 40, S4–S11 (2014).
- Nguyen, N. Q. et al. Accelerated intestinal glucose absorption in morbidly obese humans: Relationship to glucose transporters, incretin hormones, and glycemia. J. Clin. Endocrinol. Metab. 100, 968–976 (2015).
- Kosugi, R. et al. Effects of sodium-glucose cotransporter 2 inhibitor (Dapagliflozin) on food intake and plasma fibroblast growth factor 21 levels in type 2 diabetes patients. Endocr. J. 66, 677–682 (2019).
- Sargeant, J. . Effects of empagliflozin, diet, or both on physical activity and sedentary behaviour in people with type 2 diabetes: analyses from the SEESAW trial – Virtual Meeting | EASD. https://www.easd.org/virtualmeeting/home.html#!resources/effects-of-empagliflozin-diet-or-both-on-physical-activity-and-sedentary-behaviour-in-people-with-type-2-diabetes-analyses-from-the-seesaw-trial-c816c59b-2b13-4fcc-9ae4-ae3ef830dd2d (2020).
- Chen, J. F. et al. Use and effectiveness of dapagliflozin in patients with type 2 diabetes mellitus: a multicenter retrospective study in Taiwan. PeerJ 8, 1–20 (2020).