علاقة التعدّد الشّكليّ +2044A>G في جين IL-13 بالأمراض الأرجية التنفسيّة لدى جمهرة من السوريين: دراسة حالة-شاهد
2025-08-23 | المجلد السابع العدد السادس - المجلد السابع | مقالات بحثيةعبدالله شعبان بلول | عصام نصر البارودي | غزل ديب | لمى علي يوسف
الملخص
خلفيّة البحث: تُعدّ الأمراض الأرجية من أكثر المشكلات الصحية شيوعاً عالمياً، إذ تُصيب نحو ثلث سكان العالم بحسب تقارير منظمة الصحة العالمية. ويكمن الاهتمام بدراستها في آثارها السلبية على جودة حياة المرضى وإنتاجية المجتمعات. ويُعدّ الربو من أبرز أسباب الوفاة القابلة للوقاية، إذ يُسجَّل قرابة 250 ألف حالة وفاة سنوياً. وقد بيّنت الدراسات أنّ العوامل البيئية والوراثية تُعدّ من أهم عوامل الخطورة. تلعب السيتوكينات، ومنها الإنترلوكين-13(IL-13)، دوراً محورياً في توجيه الاستجابة المناعية نحو النمط Th2، وتحفيز إنتاج الأضداد IgE المرتبطة بالتأتبيّة. في هذا السياق، تمثل التعددات الشكلية مفردة النكليوتيد (SNPs) عناصر وراثية مهمة قد تؤثر في بنية البروتينات ووظائفها، أو في مستوى التعبير عنها، ما يجعلها أهدافاً مناسبة لدراسة علاقتها بالاستعداد للإصابة بالأمراض الأرجية.
هدف البحث: تحرّي العلاقة المحتملة بين التعدد الشكلي +2044A>G في جين IL-13 والاستعداد للإصابة بالأمراض الأرجية التنفسيّة لدى جمهرة من السوريّين.
المواد والطرائق: أجريت دراسة من نمط حالات-شواهد، اعتمدت فيها طرائق التشخيص السريري واختبار وخز الجلد(SPT) لتأكيد الأرجيّة لدى المرضى في ذراع الحالات ونفيها لدى الشّواهد. بُزلت عينات دم وريدي من المشاركين، وعُزل الحمض النووي الجينومي. ضُخّم التسلسل الجيني الحاوي على التعدد الشكلي +2044A>G باستخدام تفاعل البوليميراز التسلسلي(PCR) ، تلاه هضم ناتج التضخيم بوساطة أنزيم التقييدNlaIV، الذي يتعرف موقع التغير النكليوتيدي المدروس. قُرئت التسلسلات وحسبت تواترات الألائل والأنماط الجينيّة وأجريت المقارنات والتّحليلات الإحصائيّة باستعمال لغة R.
النتائج: شملت الدراسة 99 مشاركاً، منهم 64 مريضاً مشخصين سريرياً بأمراض أرجية تنفسية ونتائج إيجابية لاختبار وخز الجلد، و35 فرداً من غير المصابين كشواهِد. أظهرت النتائج وجود فوارق ذات دلالة إحصائية في توزّع الأنماط الجينية والألائل بين المجموعتين. كان تواتر الأليل G أعلى لدى المرضى مقارنةً بالشواهد، مما يشير إلى كونه عاملاً يزيد من خطر الإصابة. أظهر الأفراد الحاملون لنسخة واحدة على الأقل من الأليل G (الأنماط الجينية AG و(GG زيادة في احتماليّة الإصابة بنحو 18 ضعفاً مقارنةً بمن يحملون النّمط، (OR = 17.81) AA ، كما تبين أن الحاملين للنمط GG تحديداً أكثر عرضة للإصابة مقارنة بغير الحاملين لهذا النمط، إذ بلغت الأرجحية نحو 4.45 ضعفاً (OR = 4.45)، وكانت جميع الفروق المشار إليها ذات دلالة إحصائية (p< 0.001) .
كلمات مفتاحية : دراسة حالات-شواهد، أمراض أرجية تنفسيّة، ربو أرجي، التهاب أنف الأرجي، +2044A>G، إنترلوكين-13 ,Case-control study, respiratory allergic diseases, allergic asthma, allergic rhinitis, +2044A>G, interleukin-13
المقدمة Introduction
تعرّف الأمراض الأرجيّة على أنها جملة الحالات الناجمة عن ردّ فعل مناعيّ التهابيّ شديد استجابة للتعرض لمستضدات غير ممرضة في الحالة الطبيعية تدعى بالمستأرجات Allergens، وتشمل هذه الأمراض كلّاً من الربو الأرجي Allergic Asthma، التهاب الأنف الأرجي Allergic Rhinitis، الأرجية تجاه الطعام Food Allergy، التهاب الجلد التأتبي Atopic Dermatitis، الوذمة الوعائية Angioedema، الشرى Urticaria، الأرجية للحشرات والأدوية Insect and Drug Allergy، و التأق Anaphylaxis، (رد فعل مناعي جهازي حادّ استجابةً للتعرض لأحد المستأرجات كالأطعمة والأدوية والسموم، وقد يكون مميتاً) 1.
تشكّلُ الأمراض الأرجية واحدة من أكثر المشكلات الصحية المزمنة انتشاراً حول العالم و يبلغ معدل انتشارها نحو قرابة 30% من مجمل السكان2، وقد لوحظ الارتفاع الكبير في انتشار الأرجية في الدول الغربية والدول التي يسيطر عليها نمط الحياة الحضرية وكذلك الأمر في الدول ذات الدخل المنخفض والمتوسط، مما يجعلها من التحديّات الطبية الرئيسة في القرن الواحد والعشرين نظراً لتأثيرها السلبي على جودة ونوعية حياة الأفراد بالإضافة إلى التأثير على إنتاجيتهم مما يحمّل المجتمعات أعباءً وخسائر اقتصادية ضخمة 3,4، ويبرز الربو كأحد أكثر هذه الأمراض تأثيراً على الصجة العامة وإنتاجية الأفراد ذلك وبالإضافة إلى انتشاره الواسع (400 مليون شخص حول العالم) فإنه يسبب 250 ألف حالة وفاة سنوياً بحسب تقديرات منظمة الصحة العالمية2. وقد بينت النتائج من دراسة الشبكة العالمية للربو Global Asthma Network (GAN) والتي شملت مركزين رئيسيين في سوريا (3315 مشارك من محافظتي دمشق واللاذقية)، أن نسبة الأفراد الذين أبلغوا عن وجود الوزيز Wheezing خلال الأشهر الاثني عشر السابقة للدراسة بلغت 19.8%، في حين أبلغ 12.8% من المشاركين عن ظهور أعراض ربو حادة Severe Asthma Symptom 5.
تندرجُ الأمراضُ الأرجيّةُ تحتَ النمطِ الأوّلِ منْ تفاعلاتِ فرطِ الحساسيّةِ Type I hypersensitivity، و يتطوّرُ هذا النمطُ كغيرهِ منْ أنماطِ فرطِ الحساسيّةِ على مرحلتينِ، تُعرَفُ الأولى بمرحلةِ التحسيسِ Sensitization، حيثُ يتعرّضُ الفردُ لمُستأرجٍ ما ومنْ ثمّ تقومُ الخلايا المقدّمةُ للمستضدِّ Antigen presenting cells (APCs) بالتقامِهِ وتقديمهِ للمفاويّات التّائيّةِ T-cells فتحرّض تمايزُ التّائيّاتُ المفعّلةُ إلى خلايا تائيةٍ مساعدةٍ T-helper cells من النمطِ الثّاني Th2، وينتجُ عنْ هذا التفّعيلِ إفرازُ العديدِ منَ الإنترلوكينات Interleukins مثل IL-4، IL-13، IL-5، IL-9، IL-10. تؤدّي هذهِ الوسائطُ إلى تغيير النمطِ الإسويّ للأضّدادِ المفرزةِ من قبلِ اللمفاويّاتِ البائيّة B-cells إلى أضدادٍ من نمطِ الغلوبيوبين المناعي E (IgE)، حيث تعبر الخلايا البدينة Mast cells والأسسات Basophils على سطوحها عن مستقبلاتٍ عاليةِ الألفةِ للضّد IgE تُعرف بـ FcεRI. يشمل طور التحسيس Sensitization Stage ارتباط أضداد IgE بمستقبلاتها عالية الألفة دون أن ينجم عن ذلك تحرّرٌ لأيٍّ منَ الوسائطِ الالتهابيةِ، في حينْ يطلقُ على المرحلة الثّانية مرحلة الاستفعال Effector Stage، والّتي تُقسَمُ إلى طورَين اثنين؛ يُعرَفُ أوّلهُما بطورِ الاستجابةِ الفوريّةِ، حيثُ تؤدي معاودةُ التعرضِّ للمستأرجِ إلى ارتباطهِ بصورة نوعية إلى الأضداد IgE المرتبطةُ بالمستقبلاتِ عاليةِ الإلفةِ على سطوحِ الخلايا المحسّسةِ Sensitized Cells (الخلايا البدينة والأَسُسات) وحدوث تفعيلٍ تصالبيٍّ cross-linking activation لهذهِ المستقبلاتِ، ومنْ ثَمَّ تَفعيلُ العديدِ منْ سبلِ نقلِ الشّارةِ الخلويّة والتي تنتهي بإفراغٍ سريعٍ لمكوناتِ الحبيباتِ degranulation الموجودةِ ضمنَ هذه الخلايا والتي تشمَلُ العديدَ منَ الوسائطِ الالتهابيّةِ المصنّعةِ مُسبقاً مثلَ الهيستامينْ histamine، والبروستاغلانديناتْ prostaglandins، والليكوترينات leukotrienes 6.
يبرز الإنترلوكين-13 بالتضافر مع الإنترلوكين-4 عاملاً محورياً في تطور الاستجابات المناعية من النمط الثاني. الإنترلوكين-13 بروتين سكري بوزن جزيئي يقارب 12 كيلو دالتون، يتشابه وظيفياً مع الإنترلوكين-4 وتتوضع الجينات المرمزة لكليهما بشكل متجاور في الذراع الطويل للصبغي الخامس في الموقع الصبيغي 5q23.31 وذلك ضمن تعنقد من الجينات المرمزة لعوامل مرتبطة بالاستجابة المناعية من النمط الثاني Th2، ومنها كل من IL-4 وIL-3 وIL-5 وIL-9 وجين العامل المحفّز لنمو المحبّبات والبالعات granulocytes macrophages colony stimulating factor (GM-CSF)7.
يؤدّي IL-13 أدوارهُ في تطوّرِ الاستجابةِ الأرجيّةِ والمتمثّلَةِ في تحفيزِ تكاثرِ الخلايا البائيّةِ وتحريضِ انقلابِ النمط الإسويّ للأضداد إلى IgE (IgE isotype class switching)، وتفعيل الحمضاتِ والأسساتِ والخلايا البدينةِ، بالإضافةِ إلى تحفيزِ إنتاجِ الكولّاجين من الأرّوماتِ الليفيّةِ، والتّعبيرِ عن جزيءِ التصاقِ الخلايا الوعائيّةِ vascular cell adhesion molecule (VCAM-1) على سطوحِ الخلايا البِطانيّةِ، فضلاً عن مساهمتهِ في تقلّصِ العضلاتِ المُلس؛ الأمرُ الّذي يؤدّي إلى إعادةِ قولبةِ remodeling الطرق التنفسية 8.
تؤدي العوامل البيئية دوراً هاماً في تطور الأمراض الأرجية، إلا أن التركيبة الجينية للأفراد تشكّل عاملاً حاسماً في الأهبة لتطوير ردود الفعل التأتبية والأمراض الأرجية لاحقاً، ومن المعلوم ارتباط التغايرات الجينية ومن ضمنها التعددات الشكلية مفردة النكليوتيد Single Nucleotide Polymorphisms (SNPs) والتي تعرف على أنها استبدال لنكليوتيد واحد ضمن تسلسل الحمض النووي ويكون انتشارها في الجمهرة أعلى من 1% بالأهبة أو الاستعداد للإصابة أو حتى تطور الاستجابات المرضية وشدتها، وضمن هذا السياق؛ يشير التعددّ الشّكليّ مفردُ النكليوتيدِ +2044A>G إلى تغيّرٌ لا مترادف في تسلسلِ الدنا ينتج عنه استبدالُ الحمضِ الأمينيّ الغلوتامين في الموقعِ 130 من البنيةِ الأوليّةِ للبروتينِ المنتجِ بالحمضِ الأمينيّ الأرجنين، وقد بيّنت دراساتُ النّمذجةِ الحاسوبيةِ أهميّةُ هذا الموقعِ في حدوثِ التآثراتِ بينَ IL-13 ومستقبلاته، كما أشارت دراساتُ الكيمياءِ المناعيّة النسيجيّة إلى أن التعبير عن مستقبل الإنترلوكين-13 يزداد في الخلايا الظهارية وخلايا العضلات الملس عند مرضى الرّبو، ومن المقترَح أنّ وجود المتغاير Arg110 يزيد من إلفة ارتباط IL-13 مع هذه المستقبلات الأمر الذي يزيد من تأثيراته المختلفة على هذه الأهداف الخلوية والنسيجية 9. تهدف هذه الدراسة إلى تحريّ الارتباط المحتمل بين التعدد الشكلي +2044A>G والأهبة للإصابة بالأمراض الأرجية التنفسية عند جمهرة السوريين.
المواد والطرائق Materials and methods
قمنا بتصميم الدراسة لتكون دراسة رصدية من نمط حالة-شاهد Observational Case-Control study، حيث شملت الدراسة 64 مريضاً مشخصاً بالتهاب الأنف التحسسي أو الربو الأرجي المؤكد بواسطة اختبار الوخز بالجلد Skin Prick Test (SPT)، من كلا الجنسين وممن تزيد أعمارهم عن خمس سنوات، في حين شملت ذراع الشاهد Control 35 فرداً سليماً ظاهرياً ونفيت إصابتهم بأحد الأمراض الأرجية التنفسية اعتماداً على سلبية اختبار الوخز بالجلد SPT للمستأرجات التنفسية، استبُعِدَ من الدراسة المشاركين غير القادرين على فهم إجراءات الدراسة لأسباب معرفية أو إدراكية، والنساء الحوامل والمرضعات، والمرضى المصابين بأمراض جهازية شديدة وكذلك الذين تلقوا علاجاً بالكورتيكوستيروئيد الجهازي أو مضادات الهستامين خلال 30 يوماً قبل إجراء اختبار الوخز بالجلد SPT.
حصلت الدراسة على موافقة لجنة أخلاقيات البحث العلمي في كلية الصيدلة في جامعة دمشق برقم (5675) تاريخ (24/10/2023)، إضافة إلى الحصول على موافقة أفراد الدراسة المستنيرة قبل انخراطهم فيها،وذلك بعد تقديم الشروحات الوافية عن هدف الدراسة والفوائد المرجوة منها والمخاطر المحتملة.
أجري اختبار الوخز بالجلد تحت إشراف طبي، واستخدمت عتيدة من شركة Immunotek الإسبانية، حيث تمّ وضع قطرات من محاليل المستأرجات المختلفة المُضمّنة في العتيدة (اثنان وعشرون محلولاً أبرزها العث المنزلي البحري والطحيني ووبر الكلاب والقطط، ومن ثم وخز أماكن القطرات بواخزات عقيمة مخصصّة لهذا الاختبار، ومراقبة ظهور أعراض رد الفعل المناعي لمدة بين 15-20 دقيقة والذي يتجلّى بظهور حطاطة واحمرار في مكان الوخز، واعتمدت إيجابية الإختبار بحطاطة قطرها أعلى أو مساويٍ لثلاثة ملليميترات، وضلك بالمقارنة مع شاهدين أحدهما إيجابي (الهيستامين) والآخر سلبي وهو المحل الحامل للمستأرجات.
جُمعت العينات من عيادات الأرجية في دمشق وعيادة الدكتورة غزل ديب في اللاذقية، حيث بُزِلَ 3 مل من الدم الوريدي على أنابيب تحوي مانع التخثر إيتيلين ثنائي الأمين رباعي حمض الخل Ethylenediaminetetraacetic acid EDTA، تلاه استخلاص الدنا الجينومي خلال مدة أقصاها يومين من تاريخ السحب باستخدام عتيدة استخلاص من شركة VIVANTIS الماليزية، وتم التأكد من نقاوة الاستخلاص وقياس تراكيز الدنا الجينومي المستخلص باستخدام جهاز Nanodrop، حيث بلغ متوسط التراكيز 49.16 نانوغرام/مكل، في حين كان متوسط النقاوة 1.6.
التنميط الجيني
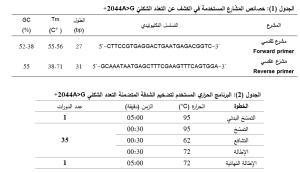
أجري تفاعل البوليمراز التسلسلي Polymerase Chain Reaction (PCR) باستخدام زوج المشارع المقتبس من الأدبيات 10، والذي تم تصميمه لتضخيم شدفة بطول 236 زوج أساس وخلق موقع تقييد للأنزيم NlaIV عند التسلسل الحاوي على التعدد الشكلي +2044A>G، ويوضح الجدول (1) تسلسل المشارع المستخدمة وخصائصها.
أُخِذَ 3 مكرولتر من منتج الـ PCR وأضيف له 1 مكرولتر من كل مَشرَع بتركيز 10 بيكومول/مكرولتر و 5 مكرولتر من مزيج لتفاعل PCR (5x Master Mix) من شركة Everogen® الروسيّة، واتبع البرنامج الحراري الموضح في الجدول (2). وتم التأكد من نجاح التضخيم بترحيل المنتجات على هلامة من الأغاروز بتركيز 2%.
نُّمِطَت العينات باتباع طريقة التعدد الشكلي لأطوال شدف التقييد Restriction Fragment Length Polymorphism (RFLP) حيث قُطِعَت منتجات الـ PCR باستخدام أنزيم NlaIV (وحدة دولية/مكروغرام)، تم ترحيل منتجات تفاعل الهضم الأنزيمي على هلامة من الأغاروز بتركيز4%، وظُهِّرَت العصابات الناتجة باستخدام جهاز إظهار وتوثيق الهلام باستخدام الأشعة فوق البنفسجية من شركة Cleaver Scientific البريطانية.
أجري التحليل الإحصائي باستخدام لغة البرمجة R وبرنامج GraphPad Prism (version 8.0.1)، قُورِنَ توزّع الأنماط الجينيّة والألائل بين مجموعتيّ الدّراسة باستخدام اختبار Chi-square لمعرفة فيما إذا كانت الفروقات الملاحظة يُعتد بها إحصائياً (P-value< 0.05)، أو أن هذه الفروقات ناتجة عن المصادفة (P-value> 0.05).
النتائج Results
نتائج تفاعل البوليميراز التسلسلي PCR والقطع الأنزيمي:
ينتج عن تفاعل PCR شدفة من DNA بطول تقريبي 236 زوج أساس تتضمن التعدد الشكلي المدروس كما يبيّن الشكل (1).
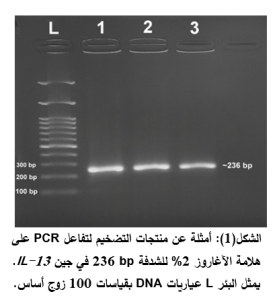
كانت نواتج RFLP متطابقة مع النتائج المتوقعة للأنماط الجينية المختلفة، حيث يتعرف أنزيم التقييد NlaIV على تسلسل الدنا GGNNCC والذي يتكرر مرتين ضمن الشدفة المضخمة؛ الأولى بعد 16 نكليوتيداً من النهاية 5’ والثانية قبل 32 نكليوتيداً من النهاية 3’ في الموقع الحاوي على التعدد الشكليّ المدروس، يعمل الموقع قرب النهاية 5’ شاهداً داخلياً لقدرة الأنزيم على القطع بصورة مستقلة عن وجود التعدد الشكلي أو غيابه، في حين يكون القطع في الموقع قرب النهاية 3’ مؤشراً لامتلاك الفرد للأليل G من التعدد السكلي المدروس، وبالنظر إلى الشكل (2) الذي يمثل ترحيل منتجات الـ PCR بعد تطبيق بروتوكول القطع نلاحظ ظهور شدفة بطول 210 زوج أساس في حال كان النمط الجيني للفرد متماثل الزيجوت للأليل A (AA)، وشدفة بطول 178 زوج أساس في حال كان النمط الجيني هو النمط المتغاير(GG)، وفي حال كان النمط الجيني متغاير الزيجوت (AG) يُلاحظ ظهور كلتا الشدفتين.

تواترات الألائل والانماط الجينية في مجموعتي الحالات والشواهد:
بيّنت مقارنة توزع الأنماط الجينية بين مجموعتي الدراسة أن تواتر النمط الجيني AA كان أعلى لدى جمهرة الشواهد بالمقارنة مع جمهرة الحالات بنسبة 54.3% مقابل 6.2%، على الترتيب. في حين كان النمط الجيني GG الأعلى تواتراً لدى الحالات (64.1%) مقابل (28.6%) عند الشواهد، أما النمط الجيني متغاير الزيجوت AG فقد كانت نسبة تواتره لدى الحالات 29.7% مقابل 17.1% لدى الشواهد، وبتطبيق اختبار كاي مربع، كانت قيمة P معتّداً بها إحصائياً بقوّة (p<0.0001). ويوضح الشكل )3 (مقارنة لتوزع الأنماط الجينية بين جمهرة الحالات وجمهرة الشواهد.
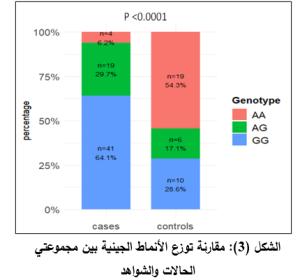
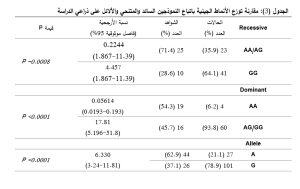
كما تمت مقارنة توزع الألائل باتباع اختبار كاي مربع حيث بلغ تواتر الأليل G نسبة قدرها 78.9% لدى مرضى الأرجية التنفسية مقابل نسبة لم تتجاوز 37.1% لدى غير المصابين (الشواهد)، ولدى حساب نسبة الأرجحية Odds Ratio (OR)، بيّنت النتائج بأن الأفراد الذين يحملون الأليل G لديهم معدل أرجحية أعلى للإصابة بـنحو ستة أضعاف من أولئك الحاملين للأليل A (OR=6.3, 95% CI (3.24-11.81))، وبمقارنة توزع الأنماط الجينية باتباع النموذج السائد تبين أن امتلاك الأفراد نسخة واحدة على الأقل من الأليل G (النمطين الجينين AG وGG) يزيد من معدل أرجحية الإصابة بنحو سبعة عشر ضِعفاً عن أولئك الذين يحملون نسختين من الأليل A (OR=17.81, 95% CI (5.196 -51.8))، أما امتلاك الأفراد لنسختين من الأليل G (النمط GG) يزيد معدل أرجحية الإصابة بنحو أربعة أضعاف بالمقارنة مع عدم وجود الأليل (النمط الجيني AA) أو امتلاك نسخة واحدة منه (النمط الجيني AG) (OR=4.457, 95% CI (1.867-11.39))، وقد كانت جميع الاختبارات المتبعّة للمقارنة معتّد بها إحصائياً (P<0.001) ويوضح الجدول (3) مقارنة تواتر الأنماط الجينية باتباع النموذجين السائد والمتنحي ومقارنة توزع الألائل بين مجموعتي الدراسة.
المناقشة Discussion
بينّت دراستنا وجود ارتباط ذي دلالة إحصائية قويّة بين النمط الجيني للتعدد الشكليّ +2044A>G والإصابة بالأمراض الأرجية التنفسية، حيث تبين أن امتلاك الأفراد للأليل G (أليل الخطورة) يزيد من أرجحية الإصابة وفق النموذجين السائد والمتنحي في حين يملك الأليل A دوراً وقائياً من الإصابة، وقد اتفقنا في ذلك مع أنوار وزملائها11 في العراق الذين وجدوا ارتباط بين النمط الجيني GG والإصابة بالربو إلا أن هذا الارتباط لم يكن معتدّاً به إحصائياً في دراستهم، واختلفنا مع كل من Beghé وزملائه في إيطاليا وBaye وزملائه في أمريكا وXi وزملائه في الصين 12–14
يمكن أن تعزى هذه الفروقات إلى اختلاف الإثنيات المدروسة، واختلاف العوامل البيئية للدراسات المختلفة والتي تؤدّي دوراً كبيراً في الأهبة للإصابة بالربو بالتضافر مع العوامل الجينيّة، و الطبيعة التغايرية للمرض Heterogenous والتعقيد المرتبط بتعدد العوامل المؤهبة من عوامل بيئية وعوامل جينية، بالإضافة إلى اختلاف تقنيات الكشف عن التعدد الشكلي بين الدراسات والتي تكون دقتّها عاملاَ مهماً في تجنب الانحياز.
الاستنتاجات Conclusions
تعد دراستنا الأولى في سورية في تحرّي فرضية وجود علاقة بين التعدّد الشكليّ +2044A>G والأمراض الأرجية التنفسيّة (الربو الأرجي والتهاب الأنف الأرجي)، وأظهرت الدراسة ارتباط الأليل G للتعدّد الشكليّ +2044A>G بزيادة كبيرة في أرجحية الإصابة بالأمراض الأرجية التنفسيّة عند جمهرة السوريين.
قائمة الاختصارات List of abbreviations
| Arginine | Arg |
| Antigen Presenting Cells | APCs |
| Global Asthma Network | GAN |
| Granulocytes Macrophages Colony Stimulating Factor | GM-CSF |
| Genome Wide Association Studies | GWAS |
| Immunoglobulin E | IgE |
| Interlukin-13 | IL-13 |
| Odds Ratio | OR |
| Polymerase chain reaction | PCR |
| Restriction fragment length polymorphism | RFLP |
| Single Nucleotide Polymorphisms | SNPs |
| Skin Prick Test | SPT |
| Vascular Cell Adhesion Molecule-1 | VCAM-1 |
الموافقة الأخلاقية والموافقة على المشاركة Ethics approval and consent to participate
حصلت هذه الدراسة على موافقة لجنة أخلاقيات البحث العلميّ في جامعة دمشق بتاريخ 24/10/2023، وبرقم 5675.
تضارب المصالح Conflict of interests
يقر المؤلفون بعدم وجود مصالح متضاربة.
التمويل Funding
تم تمويل هذا البحث من قِبَل جامعة دمشق.
مساهمات المؤلفين contributions’Authors
عبدالله بلول: الباحث الأساسي، القيام بالجزء العملي من البحث والكتابة النظرية للأطروحة والمقالة.
عصام البارودي: باحث مشارك، القيام بالجزء المتعلق بجمع العينات واستخلاص الدنا الجينومي.
غزل ديب: باحث مشارك، تسهيل جمع العينات والمعلومات الديموغرافية للمشاركين في الدراسة.
لمى يوسف: المشرف الأساسي في البحث، الإشراف على جميع تفاصيل البحث من تصميم خطة البحث والتوجيهات في الجانب العملي وتدقيق الكتابة النظرية.
المراجع :
- Graham JA, Gardner DE, Gardner SCM, Miller FJ. Toxicity of Airborne Metals. Comprehensive Toxicology, Second Edition. 2010;8:405-420. doi:10.1016/B978-0-08-046884-6.00922-2
- Pawankar R. Allergic diseases and asthma: a global public health concern and a call to action. World Allergy Organ J. 2014;7(1):12. doi:10.1186/1939-4551-7-12
- Accordini S, Corsico AG, Braggion M, et al. The Cost of Persistent Asthma in Europe: An International Population-Based Study in Adults. Int Arch Allergy Immunol. 2013;160(1):93-101. doi:10.1159/000338998,
- Pearson WS, Goates SA, Harrykissoon SD, Miller SA. State-based medicaid costs for pediatric asthma emergency department visits. Prev Chronic Dis. 2014;11. doi:10.5888/PCD11.140139,
- Mohammad Y, Rafea S, Latifeh Y, et al. Global Asthma Network Phase I Syria asthma surveillance and the impact of the war. J Thorac Dis. 2023;15(5):2873-2881. doi:10.21037/JTD-23-251/COIF)
- Chaplin DD. 1. Overview of the human immune response. Journal of Allergy and Clinical Immunology. 2006;117(2 SUPPL. 2):S430-S435. doi:10.1016/j.jaci.2005.09.034
- Zhang JH, Zhang M, Wang YN, Zhang XY. Correlation between IL-4 and IL-13 gene polymorphisms and asthma in Uygur children in Xinjiang. Exp Ther Med. 2018;17(2):1374. doi:10.3892/ETM.2018.7096
- Iwaszko M, Biały S, Bogunia-Kubik K. Significance of Interleukin (IL)-4 and IL-13 in Inflammatory Arthritis. Cells 2021, Vol 10, Page 3000. 2021;10(11):3000. doi:10.3390/CELLS10113000
- Heinzmann A, Mao XQ, Akaiwa M, et al. Genetic variants of IL-13 signalling and human asthma and atopy. Hum Mol Genet. 2000;9(4):549-559. doi:10.1093/HMG/9.4.549
- Graves PE, Kabesch M, Halonen M, et al. A cluster of seven tightly linked polymorphisms in the IL-13 gene is associated with total serum IgE levels in three populations of white children. Journal of Allergy and Clinical Immunology. 2000;105(3):506-513. doi:10.1067/MAI.2000.104940,
- Abdulla AA, Mahmood NS. Correlation Between IL-13rs20541(A> G) Gene Polymorphism and Bronchial Asthma Among Iraqi Patients. Rep Biochem Mol Biol. 2022;11(2):344-349. doi:10.52547/RBMB.11.2.344,
- Xi D, Pan S, Cui T, Wu J. Association between IL-13 gene polymorphism and asthma in Han nationality in Hubei Chinese population. Journal of Huazhong University of Science and Technology – Medical Science. 2004;24(3):219-222. doi:10.1007/BF02831994,
- Baye TM, Kovacic MB, Myers JM, et al. Differences in candidate gene association between European ancestry and African American asthmatic children. PLoS One. 2011;6(2). doi:10.1371/JOURNAL.PONE.0016522,
- Beghé B, Hall IP, Parker SG, et al. Polymorphisms in IL13 pathway genes in asthma and chronic obstructive pulmonary disease. Allergy: European Journal of Allergy and Clinical Immunology. 2010;65(4):474-481. doi:10.1111/J.1398-9995.2009.02167.X,