تحضير جسيمات نانوية لبولي كابرولاكتون محملة بحمض الديكلوفيناك بطريقة الترسيب النانوي
2025-08-23 | المجلد السابع العدد السادس - المجلد السابع | مقالات بحثيةسلافة عزيز السليمان | زكي علي عجي | أنطون موسى اللحام
الملخص
تم تحضير جسيمات نانوية لبلمر بولي كابرولاكتون ذي الوزن الجزيئي المتوسط العددي 45,000 محملة بحمض الديكلوفيناك بطريقة الترسيب النانوي، وحققت تحرراً مديداً، حيث تحرر ما يقارب 60% من الدواء خلال فترة 66 ساعة بآلية الانتشار وفق نموذج كورسماير بيباس الذي كان الأكثر تناسباً والأعلى قيمة لمعامل الارتباط بين نماذج التحرر الخمسة المدروسة، تميزت الجسيمات بشكلها الكروي، وحققت تجانس أبعاد بدرجة عالية حيث بلغت قيمة معامل التبعثر المتعدد 0.035±0.072 أي أقل من 0.5، ونصف قطر هيدروديناميكي أقل من 90 نانومتر، يعتقد أن هذه الجسيمات ستتمتع بثباتية عالية في العضوية الحية حيث تحمل كموناً كهرحركياً عالياً بقيمة 1.82±-31.73، وتم كبسلة ما يزيد عن 75% من كمية الدواء المدخلة في التحضير، تشير هذه الخصائص إلى ملاءمة النظام النانوي لتحرير و توصيل الدواء مع إمكانية استخدام الجسيمات النانوية البلمرية كنظام واعد لتحرير الأدوية بشكل متحكم فيه، كما حضرت جسيمات نانوية لبولي كابرولاكنون10,000 بنفس الطريقة وذلك بغية مقارنة تأثير الوزن الجزيئي للبلمر على الخصائص الفيزكيماوية للجسيمات المحضرة، فتفوقت الجسيمات المحضرة بالوزن الجزيئي الأصغر بصغر حجمها مقارنة بالوزن الجزيئي الأكبر للبلمر، حيث بلغ متوسط القطر الهيدروديناميكي 0.57±62.9، و لم يكن هناك فارق احصائي ذي دلالة في قيمة معامل التبعثر المتعدد بين الصيغتين، إلا أن كمونها الكهرحركي كان أدنى بشكل واضح حيث لم تتجاوز قيمته 17±4.2-.
كلمات مفتاحية : جسيمات نانوية، بولي كابرولاكتون، حمض ديكلوفيناك، تحرر مديد، طريقة الترسيب النانوي، نموذج حركيات تحرر الدواء ,Nanoparticles, Polycaprolactone, diclofenac acid, prolonged release, nanoprecipitation method, kinetics models of drug release
لقد أحدثت تقنية النانو ثورة في عالم صناعة الأدوية لما تقدمه من ميزات جعلت العلاج الدوائي أكثر فعالية وقدرة على استهداف المرض وبطريقة أكثر مضبوطية وأقل إحداثاً للآثار الجانبية [1]، حيث تتمتع الجسيمات النانوية بالقدرة على الإستهداف الدوائي إما بالحجم أو الشحنة أو الشكل أو حتى بالقدرة على ربط السطح بجزيء رابط lignad محدد [2-12]، وتتمتع الجسيمات الدوائية النانوية بذوبانية أفضل من مقابلاتها ذات الحجم الكتلي ((bulk الكبير وفترة دوران دموي blood circulation أطول ضمن الجسم الحي مما يحسن من حركيتها الدوائية ضمن العضوية الحية [14].
الديكلوفيناك هو مضاد التهاب لا ستيروئيدي يستخدم كمسكن ألم في حالات التهاب المفاصل وغيرها من الاضطرابات الالتهابية، عن طريق تثبيط إنزيمات السيكلوكسيجيناز (COX1 & COX2) ولكنه يثبط بدرجة أكبر COX2 [14]، مما يقلل من تصنيع البروستاغلاندين الذي يتوسط حدوث الوذمة والألم والحمى والالتهابات، بالإضافة إلى ذلك فلقد أظهرت الأبحاث الحديثة أن الديكلوفيناك يعمل كضدٍ تنافسي competitive antagonist لمستقبلات P2X3 في الخلايا البشرية الحسية sensory neurons والتي تلعب دورا في مسارات إشارات الألم، مما يساهم بشكل أكبر في خصائصه المسكنة[15] .
ورغم فعالية تأثيراته المسكنة إلا أن استعماله لا زال محدوداً بسبب تأثيراته الجانبية التي قد تشمل الجهاز القلبي الوعائي والجهاز المعدي المعوي بالإضافة إلى اختلاطاته الكبدية [16].
للديكلوفيناك عدة أشكال ملحية منها ديكلوفيناك الصوديوم وديكلوفيناك البوتاسيوم وديكلوفيناك دي ايثيل أمين ويعتبر حمض الديكلوفيناك أقل انحلالاً في الماء بالمقارنة مع جميع أملاحه، أما ديكلوفيناك دي ايتيل أمين فيفوقه في ذوبانيته في الماء، [17]، لذا تم اختيارهم كنموذج لتحضير جسيمات بلمرية نانوية ذات تحرر مديد بغية تحسين فعاليتهم وتقليل آثارهم الجانبية.
و لقد تم اختيار محفظته ضمن بلمر بولي كابرولاكتون الذي ينتمي إلى متعددات الإستر الأليفاتية، وهو ذو لون أبيض، كما أنه بلمر نصف بلوري ذو درجة انصهاره 59-64 ᵒم، وله درجة تحول زجاجي عند -60 ᵒم [18]، وهو كاره للماء ويعتبر من أحد أهم البلمرات المستعملة في الطب ويصنع منه الخيوط الجراحية (الدروز) Medical surgical sutures، والأجهزة الطبية المتوافقة حيوياً، ويتميز بلمر بولي كابرولاكتون عن غيره بمقاومته للأوساط الحامضية، وهو بلمر غير سمي ومتدرك ومتوافق حيوياً [20-19]، يتميز بتدركه البطيء لذا فقد استعمل في تحضير أشكال صيدلانية ذات تحرر مديد قد يصل إلى سنة [21]، يتميز بأنه أكثر كراهية للماء من كل بلمرات البولي(لاكتيد-غليكوليك) أسيد PLGA، ويحتاج زمناً أطول منهم للتدرك، كما أن قدرة الخلايا على التقاطه أكبر ]22[.
اعتمد على تحضير جسيمات بلمرية باستخدام وزنين جزيئيين للبلمر المستخدم، ثم انتقاء الصيغة ذات المواصفات الأفضل لتحقيق تحرر مطول بثباتية أعلى، لإجراء فحوص التحرر في الزجاج عليها.
المواد والطرائق Materials and Methods
بولي كابرولاكتون 45,000 و 10,000 ,Aldrich Chemistry، لوترول إف 68 life science, Lutrol f 68, Germany، وديكلوفينك الصوديوم ChemPifine chemicals, India، ايثانول مطلق Ethanol absolute ≥ 99.8% from Sigma- Aldrich، أسيتون Acetone for HPLC from ACROS، أسيتونتريلAcetonitrile Scharlau, HPLC water for HPLC grade، كل الكواشف المستخدمة الأخرى ذات درجة تحليلية مناسبة لـ HPLC.
الفحوص المطبقة
- تحري الشكل وطبيعة السطح:
يتم ذلك بالمجهر الالكتروني الماسح SEM, VEGAII-XMU-TESCAN – Czech Republic، بعد التلبيس بطبقة رقيقة من الكربون الناقل، حيث توضع قطرة على صفيحة نحاسية مغطاة بطبقة رقيقة من الكربون اللابلوري وتترك لتجف في درجة حرارة الغرفة، ثم تلبس بطبقة كربون رقيقة ناقلة باستخدام جهاز EMITECH K975x carbon coater instrument، لتفحص بعد ذلك بالمجهر الالكتروني الماسح باستخدام حزمة الكترونية متولدة عن فرق كمون 30 كيلو فولت.
- تحري الحجم وتجانس توزع الحجم والكمون الكهرحركي
باستخدام جهازDynamic light scattering (DLS)، حيث يم قياس القطر الهيدروديناميكي للجسيمات البلمرية باستخدام مقياس تشتت الضوء الديناميكي (DLS)، وقياس كمونها الكهرحركي في نفس الجهاز باستخدام خلية folded capillary cell بدرجة حرارة 25ºم باستخدام Instrument (DLS; Zetasize Nano-ZS; Malvern Instruments, UK، أجري القياس على ثلاث عينات.
3- دراسة حرائك تحرر الدواء من الجسيمات النانوية المصنعة ببولي كابرولاكتون 45,000
يحضر معلق للجسيمات النانوية وذلك ببعثرة 0.06 غ من الجسيمات النانوية في 7 مل من ماء رباعي التقطير، ثم يوزع 0.5 مل في كل أنبوب يحوي 9 مل دارئة فوسفاتية ذي باهاء (6.8)، يطبق هذا الأمر على عدد من الأنابيب مقابل لعدد الفواصل الزمنية، بحيث يستخدم كل أنبوب لفاصل زمني واحد، وتحضن في حمام مائي هزاز بحركة تقارب 30 هزة/ د وفي درجة حرارة ( 37±0.5℃ )، يؤخذ أنبوب لكل فاصل زمني محدد ويثفل على 10,000 د/ د مدة نصف ساعة في درجة حرارة 10 ⸰م، ثم يخضع الناتج لعملية الترشيح الفائق/ التثفيل باستخدام أنابيب Amicon ultra-15 k10, Millipore 10.000 MWCO,، تنبذ مدة نصف ساعة وبسرعة 8228 RCF(8228×g) في مثفلةEppendorf Centrifuge 5810 R تفحص الرشاحة الناتجة باستخدام جهاز HPLC JASCO LC-NETII/ADC وبرنامج Chrom NAV على عمود Zorbax clipse XDB C18, 4.6 * 150 mm * 5 micrometer.
يتألف الطور المتحرك من 35:65 أسيتونتريل/ ماء رباعي التقطير، ويعدل الباهاء إلى 4 بحمض الخل الثلجي وزمن التدفق 0.6 مل/ د، يتم القياس عند طول الموجة 278 نانومتر، وحرارة الفرن 25° مئوية، تمتعت السلسلة العيارية بالخطية من تركيز 0.03 مكغ/ مل وحتى تركيز 20 مكغ/ مل، بمعامل ارتباط 0.999، هذه المعايرة أجريت حسب طريقة Guterres، [23].
4- مقايسة كفاءة الكبسلة
تؤخذ عينة محضرة بتمديد (ا مل) من المعلق النانوي المحضر وتمدد إلى 133 مل بدارئة فوسفاتية ذات باهاء 6.8، وتخضع لعملية الترشيح الفائق/ التثفيل باستخدام أنابيب Amicon ultra-15, 10 k Millipore 10.000 MWCO، تثفل مدة نصف ساعة وبسرعة 8228 RCF في مثفلةEppendorf Centrifuge 5810 R، تفحص الرشاحات بجهازHPLC JASCO LC-NETII/ADC ، كما ذكر أعلاه، وتحسب كفاءة الكبسلة كما يلي:
كفاءة الكبسلة = كمية الدواء التي تمت محفظته في الجسيمات النانوية x 100 / كمية الدواء المدخل في العملية.
طرائق التحضير:
– تحضير المادة الدوائية: يضاف لكل 100 مل من محلول مائي لديكلوفيناك الصوديوم 1%، 5 مل من حمض كلور الماء 1 نظامي، ويحرك 40 دقيقة حتى انتهاء ترسب بلورات حمض الديكلوفيناك، ترشح البلورات الناتجة وتغسل 3 مرات ب 100 مل ماء رباعي التقطير، تجفف في الفرن بدرجة حرارة 45°م لمدة 72 ساعة، ثم تنقى البلورات مرتين بـ 200 مل من مزيج ايثانول/ ماء رباعي التقطير بنسبة 80/20، تجفف وتحفظ في وعاء عاتم ومحكم الأغلاق.
– تحضير جسيمات بولي كابرولاكتون الحاوية على حمض ديكلوفيناك بطريقة الترسيب النانوي:
– الطور العضوي مؤلف من محلول 4 مل يحوي حمض دكلوفيناك بتركيز 1 ملغ/ مل مع بولي كابرولاكتون 45,000 أو 10,000 بتركيز 10ملغ / مل في 3:1 أسيتون/ ايثانول.
– الطور المائي مؤلف من 40 مل من محلول مائي للوترول إف 68 بتركيز 1.5%، علماً أن حرارة الطور العضوي 30°م وحرارة الطور المائي 5 °م.
يستل الطور العضوي في المائي مع التحريك لمدة 30 دقيقة باستخدام مجانس دوار نوع (Ultra Turrax® T25, Ika.)، بسرعة 21.400 د/ د، ينقل السائل بعدها للتحريك بواسطة دافع ميكانيكي Impeller Marine Propeller بسرعة 600 د/ د لمدة ساعة ونصف، وأخيراً يتم نزع المذيب العضوي باستخدام المبخر الدوار تحت الضغط المنخفض، و الناتج النهائي بعد نزع المذيب هو 10 مل، يجفد الناتج و يحفظ بزجاجات تجفيد في درجة حرارة -20⸰ م.
التحليل الإحصائي
تم إجراء جميع التجارب ثلاث مرات. تُعرض البيانات على شكل المتوسط ± الانحراف المعياري. تم تقييم الدلالة الإحصائية باستخدام اختبار Student’s t-test (p < 0.05).
النتائج Results
يلخص الجدول (1) أدناه خصائص الجسيمات النانوية البلمرية المحضرة والمحملة بحمض الديكلوفيناك.
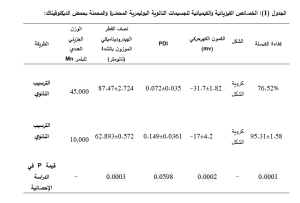


بناء على قياسات الحجم و الكمون الكهرحركي الوارد في الجدول 1، يتوقع أن تتحرر الجسيمات المحضرة من PCL45,000 على فترة زمنية أطول من تلك المحضرة من PCL10,000 ، وذلك بسبب حجمها الأكبر ووزنها الجزيئي الأعلى، كما يتوقع أن تحقق ثباتاً أعلى في الوسط المائي و الحيوي، بسبب امتلاكها كموناً كهرحركياً أعلى، لذا فقد تم اختيار الصيغة المذكورة لتحري حركيات تحررها في الزجاج.
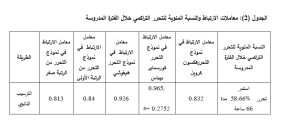
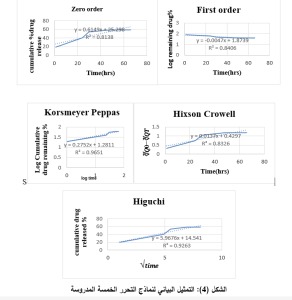
تمت دراسة حرائك تحرر حمض الديكلوفيناك من الجسيمات البلمرية النانوية المحضرة ببولي كابرولاكتون ذي الوزن الجزيئي العددي 45,000 خلال 66 ساعة لمعرفة امكانية تطبيق الجسيمات في أنظمة التحرر الدوائية المديدة [24-26]، وذلك لتفوقه في امتلاك كمون كهرحركي مرتفع فاق 30 ميللي فولت [27] الذي يدل على تباته، وذلك بهدف التنبؤ بالسلوك الذي يتبعه تحرر الدواء من الجسيمات النانوية، بحساب معامل الارتباط R²، حيث تظهر قيم معامل الارتباط لنماذج التحرر الخمسة المدروسة في الجدول (2)، يتم تمثيل النسبة المئوية التراكمية المتحررة من الدواء بيانياً مقابل الزمن في نموذج التحرر من الرتبة صفر Zero-order model، كما يتم تمثيل لوغاريتم النسبة المئوية المتبقية للدواء غير المتحررة مقابل الزمن في نموذج التحرر من الرتبة الأولى First-order model، بينما يتم تمثيل النسبة المئوية التراكمية المتحررة من الدواء مقابل الجذر التربيعي للزمن في نموذج هيغوشي Higuchi model، وتمثيل لوغاريتم النسبة المئوية التراكمية المتحررة من الدواء بيانياً مقابل لوغاريتم الزمن في نموذج كورسماير بيباس Korsmeyer-Peppas model، أما في نموذج هيكسون كرويلHixson Crowell فيتم تمثيله بيانياً بالجذر التكعيبي للنسبة المئوية المتبقية من الدواء منقوصة من الجذر التكعيبي للنسبة المئوية البدئية مقابل الزمن، ويعتبر النموذج ذو معامل الارتباط الأعلى هو الأفضل تمثيلاً لحركية تحرر الدواء [28].
تم اختبار خمسة نماذج رياضية (Zero-order, First-order, Higuchi, Korsmeyer-Peppas, Hixson-Crowell)، وحساب معاملات الارتباط (R²) لكل نموذج كما هو موضح في الجدول (2).
يظهر الجدول (2) أن معامل الارتباط الأعلى قد تحقق في نموذج كورسماير بيباس، وتدل قيمةn على آلية تحرر الدواء، حيث تظهر في الحالة أدناه أن قيمتها أقل من 0.5، مما يدل أن آلية تحرر الدواء من الجسيمات النانوية هي بآلية الانتشار [29].
المناقشة Discussion
أظهرت جسيمات PCL10,000 نصف قطر هيدروديناميكي أصغر (62.89±0.57 نانومتر) مقارنة بجسيمات PCL45,000 (87.47±2.72 نانومتر)، وذي دلالة احصائية مع بقاء مؤشر التبعثر المتعدد (PDI) منخفضًا في كلا النظامين، مما يدل على تجانس عالي.
كما حققت جسيماتPCL10,000 كفاءة كبسلة بلغت 95.31%، وهي أعلى بشكل واضح من (76.52%) لجسيمات PCL45,000 ، وهذا يشير إلى أن الوزن الجزيئي المنخفض للبلمر يعزز من قدرة الجسيمات على احتواء الدواء، ربما بسبب اختلاف في البنية الداخلية للجسيمات الناتجة عن تفاعل المذيب العضوي مع الوسط المائي خلال مرحلة تشكل الجسيمات، أو بسبب اختلاف ألفة الدواء مع البلمر باختلاف أوزانه الجزيئية، إلا أن كفاءة الكبسلة في كلتا الصيغتين تدلان على قدرة البلمر بوزنيه الجزيئيين المختلفين على احتواء الدواء ضمن الجسيمات النانوية.
حققت جسيمات PCL45,000 قيمة جهد كهروحركي (-31.7±1.82 ميلي فولت) أعلى بشكل ملحوظ مقارنةً بـ PCL10,000 (-17±4.2 ميلي فولت)، مما يعكس قوة تنافر كهروستاتيكي أكبر بين الجسيمات. ويعتبر هذا العامل هاماً في تعزيز ثباتية المعلق النانوي ومنع تكتله في الأوساط المائية والحيوية [30]
فبذلك تشير النتائج إلى أن جسيمات بولي كابرولاكتون النانوية و المحملة بحمض الديكلوفينك والمحضرة بطريقة الترسيب النانوي تتميز بالشكل الكروي وبتجانس حجمي عالٍ وحجم مناسب لتطبيقات توصيل الدواء، حيث أن القطر المتوسط في كلتا الصيغتين كان أقل من 200 نانومتر، وهو مثالي لتجاوز الحواجز البيولوجية وتحسين الامتصاص الخلوي [31]
تحرر الديكلوفيناك من الجسيمات النانوية ل PCL45 بدايةً بشكل انفجاري سريع ثم أصبح مطولاً، وقد يعزى بتحرره سريع في البداية إلى الدواء الموضع قرب سطح الجسيمات النانوية، ثم تبعه تحرر مطول الدواء المتواجد ضمن الجسيمات النانوية والمحاط ببلمر كاره للماء بطيء التدرك وعالي الوزن الجزيئي، وقد يعزى أيضاً لتدرك القسم اللابلوري قبل القسم البلوري من البلمر [32]، هذا النوع من التحرر المتحكم فيه يعتبر ميزة هامة لأنظمة توصيل الدواء النانوية، حيث يتيح إطلاقاً سريعاً لجزء من الدواء بحيث يحقق التركيز العلاجي، ثم يتبعه تحرر تدريجي بحيث يحافظ عليه ثابتاً لفترة أطول من الزمن، مما يقلل من التكرار الجرعي ويحد من الآثار الجانبية، حيث يقلل من التراكيز البلاسمية العالية التي يسببها التكرار الجرعي.
الاستنتاجات Conclusions
تمت كبسلة حمض الديكلوفيناك بنجاح ضمن جسيمات نانوية بلمرية لبولي كابرولاكتون 10,000ولبولي كابرولاكتون 45,000 الذي يتميز بفترات تدرك طويلة، مما أتاح تحرر الدواء لفترة طويلة من الزمن، حيث تحقق تحرر ما يقارب 60% من الكمية المحملة ضمن الجسيمات النانوية بآلية الانتشار خلال 66 ساعة، كما تم تقييم مختلف خصائص الجسيمات المحضرة، حيث تمتعت الجسيمات النانوية المحضرة من لبولي كابرولاكتون 45,000 بكمون كهرحركي سالب عالي، مما يوحي باحتمالية تحقيق ثباتاً جيداً في العضوية الحية، أما تلك المحضرة من بولي كابرولاكتون 10,000، وأدت طريقة الترسيب النانوي لكبسلة ما يزيد عن 75% من كمية الدواء المدخلة في عملية التحضير، وتميز حجم الجسيمات المحضرة بتجانس كبير، فبذلك تؤكد هذه الدراسة أن الجسيمات النانوية البوليمرية المحضرة بطريقة الترسيب النانوي والمحمّلة بحمض الديكلوفيناك تتمتع بخصائص فيزيائية وكيميائية ملائمة لتطبيقات توصيل الدواء، مع كفاءة كبسلة مرتفعة، تدعم هذه النتائج إمكانية استخدام هذه الجسيمات كنظام فعال وآمن لتحرير الأدوية، مع إمكانية تحسين التوافر الحيوي وتقليل الآثار الجانبية، ما يجعلها خياراً واعداً في مجال الصيدلة النانوية والتطبيقات العلاجية المستقبل.
يمكن أن تساهم الصيغة المنتقاة المحضرة من بولي كابرولاكتون 45,000في تخفيف آلام المرضى عن طريق تحرير كميات صغيرة من الدواء للحفاظ على مستويات بلاسمية علاجية مع تقليل الآثار الجانبية عند الاستعمال لفترة طويلة، وخاصة أن الدواء يقدم للجسم بحجمه النانوي الذي قد يتيح استهدافاً دوائياً أفضل، إضافة إلى ذلك يمكن أن تساهم في تحسين قبول المرضى لتناول الدواء، خاصة عند كبار السن الذين يعانون من صعوبة تذكر مواعيد الدواء، حيث تقلل هذه الصيغة من التكرار الجرعي، و تساهم عند تناولها ليلاً في تخليص المرضى من الآلام الصباحية المترافقة مع بعض الأمراض، كالتهاب المفاص الروماتوئيدي، يمكن تطبيق هذه الجسيمات عبر أنظمة ايتاء دوائي مختلفة منها الوريدي والعيني وفي الأذن الداخلية والفموي [33-37].
يوصى بإجراء دراسات ثباتية طويلة الأمد، وإجراء دراسات لاحقة في العضوية للتحري عن تأثير خصائص هذه الجسيمات في سلوكها وأدائها وتوزعها ضمن العضوية الحية، وعن ملاءمتها للتطبيق عبر نظم الإيتاء الدوائي المختلفة.
الموافقة الأخلاقية والموافقة على المشاركة Ethics approval and consent to participate
غير قابلة للتطبيق.
تضارب المصالح Conflict of Interests
يقر المؤلفون بعدم وجود مصالح متضاربة.
التمويل Funding
جامعة دمشق.
مساهمات المؤلفين Authors’ contributions
سلافة السليمان: تصميم الدراسة وتحضير العينات واستقصاء خصائصها وكتابة المنشور.
الأستاذ الدكتور أنطون اللحام: الإشراف على العمل البحثي والدعم التقني ومراجعة المنشور.
الأستاذ الدكتور زكي علي عجي الدعم التقني ومراجعة المنشور.
المراجع :
- Ureña NM, et al. The anti-arthritic activity of diclofenac lipid-core nanocapsules: stereological analysis showing more protection of deep joint components. Molecules. 2023;28(13):5219. doi:10.3390/molecules28135219.
- Jain KK. Drug delivery systems – an overview. In: Drug Delivery Systems. Totowa, NJ: Humana Press; 2008. p. 1-50.
- Hussain N, Jaitley V, Florence AT. Recent advances in the understanding of uptake micro-particulates across the gastrointestinal lymphatics. Adv Drug Deliv Rev. 2001;50:107-42. doi:10.1016/s0169-409x(01)00152-1.
- Tosi G. Polymeric nanoparticles for the drug delivery to the central nervous system. Expert Opin Drug Deliv. 2008;5:155. doi:10.1016/j.addr.2011.12.006.
- Zhang Y. Organ-specific gene expression in the rhesus monkey eye following intravenous non-viral gene transfer. Mol Vis. 2003;9:465-72. doi:10.1016/S0161-6420(03)00865-5.
- Albanese A, Tang PS, Chan WCW. The effect of nanoparticle size, shape, and surface chemistry on biological systems. Annu Rev Biomed Eng. 2012;14:1-16. doi:10.1146/annurev-bioeng-071811-150124.
- Schneider M, Stracke F, Hansen S, Schaefer UF. Nanoparticles and their interactions with the dermal barrier. Dermatoendocrinol. 2009 Jul;1(4):197-206. doi:10.4161/derm.1.4.9501.
- Emerich DF, Thanos CG. The pinpoint promise of nanoparticle-based drug delivery and molecular diagnosis. Biomol Eng. 2006;23:171-84. doi:10.1016/j.bioeng.2006.05.026.
- Honary S, Zahir F. Effect of zeta potential on the properties of nano-drug delivery systems: a review (part 1). Trop J Pharm Res. 2013;12(2):255-64. doi:10.4314/tjpr.v12i2.19.
- Zhang W, et al. Effects of morphology and size of nanoscale drug carriers on cellular uptake and internalization process: a review. RSC Adv. 2023;13:80. doi:10.1039/D2RA06888E.
- Sailaja AK, Deshmukh S. Applications of nanoparticles in drug targeting. J Gen Med Clin Pract. 2024;7(15). doi:10.31579/2639-4162/217.
- Liu C, et al. Research and application of targeting nano-drugs. Nano Biomed Eng. 2011;3(2):73-83. doi:10.5101/nbe.v3i2.p73-83.
- Onoue S. Nanodrugs: pharmacokinetics and safety. Int J Nanomedicine. 2014;9:1025-37. doi:10.2147/IJN.S38378.
- Altman R, et al. Advances in NSAID development: evolution of diclofenac products using pharmaceutical technology. Drugs. 2015;75:859-77. doi:10.1007/s40265-015-0392-z.
- Grohs L, et al. Diclofenac and other non-steroidal anti-inflammatory drugs (NSAIDs) are competitive antagonists of the human P2X3 receptor. Front Pharmacol. 2023;14:1120360. doi:10.3389/fphar.2023.1120360.
- Gan TJ, et al. Diclofenac: an update on its mechanism of action and safety profile. Curr Med Res Opin. 2010;26(7):1715-31. doi:10.1185/03007995.2010.486301.
- Baena AY, et al. Preparation and physicochemical characterization of some polyelectrolyte diclofenac complexes. Vitae. 2011;18(3):305-11. Available from: https://revistas.udea.edu.co/index.php/vitae.
- Agarwal S, Speyerer C. Degradable blends of semi-crystalline and amorphous branched poly(caprolactone): effect of microstructure on blend properties. Polymer. 2010;51:1024-32. doi:10.1016/j.polymer.2010.01.020.
- Benoit MA, et al. Preparation and characterization of protein-loaded poly(o-caprolactone) microparticles for oral vaccine delivery. Int J Pharm. 1999;184:73-84. doi:10.1016/s0378-5173(99)00109-x.
- Tang ZG, et al. Control of the domain microstructures of PLGA and PCL binary systems: importance of morphology in controlled drug release. Trans IChemE, Part A. 2007;85(7):1044-50. doi:10.1205/cherd06217.
- Kohn J, Langer R. Bioresorbable and bioerodible materials. In: Ratner B, et al., editors. Biomaterials Science. San Diego: Academic Press; 1996. p. 64-72.
- Eldridge JH, et al. Controlled vaccine release in the gut-associated lymphoid tissues. I. Orally administrated biodegradable microspheres target the Peyer’s patches. J Control Release. 1990;11:205-14. doi:10.1016/0168-3659(90)90133-E.
- Guterres SS, et al. Puisieux. Poly(DL-lactide) nanocapsules containing diclofenac: I. Formulation and stability study. Int J Pharm. 1995;113:57-63. doi:10.1016/0378-5173(94)00254-7.
- Narwade AR, Mahale AM. A research on: Formulation and evaluation of sustained release matrix tablets. GSC Biol Pharm Sci. 2024;29(2):123-57. doi:10.30574/gscbps.2024.29.2.0363.
- Esteruelas G, et al. Diclofenac loaded biodegradable nanoparticles as antitumoral and antiangiogenic therapy. Pharmaceutics. 2023;15(1):102. doi:10.3390/pharmaceutics15010102.
- Badaoui FZ, Bouzid D. Formulation and optimization of diclofenac sodium loaded ethylcellulose nanoparticles. Braz J Pharm Sci. 2022;58:e19586. doi:10.1590/s2175-97902022e19586.
- Németh Z, et al. Quality by design-driven zeta potential optimisation study of liposomes with charge imparting membrane additives. Pharmaceutics. 2022;14(9):1798. doi:10.3390/pharmaceutics14091798.
- Ekenna IC, et al. Comparison of the use of kinetic model plots and DD solver software to evaluate the drug release from griseofulvin tablets. J Drug Deliv Ther. 2022;12(2-s):5-13. doi:10.22270/jddt.v12i2-S.5402.
- Akombaetwa N, et al. Formulation and assessment of the efficacy and stability of an ointment containing Ocimum americanum L. extract. Clin Complement Med Pharmacol. 2023. doi:10.1016/j.ccmp.2022.100078.
- Krstić M, Medarević Đ, Đuriš J, Ibrić S. Self-nanoemulsifying drug delivery systems (SNEDDS) and self-microemulsifying drug delivery systems (SMEDDS) as lipid nanocarriers for improving dissolution rate and bioavailability of poorly soluble drugs. In: Grumezescu AM, editor. Lipid Nanocarriers for Drug Targeting. William Andrew Publishing; 2018. p. 473-508. doi:10.1016/B978-0-12-813687-4.00012-8.
- Kulkarni SA, Feng SS. Effects of particle size and surface modification on cellular uptake and biodistribution of polymeric nanoparticles for drug delivery. Pharm Res. 2013;30(9):2512-22. doi:10.1007/s11095-012-0958-3.
- Miyajima M, et al. Effect of polymer crystallinity on papaverine release from poly (-lactic acid) matrix. J Control Release. 1997;49:207-15. doi:10.1016/S0168-3659(97)00081-3.
- Mok ZH. The effect of particle size on drug bioavailability in various parts of the body. Pharm Sci Adv. 2024;2:100031. doi:10.1016/j.pscia.2023.100031.
- Chenthamara, D., Subramaniam, S., Ramakrishnan, S.G. et al. Therapeutic efficacy of nanoparticles and routes of administration. Biomater Res 23, 20 (2019). https://doi.org/10.1186/s40824-019-0166-x.
- Merisko-Liversidge E, Liversidge GG. Nanosizing for oral and parenteral drug delivery: A perspective on formulating poorly-water soluble compounds using wet media milling technology. Adv Drug Deliv Rev. 2011;63(6):427-440. doi:10.1016/j.addr.2010.12.007.
- Amrutkar CS, Patil SB. Nanocarriers for ocular drug delivery: recent advances and future opportunities. Indian J Ophthalmol. 2023;71(6):2355-2366.
- Banerjee, A., Qi, J., Gogoi, R., Wong, J., & Mitragotri, S. (2016). Role of nanoparticle size, shape and surface chemistry in oral drug delivery. Journal of Controlled Release, 238, 176–185. https://doi.org/10.1016/j.jconrel.2016.07.051.