تحضير مستحلبات ميكروية من الكلوزابين الأنفيّ وتقييمها في الزجاج
2025-08-23 | المجلد السابع العدد السادس - المجلد السابع | مقالات بحثيةميري رياض الدير | محمد عبد الرؤوف عثمان
الملخص
يعتبر العلاج الدوائي الجهازي في مرض الفصام تحدياً كبيراً بسبب وجود الحاجز الدموي الدماغي (BBB) والبروتين السكري (Pgp) الذي يشكّل عائق ويمنع دخول العديد من الأدوية إلى الدماغ.
أثبت العديد من الباحثين أن العديد من الصيغ الأنفية مثل المستحلبات الميكروية والجسيمات النانوية، يمكن استخدامها لنقل جزيئات الدواء بشكل فعال إلى الجهاز العصبي المركزي (CNS)، عبر المسارات العصبية الشمية والعصب ثلاثي التوائم.
في هذا البحث تم تحضير مستحلبات ميكروية من الكلوزابين للإيتاء الأنفيّ، باستخدام سواغات مختلفة مثل حمض الزيت، توين 80، وبولي ايثيلين غليكول 400.
بهدف تحسين انحلال الكلوزابين الكاره للماء وتوافره الحيوي، ونفاذيته إلى الدماغ، وللتقليل من جرعة الدواء مما يقلل التأثيرات الجانبية الغير محتملة من المرضى.
وقُيِّمت الخصائص الفيزيوكيميائية للصيغ الناتجة من حيث الشفافية، الثباتية الفيزيائية، النفاذية، محتوى الدواء، قيم باهاء الصيغ، اللزوجة. وأجريت دراسات التحرر في الزجاج باستخدام أكياس التحال, ودرست التآثرات بين المادة الدوائية والسواغات، وقُيِّمَت الصيغ باستخدام المجهر الالكتروني الماسح (SEM)، المسح الطيفي بالأشعة تحت الحمراء (FTIR)، والمسح الحراري التفاضلي (DSC)، وتم تقييم تأثير تركيز مزيج العوامل الفعالة على السطح والعوامل المساعدة على معدل تحرر الكلوزابين.
تمّ تحضير مستحلبات شفافة ذات نفاذية ضوئية عالية، ثابتة فيزيائياً، وكانت قيم باهاء الصيغ (5.23-5.7) ملائمة للإيتاء الأنفي. أعطت جميع الصيغ تحرراً مديداً خلال 24 ساعة، وأظهرت نتائج المسح الطيفي بواسطة FTIR وDSC قلّة التآثرات بين المادة الدوائية والسواغات المستخدمة.
كلمات مفتاحية : الإيتاء الأنفي، مستحلبات ميكروية، كلوزابين، الفُصام، العوامل الفعالة على السطح Intranasal Administration, Microemulsion, Clozapine, Schizophrenia, Surfactants
المقدمة Introduction
وفقًا لمنظمة الصحة العالمية (WHO)، يعاني حوالي 20 مليون شخص من مرض الفصام في جميع أنحاء العالم، كما أن الأشخاص المصابون بالفصام يموتون في سن مبكرة، بتواتر 3-4 مرات أعلى من عامة السكان.
يتطور المرض بسبب التغير في مستويات النواقل العصبية في الدماغ، مثل الدوبامين والسيروتونين.
ان السبب الأساسي لتطور الفصام هو زيادة مستويات الدوبامين في منطقة النواة المتكئة Nucleus Accumbens)) في الدماغ، علاوة على ذلك، يؤدي انخفاض مستويات الدوبامين في المنطقة الأمامية الصدغية من الدماغ في النهاية إلى ظهور أعراض إيجابية وسلبية للمرض، على التوالي، إذ تهدف طرائق العلاج إلى تقليل مستويات الدوبامين وبالتالي التخلص من فرط النشاط .[1]
ذهان غير نمطي متعدد المستقبلات معتمد لعلاج الفصام المقاوم للأدوية .[2]
يؤثر الكلوزابين من خلال مجموعة من التأثيرات المناهضة للمستقبلات D2 في المسار الحوفي المتوسط، ومستقبلات 5-HT2A في القشرة الأمامية. إنّ حجب المستقبلات D2 يخفّف الأعراض الإيجابية بينما حجب المستقبلات 5-HT2A يخفف الأعراض السلبية.
يصل الكلوزابين الممتص من الأقراص الفموية إلى الدماغ بِنِسب ضئيلة بسبب:
الحاجز الدموي الدماغي، يتخرّب في بيئة الجهاز الهضمي القاسية، والمرور الكبدي الأول.
الكلوزابين كاره للماء، توافره الحيوي أقل من (27%) بسبب تأثير الاستقلاب الكبدي الأول العالي بواسطة CYP1A2 وCYP3A4، لتكوين نوركلوزابين (Norclozapine) أو N-desmethylclozapine، والذي يعتبر المستقلب الرئيسي 20-30%)) [3].
لا يعتبر الكلوزابين الخط الأول في العلاج لأنه قد يكون من الصعب في كثير من الأحيان على بعض المرضى تحمله لأن بعض الآثار الجانبية يمكن أن تكون خطرة ومهددة للحياة مثل (التخدير، وزيادة الوزن، سيلان اللعاب، التهاب عضلة القلب، والنوبات الصرعية، وندرة المحببات ((agranulocytosis، ونقص الحركة المعدية المعوية) [4].
يتوقف (69-82%) من المرضى عن تناول الدواء بسبب آثاره الجانبية التي لا تُحتَمَل .[3]
لتجنب المرور الكبدي الأول وكذلك لتعزيز التوافر الحيوي وكفاءة التهديف الدماغي لـلكلوزابين، ينبغي البحث عن طرائق بديلة للإيتاء [5].
في الآونة الأخيرة، اكتسب الاهتمام بالطريق الأنفي لتهديف الأدوية إلى الدماغ، لتجاوز الحاجز الدموي الدماغي أهمية، بفضل الارتباط الفريد بين الأنف والدماغ من خلال مسار العصب الشمي [3].
يمكن للأدوية القابلة للذوبان في الماء أن تنتشر بسهولة في الجسم، بينما الأدوية الذوابة في الدسم، ضعيفة الذوبان في الماء، توافرها الحيوي منخفض. تعتبر المستحلبات الميكروية من الأنظمة المناسبة لتوصيل الأدوية الكارهة للماء، حيث أنها ثابتة حرارياً، ولها خصائص فريدة، إذ تتمتع بأبعاد قطيرات صغيرة (أبعاد نانوية)، وثبات عالي، ومساحة سطح واسعة، وتوتر سطحي منخفض وتتشكل عفوياً Spontaneously [6].
يهدف هذا البحث إلى صياغة مستحلبات ميكروية من الكلوزابين للإيتاء الأنفي، باستخدام سواغات مختلفة للتغلب على ضعف انحلال الكلوزابين في الماء وتحسين توافره الحيوي، ويمكن أن يتجنب هذا الطريق أيضاً عملية المرور الكبدي الأول ويوفر طريقة عمليّة وغير جراحية وفعالة لتوصيل الدواء إلى الدماغ، وبالتالي الحصول على تحرّر مديد للدواء وزيادة التوافر الحيوي، إضافة إلى تقييم الصيغ المحضرة من حيث خصائصها الفيزيوكيميائية والميكانيكية، ومن ثم تحديد الصيغ التي تحقق أفضل الخصائص.
المواد والطرائق Materials and methods
الموادMaterials :
الكلوزابين Clozapine)) من (Global Calcium, India)
حمض الزيت Oleic Acid)) من (Panreac corp, Spain)
ايزوبروبيل ميريستات (Isopropyl Myristate) من (Cisme, Italy)
زيت دوار الشمس من (Croda, India)
بروبيلين غليكول propylene glycol)) والغليسيرين(Glycerin) من Hutong Global, China))
بولي ايتلين غليكول 400 polyethylene glycol 400)) من (Sigma-Aldrich, Germany)
توين 80 و20 Tween 80,20)) من Riedel-de Haen, Germany))
الطرائقMethods :
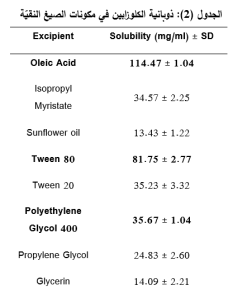
دراسة ذوبانية الكلوزابين في السواغات النقية:
تم دراسة الذوبانية بطريقة الدورق الهزاز, حيث تم إضافة كمية فائضة من الكلوزابين وبعثرتها في 2 مل من الزيوت والعوامل الفعالة سطحياً والمواد المساعدة في أنابيب تثفيل، ثم تمّ تعريض العينات للاهتزاز ضمن المازج (Shaker) لمدة 48 ساعة بدرجة حرارة 25°C للوصول الى التوازن, ثفلت بعدها بسرعة 6000 دورة بالدقيقة لمدة نصف ساعة. أُخِذَ 1 مل من السائل الطافي ومدد بالإيثانول 96%، وتمّت المقايسة بمقياس الطيف الضوئي عند طول الموجة 232 nm.
تحضير المستحلبات الميكروية:
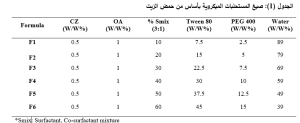
تم تحضير 6 صيغ بأساس من حمض الزيت 1% ومزيج من مواد فعالة سطحياً ومواد مساعدة (Smix) توين 80 وPEG 400 بنسب 1:3 على التوالي وبتراكيز من 10% الى.60%
تم مزج حمض الزيت وتوين 80 و PEG 400 على حمام الأمواج فوق الصوتية، Digital ultrasonic cleaner, Italy)، لمدة 10 دقائق، ثم تم إضافة المادة الفعالة والتحريك على محرك مغناطيسي بدرجة حرارة40°C حتى تمام الانحلال، ثم تمّ اضافة الماء قطرة فقطرة مع التحريك بسرعة 750 دورة في الدقيقة لمدة 15 دقيقة، ثمّ يُعرّض المستحلب للأمواج فوق الصوتية لمدة 15 دقيقة ويُترك للتقييم في اليوم التالي.
تقييم الصيغ المحضرة:
فحص المظهر الفيزيائي :[7] Physical appearance
الحالة الفيزيائية عيانياً: الشفافية، انفصال الأطوار، الرواق/ العكر.
قياس نفاذية المستحلبات الميكروية [8] Transmittance %:
يعتبر فحص نفاذية الضوء ضمن عينة المستحلب الممددة خاصة ضوئية مميزة له تشير أو تقيس عكر هذا المستحلب، من خلال علاقتها بأبعاد قطيرات الطور المبعثر. تم القياس باستخدام جهاز الطيف الضوئي(PG Instruments T80+, UK) ، حيث أُخِذَ 1مل من كل عينة مستحلب ومُددت باستخدام الماء المقطر 10 أضعاف، ثم قيست نفاذيته (T%) عند طول موجة 650 نم باستخدام الماء المقطر كناصع.
فحص الثبات الفيزيائي للمستحلبات الميكروية Physical Stability [9]:
تمت دراسة الثباتية الفيزيائية للمستحلب الميكروي باستخدام التثفيل (HERMLE Z 200A, Germany) من خلال تثفيل 5غ من المستحلبات الدوائية بسرعة 6000 rpmولمدة نصف ساعة بدرجة حرارة 25°C، تعتبر المستحلبات ثابتة في نهاية الفحص في حال عدم حدوث أي فصل للأطوار أو ترسب للمادة الفعالة.
محتوى الدّواء [10] Drug content:
تم وزن كميّة من المستحلب مكافئة إلى (5 ملغ) دواء وحلّها في بالون مُعاير سعة 100 مل باستخدام الوقاء الفوسفاتي + 10% ايثانول، ثم أُخِذَ 1 مل من المحلول السّابق وتمّ تمديده في بالون مُعاير سعة 10 مل بواسطة المزيج السابق حتى خطّ العيار، وتم تحليل المحلول النّاتج بعد ترشيحه بواسطة مرشحة ميكروية (0.22 ميكرومتر)، باستخدام مقياس الطّيف الضّوئيّ عند طول موجة امتصاص أعظمي 232 nm.
قياس لزوجة المستحلبات [10] Viscosity Measurement:
أُجري فحص اللزوجة على عيّنات بحجم 50 مل من كافة الصيغ المُحضّرة، وذلك بواسطة جهاز قياس لزوجة دورانيّ FUNGILAB S.A. VISCO ELITE, Spain)) باستخدام طريقة بروكفيلد Brookfield method)) عند درجة الحرارة 30 درجة مئويّة، حيث أُخذت الشروط المناسبة للصيغ من حيث نمط المغزل spindle (نوع R6) وسرعة الدوران 100 rpm. يُعبّر عن قيمة اللزوجة بواحدة السنتيبواز cP.
قياس درجة الباهاء [11] pH Measurement:
تم استخدام جهاز قياس قيمة باهاء الوسط (Hanna Instruments pH 211, Italy), حيث تمّ أخذ 1مل من كل عينة مستحلب ومُدِّدت باستخدام الماء المقطر 10 أضعاف، ثم قياس درجة ال pH له.
قياس الناقلية الكهربائية Conductivity Measurement [12]:
تم قياس الناقلية الكهربائية للـمستحلبات عند درجة حرارة الغرفة باستخدام مقياس الناقلية
(APERA INSTRUMENTS, EC700 Conductivity Meter)، المعاير بمحلول قياسي من KCl. تم غسل القطب قبل كل قياس باستخدام الماء المقطر مرة ثم الغسل بالعينة مرتين، يُعبّر عن قيمة الناقلية بواحدة (µS/cm).
قرينة الانكسار Refractive Index [13]:
تم تحديد قرينة الانكسار للمستحلبات الميكروية المحضرة عند درجة حرارة 25 درجة مئوية بواسطة مقياس الانكسار (CARL ZEISS JENA) وذلك بوضع قطرة واحدة من المستحلب الميكروي على الشريحة، تم معايرة مقياس الانكسار باستخدام قرينة الانكسار للماء المقطر.
قياس متوسط أبعاد الجسيمات ومَنسَب التشتُّت المتعدد (PDI) :[14]
قيس متوسط أبعاد الجسيمات (Droplet Size) باستخدام تقنية تشتت الضوء الديناميكي Dynamic Light Scattering DLS ضمن جهاز (Nanosizer, Malvern, UK) لتقييم أبعاد القطيرات، والجسيمات المُبعثرة ومدى تجانس توزعها بالاعتماد على مَنسَب التشتُّت المتعدد Polydispersity Index (PDI)، والذي كلما صَغُرت قيمته وكانت أقل من .50 كان مجال توزع هذه الأبعاد ضيق أي عينة متجانسة. تمّ الفحص بأخذ (1 مل) من كل صيغة وتمديدها بالماء ثنائي التقطير 50 ضعف.
المجهر الالكتروني الماسح:[15] Scanning Electron Microscopy (SEM)
تم استخدام مجهر الكتروني ماسح (TESCAN, VEGA, Czech Republic) لفحص شكل وخواص سطح وحجم قطيرات الطور الداخلي، مُدِّدَت العينة عشر مرات باستخدام الماء المقطر بدون أي طلي.
دراسة تحرر المادة الدوائية من المستحلبات الميكروية باستخدام أكياس التحال[10] :
تمّ استخدام أكياس التحال Aldon Corporation, USA)) وهي عبارة عن غشاء نصف نفوذ من أسيتات السيللوز، ذات (MWCO 12-14 KDa) لدراسة تحرر الكلوزابين من المستحلبات الميكروية في الزجاج:
خطوات العمل:
أُخِذَ 1 مل من كل صيغة محضرة، ووضعت ضمن كيس التحال المرطب مسبقاُ عن طريق نقعه ضمن وقاء فوسفاتي (pH 6.4) لمدة 24 ساعة.
وضع كيس التحال، بعد اغلاقه، ضمن 200 مل من مزيج وقاء فوسفاتي (pH 6.4) + 10% ايثانول 96% ضمن بيشر زجاجي والتحريك بسرعة 200 rpm بدرجة حرارة 1±34 درجة مئوية، باستخدام حمام مائي ومحرك مغناطيسي China) , (DLAB MS7-H550، وسحب 5 مل من البيشر الزجاجي بفواصل زمنية محددة (0.5,1,2,3,4,5,6,7,8,24 ساعة)، مع مراعاة تعويض الحجم المسحوب مباشرة بالمزيج السابق في كل مرة للحفاظ على شرط الإغراق (Sink Condition).
حُدِّدَت النسبة المئوية المتحررة عن طريق قياس الامتصاص عند طول موجة 232 nm باستخدام مقياس الطيف الضوئي، مقابل مزيج وقاء فوسفاتي (pH 6.4) + 10% ايثانول 96% كشاهد.
الدّراسة الإحصائية:
تمَّ اعتماد اختبار (One-way Anova) للنسب المئوية المتحررة من الكلوزابين النقي والصيغ المحضرة، واعتُبرت الفروق ذات أهمية إحصائية عند مستوى دلالة (P < 0.05).
دراسة التآثرات بين الكلوزابين والسواغات المستخدمة Drug – excipient interactions:
المسح الحراري التفاضلي Differential Scanning Calorimetry [16]:
تم اجراء المسح الحراري التفاضلي باستخدام جهاز (SETARAM DSC 131,France)، حيث تم وزن عينات (4-5 ميلي غرام) بشكل دقيق، مع وضعها ضمن بوتقة خاصة من الألمنيوم، وتمّ احكام اغلاقها جيدا بواسطة مكبس خاص. أجري الاختبار مع استخدام بوتقة ثانية فارغة من الالمنيوم كشاهد، وذلك بتعريض العينات إلى حرارة بمعدل متزايد 10°C/min. تم اجراء الاختبار على المسحوق النقيّ للكلوزابين والسواغات، من ثم على المزائج الفيزيائية للمادة الفعالة مع كل سواغ وذلك بنسب (1:1).
المسح الطيفي بالأشعة تحت الحمراء FTIR Spectroscopy [17]:
تم القيام بالمسح بالأشعة تحت الحمراء باستخدام جهاز (Bruker IR-10049361 FTIR, Germany)، لكل من الكلوزابين ومن ثمّ على المزيج الفيزيائي للمادة الفعالة مع كل سواغ مُستخدَم، بنسب (1:1)، وذلك بهدف التحري عن إمكانية حدوث أي تآثر بين الدواء والسواغات الداخلة في الصيغ.
النتائج والمناقشة Results and Discussion
نتائج دراسة ذوبانية الكلوزابين في السواغات النقية:
يوضح الجدول (2) قيم ذوبانية الكلوزابين في الزيوت والعوامل الفعالة سطحياً والعوامل المساعدة.
تم اختيار السواغات التي أبدت قدرة أكبر على حل الكلوزابين (حمض الزيت، بولي إيثيلين غليكول 400، التوين 80).
نتائج تقييم الصيغ المحضرة:
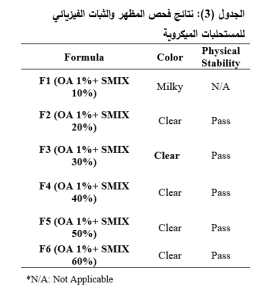
نتائج فحص المظهر والثبات الفيزيائي:
يبين الجدول (3) نتائج فحص المظهر والثبات الفيزيائي للمستحلبات, حيث كانت الصيغة F1 عكرة بلون حليبي أما باقي الصيغ المحضرة كانت: شفافة وبلون أصفر. يبين الشكل (1) مظهر الصيغ التي حققت الثبات والمظهر الفيزيائي.

نتائج دراسة النفاذية الضوئية للمستحلبات T%:
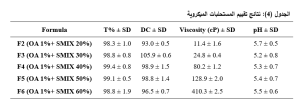
يبين الجدول (4) قيم نفاذية الصيغ المحضرة، حيث تراوحت قيم النفاذية للصيغ المحضرة بين %98.33 إلى 99.38%، حيث كانت أعلاها في الصيغة F4. مما قد يدل على صغر أبعاد الطور الداخلي.
نتائج دراسة محتوى الصيغ المحضرة من المادة الفعالة:
يبين الجدول (4) نتائج المحتوى الفعلي من المادة الفعالة ضمن العينات المأخوذة من كل صيغة محضرة بثلاث تكرارات. تراوحت نتائج محتوى الصيغ المحضرة بين %93.0 و%105.9 وذلك يتوافق مع متطلّبات دستور الأدوية الأمريكي USP 44 [18].
نتائج دراسة لزوجة الصيغ المحضرة:
تراوحت قيم اللزوجة بين 11.4 cP و410.3 cP. (الجدول 4) إذ تبين أنّ زيادة تراكيز مزيج العوامل الفعالة على السطح والعوامل المساعدة يؤدي إلى زيادة لزوجة الصيغ المحضرة، قد يكون السبب هو أن السلاسل المحبة للماء للعامل الفعال على السطح غير الأيوني (توين 80) والعامل المساعد (PEG 400) تتميه بشدّة وترتبط ببعضها البعض بروابط هيدروجينية مما يسمح بتداخل قوي[19] .
نتائج دراسة قيم باهاء pH المستحلبات:
تراوح مجال القيم لجميع الصيغ المُحضّرة ما بين 5.2 و5.7، (الجدول 4)، وهذا يعني أنّ الصيغ ضمن مجال الباهاء pH الفيزيولوجي المقبول 6.5) -4.5) والذي لا يُسبّب تخريشاً للأنف، ذلك أن حمض الزيت حمض ضعيف، وبقيّة مكونات الصيغ غير متأيّنة .[20]
نتائج قياس الناقلية الكهربائية وقرينة الانكسار:
تراوح مجال قيم الناقلية الكهربائية للصيغ المُحضّرة ما بين 65.6 و161.8 ميكروسيمنس/سم أي أن الناقلية الكهربائية للمستحلبات ازدادت بزيادة تراكيز الشوارد في الطور المائي.
وقد ورد في الدراسات السابقة أن الناقلية الكهربائية للمستحلبات الميكروية من نمط الماء في الزيت (w/o) تكون عادة أقل من (µS/cm) 10، بينما تتمتع المستحلبات من نمط الزيت في الماء (o/w) بناقلية أعلى، تزيد عن (µS/cm)10 .[19]
أما مجال قيم قرائن الانكسار للصيغ المحضرة تراوح بين 1.366 و1.426، وبالمقارنة مع قيم قرائن انكسار مكونات الصيغ:
الماء: 1.328، حمض الزيت: 1.467، التوين 80: 1.475، :PEG 400 1.469.
تبين أن ازدياد تراكيز التوين 80 وبولي ايثيلين غليكول سبب زيادة قرائن انكسار المستحلبات، وذلك لأن كل منهما له طبيعة محبة للماء، لأنّ عند مزج التوين 80 ذو الكثافة (1.08 g/cm3) والـ PEG 400 ذو الكثافة (1.12 g/cm3) مع الماء تزداد الكثافة وبالتالي تزداد قرينة الانكسار.
دراسة أبعاد قطيرات المستحلبات بـالـ Nanosizer:
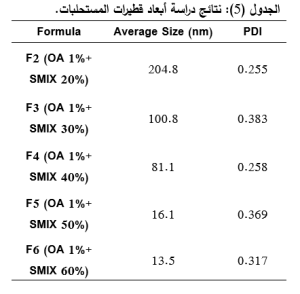
يوضح الجدول (5) نتائج متوسط أبعاد قطيرات المستحلبات الميكروية باستخدام جهاز الـ Nanosizer.
اعتمد متوسط أبعاد القطيرات على تراكيز الـ Smix، تراوحت أبعاد قطيرات المستحلبات الميكروية بأساس من حمض الزيت بين 13 و204 نانومتر.
انخفضت أبعاد القطيرات بازدياد تراكيز مزيج العامل الفعال على السطح والعامل المساعد (Smix) بفارق يعتد به احصائياً (P value < 0.05).
وهو ما يتوافق مع دراسة Ramreddy وزملائه عام 2018 حيث قاموا بتحضير مستحلبات ميكروية من الديازيبام للإيتاء الأنفي[16] .
كانت قيم الـ PDI أقل من 0.5 لجميع صيغ المستحلبات الميكروية مما يشير إلى تقارب حجم القطيرات وتجانسها.
نتائج المجهر الالكتروني الماسح :(SEM)
يُظهِر الشكل (2) صور ال SEM للمستحلبات الميكروية حيث تظهر القطيرات بأشكال كرويّة.

نتائج دراسة تحرر المادة الدوائية من الصيغ المحضرة في الزجاج:
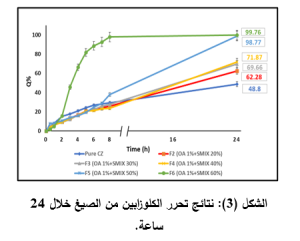
امتدّ تحرر جميع الصيغ إلى 24 ساعة ماعدا الصيغة F6، حيث حررت 97% من المادة الفعالة خلال 8 ساعات أما باقي الصيغ فأعطت تحرراً بين 23% و38% خلال 8 ساعات وتحرراً بين 62% و98% خلال 24 ساعة.
ومن خلال الدراسة الإحصائية (One-way Anova) على الصيغ المشتركة بنوع الزيت والمختلفة بنسبة Smix تبين وجود فارق جوهري ,(P<0.05, n=3) في التحرر بين الصيغ والمادة النقية عند الـ 24 ساعة، حيث كانت قيمة P-Value = 0.0075. مما يبين أثر زيادة نسبة Smix في تحسين التحرر، حيث ازداد معدل تحرر الكلوزابين بازدياد تركيز مزيج التوين 80 وPEG 400، وهو ما يتوافق مع دراسة قام بها Jain وزملائه عام 2023 حيث قاموا بتحضير مستحلبات ميكروية من الكيتوكونازول، وجدوا أنّ زيادة تراكيز الـ Smix سيؤدي إلى تعزيز انحلالية الدواء في المستحلب الميكروي وأبعاد قطيرات أصغر مما يؤدي إلى زيادة مساحة السطح وبالتالي ازدياد معدل التحرر .[21]
يبين الشكل (3) النسب المئوية المتحررة (Q%) مقابل الزمن (T) لكل من الصيغ المدروسة والكلوزابين النقي خلال 24 ساعة.
نتائج دراسة التآثرات بين الكلوزابين والسواغات المستخدمة:
نتائج المسح الحراري التفاضلي DSC:
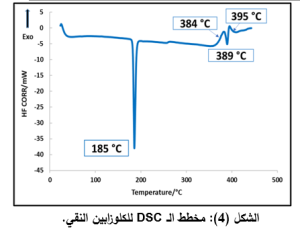
في مخطط الـ DSC للكلوزابين النقي (الشكل 4) يُلاحَظ:
قمة حادة ماصة للحرارة عند الدرجة 185 مئوية، تشير إلى درجة انصهار الكلوزابين وهي قمة حادة مما يدل على طبيعة الكلوزابين البلورية ونقاوته .[22]
قد تشير القمة الماصة للحرارة عند درجة 389 مئوية الى انفصال حلقة الببرازين عن حلقة البنزوديازبين السباعية، اما القمتين الناشرتين للحرارة عند درجتي الحرارة 384،395 قد تشيران الى تفكك المجوعات الأمينية وتخرب الكلوزابين على الترتيب.
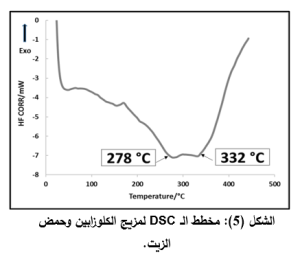
في مخطط الـ DSC لمزيج الكلوزابين وحمض الزيت (الشكل 5):
غابت قمة انصهار الكلوزابين، مما يدل على انحلاله بحمض الزيت، القمتين الماصتين للحرارة عند درجتي الحرارة 332،278 تشيران الى درجة غليان وتخرب حمض الزيت على الترتيب.
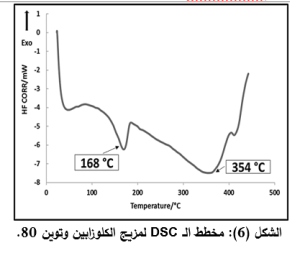
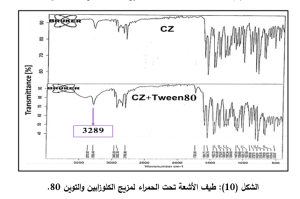
في مخطط الـ DSC لمزيج الكلوزابين والتوين 80 (الشكل 6):
هناك انزياح في درجة انصهار الكلوزابين إلى الدرجة °C168، وانخفاض في شدة القمة مما قد يدل على انحلال جزئي للكلوزابين في التوين 80، أيضاً قمة ماصة للحرارة عند درجة الحرارة 354 قد تشير الى تخرب التوين 80.
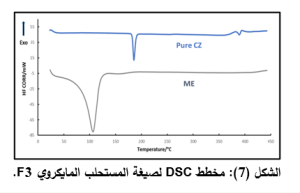
في مخطط الـ DSC لصيغة المستحلب الميكروي F3 (الشكل 7):
هناك غياب قمة انصهار الكلوزابين، مما يدل على انحلاله الكامل في الصيغة، القمة الماصة للحرارة عند درجة الحرارة 106 قد تشير الى تبخر ماء المستحلب.
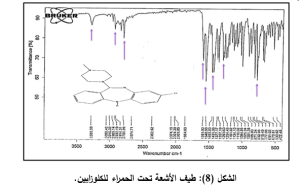
نتائج المسح الطيفي بالأشعة تحت الحمراء FTIR Spectroscopy:
يوضح الشكل (8)، طيف الأشعة تحت الحمراء للكلوزابين، حيث يُظهِر امتطاط المجموعة الأمينية العطرية عند العدد 3285، امتطاط C-H العطرية عند العددين 3056, 3001، وامتطاط C-H الألفاتية عند الأعداد 2969,2933,2800 ، انحناء رابطة الأمين الثانوي عند العدد 1592، امتطاط الرابطة الايمينية عند العدد 1549، امتطاط الرابطة الكربونية المضاعفة عند العددين 14321454, وامتطاط رابطة الأمين الثالثي عند العدد 1293، ورابطة C-Cl عند العدد 815[22,23] .
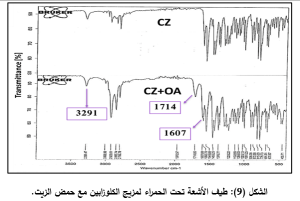
في طيف مزيج الكلوزابين مع حمض الزيت (الشكل 9)، كان هناك انزياح في قمة المجموعة الأمينية العطرية، وهذا ربما يشير الى تداخل بين حمض الزيت والكلوزابين، أيضا هناك انزياح في قمة المجموعة الكربوكسيلية لحمض الزيت من العدد 1708 الى 1714 مع انخفاض شديد بشدة القمة وظهور قمة جديدة عند العدد الموجي 1607 قد تعود إلى التآثر أو التفاعل بين حمض الزيت الضعيف والكلوزابين القلوي الضعيف.
أما في طيف مزيج الكلوزابين وتوين 80 (الشكل 10)، هناك انزياح واتساع القمم الدالة على مجموعات الهيدروكسيل في التوين 80 من العدد 3473 الى 3373 وأيضا انزياح في قمم المجموعات الأمينية العطرية من العدد الموجي 3285 الى 3289 وهذا ربما يشير الى تشكل روابط هيدروجينية بين المجموعة الهيدروكسيلية للتوين 80 والمجموعة الأمينية للكلوزابين.
تم تقييم واختيار الصيغ والتحري عن التآثرات بين الدواء والسواغات، فلم يلاحظ تغيرات جوهرية في أطياف الـ FTIR ومخططات التحليل الحراري للدواء عند صياغته بشكل مستحلبات.
الاستنتاجات Conclusions
تمَّ صياغة مستحلبات ميكروية من الكلوزابين الكاره للماء، لتحسين انحلاله وتوافره الحيوي.
تمتعت جميع الصيغ المحضرة بثباتية فيزيائية، وكانت قيم باهاء الصيغ المحضرة ملائمة للإيتاء الأنفيّ،
وتمتعت بخصائص انسياب مناسبة. كما تبين أنّ زيادة تراكيز مزيج العوامل الفعالة على السطح والعوامل المساعدة يؤدي إلى زيادة لزوجة الصيغ المحضرة، وزيادة معدلات تحرر الكلوزابين، إذ حرّرت جميع الصيغ بشكل مستديم للدواء خلال 24 ساعة. تمّ دراسة التآثرات بين الدواء والسواغات في الصيغ والحصول على مستحلبات ملائمة للتطبيق السريري.
قائمة الاختصارات List of abbreviations
| المقابل باللّغة العربيّة | الاختصار | المقابل باللّغة الإنكليزيّة |
| الحاجز الدموي الدماغي | BBB | Blood Brain Barrier |
| التصنيف الصيدلاني الحيوي | BCS | Biopharmaceutical Classification System |
| الماسح الحراري التّفاضلي | DSC | Differential scanning calorimetry |
| محتوى الدّواء | DC | Drug content |
| تحويل فورييه في طيف الأشعّة تحت الحمراء | FTIR | Fourier transform infrared spectroscopy |
| الجهاز العصبي المركزي | CNS | Central Nervous System |
| المستحلبات الميكروية | ME | Microemulsion |
| غير قابل للتطبيق | N/A | Not Applicable |
| حمض الزيت | OA | Oleic Acid |
| بولي ايثيلين غليكول 400 | PEG 400 | Polyethylene Glycol 400 |
| مَنسَب التشتُّت المتعدد | PDI | Polydispersity Index |
| البروتين السكري P | Pgp | P-glycoprotein |
| مجهر إلكتروني ماسح | SEM | Scanning electron microscope |
| مزيج العوامل الفعالة سطحياً والعوامل المساعدة | Smix | Surfactant, Co-surfactant mixture |
| دستور الأدوية الأمريكي | USP | United States Pharmacopeia |
| منظمة الصحة العالمية | WHO | World Health Organization |
الموافقة الأخلاقية والموافقة على المشاركة Ethics
approval and consent to participate
غير قابلة للتطبيق.
تضارب المصالح Conflict of interests
يقرُ المؤلفون بعدم وجود مصالح مُتضاربة.
التمويل Funding
مُوِّل هذا البحث من قبل جامعة دمشق.
مساهمات المؤلفين Author’s contributions
تولت المؤلفة (ميري رياض الدير) جميع الأنشطة المتعلقة بالبحث من تصميم الدّراسة، جمع البيانات، التّحليل، وكتابة المقال.
كان المشرف (الدكتور محمد عبد الرؤوف عثمان) مسؤولاً عن تقديم الإرشادات الأكاديمية، وضمان جودة المحتوى من خلال مراجعة المسودة النّهائية.
المراجع :- Rajendran R, Menon KN, Nair SC. Nanotechnology Approaches for Enhanced CNS Drug Delivery in the Management of Schizophrenia. Advanced Pharmaceutical Bulletin. 2021;12(3):490–508.
- De Berardis D, Rapini G, Olivieri L, Di Nicola D, Tomasetti C, Valchera A, et al. Safety of antipsychotics for the treatment of schizophrenia: a focus on the adverse effects of clozapine. Therapeutic Advances in Drug Safety. 2018;9(5):237–56.
- Ravikrishna V, Krishnaveni J. Development and evaluation of clozapine intranasal mucoadhesive in situ gels for brain targeting. Journal of Drug Delivery and Therapeutics. 2019;9(2-s):198–207.
- Iqbal E, Govind R, Romero A, Dzahini O, Broadbent M, Stewart R, et al. The side effect profile of Clozapine in real world data of three large mental health hospitals. De Luca V, editor. PLOS ONE. 2020 Dec 8;15(12):e0243437.
- Albitar O, Harun SN, Zainal H, Ibrahim B, Sheikh Ghadzi SM. Population Pharmacokinetics of Clozapine: A Systematic Review. BioMed Research International. 2020;1–11.
- Maleki Dizaj S. Preparation and study of vitamin A palmitate microemulsion drug delivery system and investigation of co-surfactant effect. Journal of Nanostructure in Chemistry. 2013;3(1).
- Mehta SK, Kaur G, Bhasin KK. Analysis of Tween based microemulsion in the presence of TB drug rifampicin. Colloids and Surfaces B: Biointerfaces. 2007;60(1):95–104.
- Patel N, Baldaniya M, Raval M, Sheth N. Formulation and Development of In Situ Nasal Gelling Systems for Quetiapine Fumarate-Loaded Mucoadhesive Microemulsion. Journal of Pharmaceutical Innovation. 2015;10(4):357–73.
- Hashem FM, Shaker DS, Ghorab MK, Nasr M, Ismail A. Formulation, Characterization, and Clinical Evaluation of Microemulsion Containing Clotrimazole for Topical Delivery. AAPS PharmSciTech. 2011;12(3):879–86.
- Abdulla NA, Balata GF, El-ghamry HA, Gomaa E. Intranasal delivery of Clozapine using nanoemulsion-based in-situ gels: An approach for bioavailability enhancement. Saudi Pharmaceutical Journal. 2021;29(12):1466–85.
- Halde BR, Darekar AB, Saudagar RB. Design Development and Evaluation of Agomelatine Microemulsion for Intranasal Delivery. Journal of Drug Delivery and Therapeutics. 2019 Feb 15;9(1-s):132–8.
- Wen MM, Ismail NIK, Nasra MMA, El-Kamel AH. Repurposing ibuprofen-loaded microemulsion for the management of Alzheimer’s disease: evidence of potential intranasal brain targeting. Drug Delivery. 2021 Jan 1;28(1):1188–203.
- Kajbafvala A, Salabat A, Salimi A. Formulation, characterization, and in vitro/ex vivo evaluation of quercetin-loaded microemulsion for topical application. Pharmaceutical Development and Technology. 2016 Dec 9;23(8):741–50.
- Fawaz W, Hasian J, Alghoraibi I. Preparation, Characterization, and Release Profile Study of Vincristine Sulfate-loaded Polycaprolactone Nanoparticles. Micro and Nanosystems. 2023 Dec;15(4):300–7.
- Yousfan A, Rubio N, Natouf AH, Daher A, Al-Kafry N, Venner K, et al. Preparation and characterisation of PHT-loaded chitosan lecithin nanoparticles for intranasal drug delivery to the brain. RSC Advances. 2020;10(48):28992–9009.
- Ramreddy S, Janapareddi K. Brain targeting of chitosan-based diazepam mucoadhesive microemulsions via nasal route: formulation optimization, characterization, pharmacokinetic and pharmacodynamic evaluation. Drug Development and Industrial Pharmacy. 2018 Oct 24;45(1):147–58.
- Devanand A, Shinde M, Student, Bamu. Preparation and Evaluation of Microemulsion Containing Antihypertensive Drug. International Journal of Current Science. 2022;12(1):2250–1770.
- States U. The United States Pharmacopeia 2021: USP 44; The national formulary: NF 39. Rockville,Md United States Pharmacopeial Convention Copyright © The United States Pharmacopeial Convention, 1 Twinbrook Parkway, Rockville, Md 2; 2021.
- Ngawhirunpat T, Worachun N, Opanasopit P, Rojanarata T, Panomsuk S. Cremophor RH40-PEG 400 microemulsions as transdermal drug delivery carrier for ketoprofen. Pharmaceutical Development and Technology. 2011 Oct 24;18(4):798–803.
- JP, B. DA, B. SR. A Recent Review on Nasal Microemulsion for Treatment of CNS Disorder. International Journal of Current Pharmaceutical Research. 2017;9(4):5.
- Jain P, Soni R, Paswan Sk, Soni Pk. Ketoconazole Laden Microemulsion Based Gel Formulation Against Skin Fungal Infection. International Journal of Applied Pharmaceutics. 2023 May 7;15(3):49–60.
- Tan MSA, Pandey P, Falconer JR, Siskind DJ, Balmanno A, Parekh HS. Clozapine-Encapsulated Binary Mixed Micelles in Thermosensitive Sol–Gels for Intranasal Administration. Gels. 2022 Jan 5;8(1):38.
- Kota RB, Kaliyaperumal S. Superporous Hydrogels as Super Disintegrants in Formulating Oral Disintegrating Tablets of Clozapine for the Treatment of Schizophrenia. International Journal of Drug Delivery Technology. 2024 Sep 25;14(03):1716–21.