عوز الحديد لدى أطفال سوريين مصابين بأدواء قلب خلقيّة: علاقته بنوب الزرقة ونقص الوزن وفائدة مؤشرات الكريات الحمراء في التحري عنه
2025-08-23 | المجلد السابع العدد السادس - المجلد السابع | مقالات بحثيةرشا عبود الخليف | رنوه محمود السيّد
الملخص
خلفية البحث وهدفه: تمثل أمراض القلب الخلقية خللاً في بنية القلب منذ الولادة، تنقسم الى آفات يتغير فيها دوران الدم تسبب الزرقة وتدعى مزرقة وأخرى غير مزرقة، وتسبب العديد من تلك الآفات نقصاً في الأكسجة قد يسبب عوزاً بدوره في الحديد مما يؤدي الى تزايد في معدلات المراضة والوفيات المرتبطة بتلك الآفات. تهدف الدراسة إلى تقييم عوز الحديد لدى الأطفال السوريين المصابين بأدواء قلب خلقية وعلاقته بتكرار نوب الزرقة ونقص الوزن كما وتهدف أيضاً الى إمكانية الاستفادة من اختبارات التعداد الكامل للدم في التنبؤ بعوز الحديد.
مواد البحث وطرائقه: أُجريت دراسة حالة-شاهد شملت 100 طفل (30 في مجموعة الشواهد و35 مصابًا بأمراض قلب خلقية غير مزرقة و35 مصابًا بأمراض قلب خلقية مزرقة). شملت معايير الإشتمال الأطفال المشخصين بأفات غير مزرقة مثل الفتحة بين البطينين أو الأذينين، والمصابين برباعي فالو أو تبادل منشأ الأوعية الكبيرة، والذين تم تشخيصهم باستخدام الإيكو ثنائي الأبعاد. تم استبعاد الأطفال الذين خضعوا لجراحة، أو تلقوا مكملات الحديد، أو لديهم أمراض دموية أو انتانات.
تم جمع العينات في مستشفى الأطفال الجامعي ومستشفى جراحة القلب بدمشق بعد الحصول على موافقة أولياء الأمور. تم إجراء الفحوصات التالية: التعداد الكامل للدم، الحديد، السعة الرابطة للحديد غير المشبعة، الفيريتين. أُجريت الدراسة الإحصائية باستخدام برنامج SPSS الإصدار 16 مع استخدام اختبارات مختلفة لتحديد الفروقات والعلاقات الإحصائية، واعتُبرت قيمة P<0.05 ذات دلالة إحصائية.
النتائج: أظهرت النتائج أن المرضى في كلا مجموعتي الدراسة (المصابين بآفات مزرقة وغير مزرقة) سجلوا انخفاضًا ذا دلالة إحصائية في مستويات الفيريتين مقارنة بالمجموعة الشاهدة (P=<0.001,P=0.042) على التوالي، مما يعكس تراجعًا حادًا في مستوى الحديد المخزون لديهم. كان الفارق واضحًا في مستويات الحديد في الدم بين مرضى الآفات المزرقة ومرضى الآفات غير المزرقة (P=0.028)، وكذلك بينهم وبين الشواهد (P=<0.001)، بينما لم يكن ذا دلالة إحصائية بين مرضى الآفات غير المزرقة والشواهد (P=0.053). وكان انتشار عوز الحديد لدى الأطفال المرضى أعلى منه لدى الأطفال الشواهد، وكان هذا الفرق ذا دلالة إحصائية (P=0.002)، حيث بلغت النسبة الأعلى لدى المجموعة المزرقة (60%). وُجد أيضًا ارتباط إيجابي متوسط بين عوز الحديد وزيادة نوب الزرقة (قيمة معامل الارتباط فاي=0.386)، حيث ارتفعت احتمالية حدوثها بمعدل 6.6 مرات لدى الأطفال الذين يعانون من عوز الحديد (P=0.02). وكان هناك ارتباط بين عوز الحديد ونقص الوزن لدى الأطفال المصابين بأدواء قلب خلقية مزرقة (P=0.022). أظهرت نتائج تحليل الانحدار اللوجستي أن كلاً من عرض توزيع كريات الدم الحمراء ومؤشر مينتزر يمثلان مؤشرين تنبؤيين جيدين لعوز الحديد لدى الأطفال المصابين بآفات مزرقة .
الاستنتاجات: تشير الدراسة الى أن الأطفال المصابين بأدواء قلب خلقية، ولا سيما في الحالات المزرقة، أكثر عرضة للإصابة بعوز الحديد، والذي يرتبط بزيادة تواتر نوب الزرقة، نقص الوزن وتفاقم المراضة. وأظهرت مؤشرات مثل عرض توزيع كريات الدم الحمراء ومؤشر مينتزر قدرة على التنبؤ بعوز الحديد لديهم.
كلمات مفتاحية : أدواء القلب الخلقية ، نوب الزرقة، عوز الحديد، الفيريتين، عرض توزيع كريات الدم الحمراء، مؤشر مينتزر، نقص الوزن , Congenital heart disease, Cyanotic spells, Iron deficiency, Ferritin, Red cell distribution width (RDW), Mentzer index, Weight loss
المقدمة Introduction
تُعرَّف أدواء القلب الخلقية بأنها خلل في هيكل أو وظيفة القلب والدورة الدموية منذ الولادة، سواء ظهرت أعراضها فورًا في مرحلة الطفولة أو بقيت غير عرضية [1].
تُشكّل أدواء القلب الخلقية حوالي ثلث التشوهات الخلقية عالميًا، حيث يُقدّر حدوثها بمعدل 8 إصابات بين كل 1000 ولادة.[2] ترتبط هذه الآفات بمعدلات مرتفعة من المراضة والوفيات، إذ تُعدّ السبب الثاني لوفيات الرضّع بعد الأمراض المعدية [3].
تطرح أدواء القلب الخلقية عامة(فتحة ما بين البطينين، فتحة ما بين الأذينتين، رباعي فالو، تبادل منشأ الأوعية الكبيرة)، والآفات المُزرّقة منها خاصة (رباعي فالو، تبادل منشأ الأوعية الكبيرة)، تحديات صحية متعددة اذ تترافق هذه العيوب مع نقص في اشباع الاكسجين في الدم الشرياني، مما يُحفّز زيادة إنتاج الإريثروبويتين، الذي يؤدي بدوره إلى زيادة كتلة كريات الدم الحمراء كمحاولة لتعويض نقص الأكسجين [4].
الا أن هذا التكيف غالباً ما يؤدي الى نقص في الحديد [5].وأيضاً الى ظهور أعراض فرط اللزوجة، مثل: الصداع، الدوار، حوادث الأوعية الدموية الدماغية، وتشوه كريات الدم الحمراء، مما يؤدي إلى تكون تجمعات خلوية قد تسبب انسداد الأوعية الدموية. كما تكون تلك الكريات أقل نفوذية وأكثر تصلباً لدى الأطفال الذين يعانون من فقر الدم الناجم عن عوز الحديد وبالتالي أكثر تسبباً باحداث الصمّات. [6,7]
وعموماً تزداد المراضة لدى الأطفال المصابين بأدواء قلب خلقية ناقصي الحديد متمثلة ب: فقدان الشهية، انخفاض الحيوية، الهيوجية، بطء في زيادة الوزن، وتأخر في النمو الروحي الحركي وكذلك نوب الزرقة لدى الأطفال ممن لديهم آفة من النمط المزرّق، وبالتالي ارتفاع معدلات الوفيات بين الأطفال المصابين بتلك الآفات.]8،9[ إضافة إلى ذلك، قد يخفي تركيز الهيموغلوبين الطبيعي لدى هؤلاء الأطفال عوز الحديد.]11،10[
واذا اضفنا الى كل ما سبق كون عوز الحديد هو العوز التغذوي الأكثر انتشاراً على مستوى العالم وفقاً لمنظمة الصحة العالمية ]12[ سيكون كل من كشف ومعالجة عوز الحديد ضرورة ملحة لرعاية هؤلاء الأطفال وتخفيف المراضة قبل الجراحة التي قد تتأخر وأيضاً خلال العمل الجراحي والرعاية التالية له. انطلاقًا مما سبق، هدفت الدراسة إلى تقييم حالة الحديد لدى الأطفال السوريين المصابين بمختلف أنماط أدواء القلب الخلقية مقارنةً بالمجموعة الشاهدة، وفيما بين مجموعتي الآفات غير المُزرّقة والمُزرّقة، ودراسة انتشار عوز الحديد لدى هؤلاء الأطفال بالإضافة إلى دراسة العلاقة بين عوز الحديد وتواتر نوب الزرقة ونقص الوزن، وقدرة اختبارات التعداد الكامل للدم المجراة روتينياً على التنبؤ بعوز الحديد.
المواد والطرائق Materials and Methods
نمط الدراسة وجمع العينات:
اشتملت هذه الدراسة التي هي من نمط حالة-شاهد case-control study على 65 طفلاً سورياً، 30 منهم شواهد و35 منهم مصابين بأدواء قلب خلقية غير مزرقة توزعوا بين 11 مريض مصابين بفتحة ما بين الأذينتين و 24 مريض مصابين بفتحة ما بين البطينين و35 منهم مصابين بأدواء قلب خلقية مزرقة توزعوا بين 18 مريض مصابين بداء رباعي فالو و 17 مريض مصابين بداء تبادل منشأ الأوعية الكبيرة.
تضمنت معايير الاشتمال بالنسبة للمجموعة المرضية أطفال مشخصين بأدواء القلب الخلقيّة المزرّقة (رباعي فالو، تبادل منشأ الأوعية الكبيرة) أو أدواء القلب الخلقية غير المزرّقة (فتحة ما بين الأذينتين، فتحة ما بين البطينين) بواسطة ايكو ثنائي الأبعاد، وبالنسبة لمجموعة الشواهد اشتملت أطفال أصحّاء ليس لديهم أعراض أو علامات تشير الى المرض.
تضمنت معايير الاستبعاد الأطفال الذين خضعوا لجراحة مؤخراً، الأطفال الذين تلقوا مكملات الحديد في الأشهر الستة الأخيرة، الأطفال الذين خضعوا لعملية تبديل جزئي للدم، نقل دم، والفصد المتكرر في الأشهر الستة الأخيرة، الأطفال المشخصون بفقر دم وراثي أو لأسباب أخرى، الأطفال المصابون بانتانات.
تمت عملية الاعتيان في كل من مستشفى الأطفال الجامعي ومستشفى جراحة القلب في دمشق.
بعد الحصول على الموافقة المستنيرة من قبل أولياء الأطفال، تم جمع دم وريدي على أنابيب حاوية على مضاد تخثر EDTA ومن ثم تم اجراء اختبار تعداد الدم الكامل على جهاز التعداد في مخبر الدمويات في مستشفى الأطفال الجامعي في دمشق في حالة عدم توفر النتيجة في ملفات المرضى.
كما تم جمع دم وريدي على أنابيب سحب دم جاف ومن ثم تم تثفيلها في المثفلة الموجودة في مخبر مستشفى الأطفال الجامعي والحصول على المصل الذي تم جمعه في أنابيب ابندورف وحفظه بدرجة حرارة -20 درجة مئوية في مجمدة مخبر مستشفى الأطفال الجامعي ليتم إجراء بقية الاختبارات عليه. تم الحصول على بيانات المرضى ومعدل حدوث نوبات الزرقة لديهم من خلال متابعة ملفاتهم وإجراء مقابلة مع الأهالي.
تم اجراء مقايسة الحديد (معايرة لونية) في المصل باستخدام Iron FS Ferene KIT لشركة BioMajesty في مستشفى الأطفال الجامعي. تم اجراء مقايسة السعة الرابطة للحديد غير المشبعة UIBC(unsaturated iron-binding capacity) ،وهي تمثل الجزء من السعة الذي لم يرتبط به الحديد في المصل، (معايرة لونية) في المصل باستخدام UIBC FS KIT لشركة Biomajesty في مستشفى الأطفال الجامعي وتم حساب قيمة TIBC بوساطة المعادلة التالية :
TIBC= FE+UIBC
وتم حساب نسبة اشباع الترانسفرين بوساطة المعادلة التالية:
TSAT%=(FE/TIBC)*100
وتم حساب Mentezer Index من خلال المعادلة التالية:
Mentezer Index= MCV/RBC
تم اجراء مقايسة الفيريتين(طريقة اللمعان الكيميائي المناعي CLIA sandwich) في المصل باستخدام Ferritin CLIA KIT لشركة Mindray على جهاز CL-1000 في مخبر الفاهوم وكنامة في دمشق. تم تحديد وجود عوز الحديد لدى الأطفال المشمولين في الدراسة استنادًا إلى تركيز فيريتين المصل، وِفقًا للمعايير التالية: يُعد الطفل مصابًا بعوز الحديد إذا كانت مستويات فيريتين المصل أقل من 12 نانوغرام/مل لدى الأطفال بعمر ≤ 5 سنوات، وأقل من 15 نانوغرام/مل لدى الأطفال بعمر أكبرمن 5 سنوات. في المقابل، يُعد الطفل غير مصاب بعوز الحديد إذا تجاوزت مستويات الفيريتين هذه القيم، بحسب الفئة العمرية.]13،14[
بالنسبة لكل من حديد المصل والسعة الكلية الرابطة للحديد TIBC تم اعتماد القيم المرجعية للكيت الذي تم استخدامه (المجالات المرجعية لحديد المصل: 28-135 مكغ/دل للأطفال الذين تقل أعمارهم عن 6 أشهر، 35-155 مكغ/دل للأطفال الذين تتراوح أعمارهم بين 6 و 24 شهر، 22-135 مكغ/دل للأطفال الذين تتراوح أعمارهم بين 2 و 12 سنة، المجالات المرجعية للسعة الكلية الرابطة للحديد TIBC: 120-450 مكغ/دل).
أما بالنسبة لاختبارات التعداد الكامل للدم فقد تم استخدام القيم المرجعية المعتمدة في مستشفى الأطفال الجامعي في دمشق (HGB:11.5-16.5g/dl، 35-55%HCT:، MCV:75-100 fl، MCH:25-35 pg، MCHC:31-38 g/dl، RDW:11-16%) تم تقييم الوزن للأطفال اعتماداً على معايير منظمة الصحة العالمية لنمو الأطفال، والتي تستند الى مؤشرات الوزن بالنسبة للعمر]15[.
الدراسة الإحصائية:
تم استخدام برنامج SPSS الإصدار 16 لانجاز كامل الدراسة الإحصائية، واعتبرت قيمة P<0.05 قيمة يُعتَد بها احصائياً.
النتائج Results
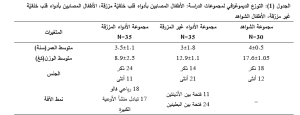
ظهرت لدينا فروق ذات دلالة إحصائية بين مجموعة الأطفال المصابين بأدواء قلب خلقيّة مزرّقة والأطفال المصابين بأدواء قلب خلقيّة غير مزرّقة وذلك تبعاً لجميع المتغيرات ما عدا MCV،HGB (الجدول 2)، وكذلك بين الأطفال المصابين بأدواء قلب خلقيّة مزرّقة والأطفال الشواهد تبعاً لجميع المتغيرات ما عدا MCV (الجدول3).
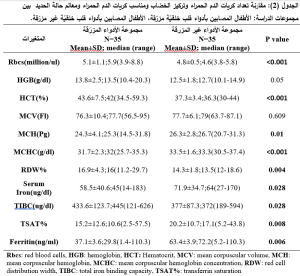
تم استخدام الاختبارات الإحصائية التالية: Shapiro-Wilk test: لتحري نمط توزع القيم بين المجموعات المختلفة، T test: لمقارنة القيم التي تتبع التوزع الطبيعي بين المجموعتين، Mann-Whitney u test: لمقارنة القيم التي تتبع التوزع الغير طبيعي بين المجموعتين. واعتبرت قيمة P<0.05 قيمة يُعتَد بها احصائياً.
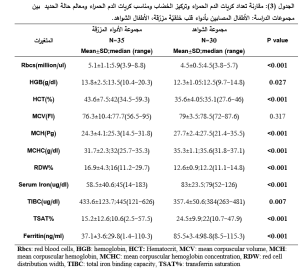
تم استخدام الاختبارات الإحصائية التالية: Shapiro-Wilk test: لتحري نمط توزع القيم بين المجموعات المختلفة، T test: لمقارنة القيم التي تتبع التوزع الطبيعي بين المجموعتين، Mann-Whitney u test: لمقارنة القيم التي تتبع التوزع الغير طبيعي بين المجموعتين. واعتبرت قيمة P<0.05 قيمة يُعتَد بها احصائياً.
كما ظهرت لدينا فروق ذات دلالة إحصائية بين مجموعة الأطفال المصابين بأدواء قلب خلقيّة غير مزرّقة ومجموعة الشواهد وذلك تبعاً لكل من HCT,MCHC,RDW والفيريتين فقط (الجدول 4)
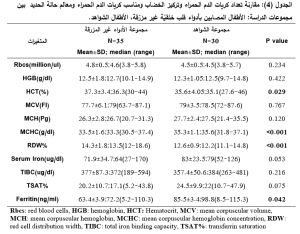
تم استخدام الاختبارات الإحصائية التالية: Shapiro-Wilk test: لتحري نمط توزع القيم بين المجموعات المختلفة، T test: لمقارنة القيم التي تتبع التوزع الطبيعي بين المجموعتين، Mann-Whitney u test: لمقارنة القيم التي تتبع التوزع الغير طبيعي بين المجموعتين. واعتبرت قيمة P<0.05 قيمة يُعتَد بها احصائياً.
كان انتشار عوز الحديد لدى الأطفال المرضى أعلى منه لدى الأطفال الشواهد وكان هذا الفرق ذا دلالة إحصائية حيث كانت نسبة الانتشار الأعلى لدى الأطفال المصابين بأدواء قلب خلقيّة مزرّقة (الجدول 5).
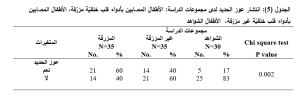
وجود عوز الحديد: مستويات فيريتين المصل أقل من 12 ng/ml للأطفال الذين أعمارهم أقل أو تساوي 5 سنوات، مستويات فيريتين المصل أقل من 15 ng/ml للأطفال الذين أعمارهم أكبر من 5 سنوات، غياب عوز الحديد: مستويات فيريتين المصل أكبر من 12 ng/ml للأطفال الذين أعمارهم أقل أو تساوي 5 سنوات، مستويات فيريتين المصل أكبر من 15 ng/ml للأطفال الذين أعمارهم أكبر من 5 سنوات. تم استخدام اختبار كاي التربيعي واعتبرت قيمة P<0.05 قيمة يُعتَد بها احصائياً.
وعند المقارنة بين الأطفال المصابين بعوز الحديد ضمن مجموعات الدراسة، ظهرت لدينا فروق إحصائية بينهم تبعاً لكل من المتغيرات HGB,TIBC,RDW فقط (الجدول 6).
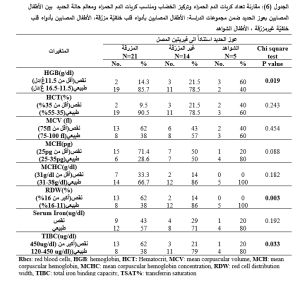
المجالات المرجعية لحديد المصل(تبعاً للكيت الذي تم استخدامه): 28-135 مكغ/دل للأطفال الذين تقل أعمارهم عن 6 أشهر، 35-155 مكغ/دل للأطفال الذين تتراوح أعمارهم بين 6 و 24 شهر، 22-135 مكغ/دل للأطفال الذين تتراوح أعمارهم بين 2 و 12 سنة.
تم استخدام اختبار كاي التربيعي واعتبرت قيمة P<0.05 قيمة يُعتَد بها احصائياً.
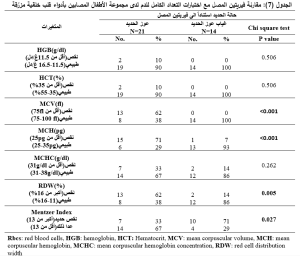
ولتقييم مدى قدرة اختبارات التعداد الكامل للدم على التنبؤ بعوز الحديد، قمنا بمقارنة حالة الحديد بناءً على اختبارات التعداد الكامل للدم مع حالة الحديد استناداً الى فيريتين المصل باستخدام اختبار كاي التربيعي، فأظهرت لدينا MCV,MCH,RDW,Mentzer Index دلالة إحصائية في مجموعة الأطفال المصابين بأدواء قلب خلقية مزرقة (الجدول 7)، وكل من MCV,MCH في مجموعة الأطفال المصابين بأدواء قلب خلقية غير مزرقة (الجدول 8). ولتحديد المؤشر المستقل القادر على التنبؤ بعوز الحديد قمنا باجراء اختبار الانحدار اللوجستي ، فمن بين كل الاختبارات التي أظهرت دلالة إحصائية (في اختبار كاي التربيعي)، كان فقط RDW,Mentzer Index مؤشرين مستقلين تنبؤيين لعوز الحديد وذلك في مجموعة الأطفال المصابين بأدواء قلب خلقية مزرقة (الجدول9,10 ).
تم استخدام اختبار كاي التربيعي واعتبرت قيمة P<0.05 قيمة يُعتَد بها احصائياً.
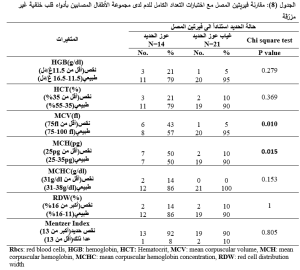
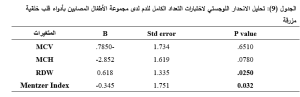
تم استخدام اختبار الانحدار اللوجستي الثنائي واعتبرت قيمة P<0.05 قيمة يُعتَد بها احصائياً.
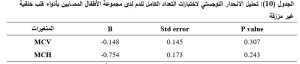
تم استخدام اختبار الانحدار اللوجستي واعتبرت قيمة P<0.05 قيمة يُعتَد بها احصائياً.
كان لدى 21 طفل من الأطفال المصابين بأدواء قلب خلقيّة مزرّقة عوز حديد (60%) في حين لم يكن لدى 14 منهم عوز حديد (40%). وقد سجلت نوب زرقة متكررة لدى 13 منهم (37.14). وجدت علاقة يعتد بها احصائياً بين عوز الحديد وتكرار نوب الزرقة (P=0.02). حيث كان انتشار نوب الزرقة في مجموعة الأطفال ذوي عوز الحديد (31.4%) أعلى منه في مجموعة الأطفال غير المصابين بعوز الحديد (5.7%). وبلغت نسبة الأرجحية 6.6 وقيمة معامل الارتباط فاي0.386 مما يشير الى وجود علاقة إيجابية طردية متوسطة بين هذين المتغيرين(الجدول 11).
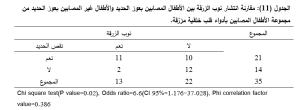
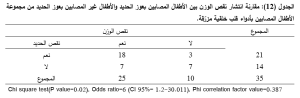
وجدت علاقة يعتد بها احصائياً بين عوز الحديد ونقص الوزن (P=0.022). حيث كان انتشار نقص الوزن في مجموعة الأطفال ذوي عوز الحديد (51.4%) أعلى منه في مجموعة الأطفال غير المصابين بعوز الحديد (20%) . وبلغت نسبة الأرجحية 6 وقيمة معامل الارتباط فاي0.387 مما يشير الى وجود علاقة إيجابية طردية متوسطة بين هذين المتغيرين(الجدول 12).
تم تقييم الوزن للأطفال اعتماداً على معايير منظمة الصحة العالمية لنمو الأطفال، والتي تستند الى مؤشرات الوزن بالنسبة للعمر[15].
المناقشة Discussion
أبدى المرضى في كلتا مجموعتي الدراسة من آفات مزرقة وغير مزرقة انخفاضاً ذا دلالة إحصائية في مستويات الفيريتين بالمقارنة مع المجموعة الشاهدة من الأطفال مما يشير الى استنفاد مخزون الحديد لديهم، لكنه كان اكثر انخفاضاً لدى مجموعة الآفات المزرقة. وقد دعمت هذه النتيجة عدة دراسات سابقة أشارت إلى انخفاض الفيريتين لدى مرضى الآفات المزرقة ]8،16،17،21[ ، كما لوحظ فرق واضح في مستويات الحديد المصلية بين مرضى الآفات المزرقة ومرضى الآفات غير المزرّقة وقد يعود ذلك جزئياً على الأقل لتأثير الآفة على تغذية الطفل من جهة ولتعرضه المتكرر للإنتانات من جهة أخرى وهو ما أشار اليه أيضا Binh T et al [19] . كذلك أظهرت المقارنة بين المرضى والشواهد في مجموعة الأفات المزرقة تحديداً وجود فرق واضح في مستويات الحديد، بما يتوافق مع نتائج دراسات أخرى أظهرت نقص مستويات الحديد المصلية لدى هذه الفئة من المرضى [8, 17، 20, 21].
كما كان عوز الحديد )تبعاً لمستويات الفيريتين( أكثر انتشاراً لدى الأطفال المصابين بأدواء قلب خلقيّة مزرّقة حيث بلغ معدل الانتشار 60% وكان هذا الفرق ذا دلالة إحصائية. تتوافق هذه النتيجة مع ما ورد في دراسات سابقة أجراها Mir A et al[8] ومع دراسة أجراها Soni S et al[16] ومع دراسة أجراها Mukherjee M et al[17] والتي سجلت معدلات انتشار لعوز الحديد 47.5%،46%،47.06% على التوالي. ومن الملفت أن معدل انتشار العوز في دراستنا كان أعلى من المعدلات الملاحظة في دراسات أجريت على البالغين المصابين بآفات قلب خلقية]18[. مما يعزز الفرضية بأن الفئة العمرية الأصغر، خصوصاً الرضع والأطفال الصغار، تكون أكثر عرضة للإصابة بعوز الحديد الغذائي. ومن ناحية أخرى، تشير دراستنا الى أن السعة الكلية للارتباط بالحديد TIBC لم تكن منخفضة كما هو الحال في حالات نقص الحديد الناتج عن سوء التغذية فقط، مما يدعم كون عوز الحديد لدى الأطفال المصابين بأدواء قلب خلقية مزرقة يعود الى آليات مرضية مرافقة لأمراض القلب الخلقية وليس فقط لنقص المدخول الغذائي.
إن نمط الآفة القلبية يعد مساهماً أساسياً في تطور عوز الحديد لدى الأطفال المصابين بأمراض قلب خلقية وخصوصاً في الحالات المزرقة، فبالإضافة لنقص أكسجة النسج التي تحفز إفراز الإيريتروبيوتين يتعرض الأطفال المرضى للإنتانات التي تسهم أيضاً في انخفاض نسب الحديد المصلية بآلية فيزيولوجية من جهة وبما تسببه من جهة أخرى هي والإصابة الأولية من نقص في الشهية واضطراب في التغذية لديهم وبالتالي يمكننا تفسير ازدياد انتشار عوز الحديد عند الأطفال المصابين بآفة مزرقة بتضافر تأثير العوامل السابقة.
إن الترافق الملحوظ لعوز الحديد والاختطار المرتفع لتكرار نوب الزرقة لدى الأطفال المصابين بآفات كرباعي فالو وتبادل منشأ الأوعية يبين وجود عامل اختطار يمكن تعديله والتقليل من حصول الاختلاطات الخطيرة والمميتة لدى هؤلاء الأطفال. وقد تضمنت بعض المرشدات العلاجية الخاصة بمرضى رباعي فالو ادراج مكملات الحديد الفموية ]22[.
من جانب آخر سيساهم عوز الحديد في نقص النمو الملاحظ لدى مجمل الأطفال المرضى، و هذا النقص في الأعوام الأولى للحياة سيكون من الصعب تجاوزه لاحقاً.
كما يشكل الحديد عاملاً مساعداً أساسياً للعديد من الأنزيمات الميتوكوندرية وبالتالي فإن نقصه قد يسهم في تفاقم بعض العيوب الميتوكوندرية التي تم وصفها لدى مجموعة متنوعة من المرضى بمن فيهم مرضى آفات القلب الخلقية. وتشير بعض الدراسات الى احتمالية وجود علاقة بين عوز الحديد وحدوث هذه الاضطرابات على مستوى الميتوكوندريا]23[ مما يجعله عامل اختطار إضافي يجب الانتباه اليه.
إضافة لما سبق وجدنا ازدياداً ذا دلالة إحصائية في تواتر نوب الزرقة لدى الأطفال المصابين بأدواء قلب خلقيّة مزرّقة ممن لديهم عوز حديد مقارنةً بالأطفال غير المصابين بعوز الحديد من نفس المجموعة، وقد يكون ذلك عائداً لتراجع وظيفة الهيموغلوبين، توافقنا في ذلك مع دراسة Mukherjee M et al[17] ومع دراسة Rahman M et al[24]. كما وجدنا أيضاً لديهم انتشاراً لنقص الوزن ذا دلالة إحصائية.وذلك نتيجة نقص الأكسجة المزمن وتراجع القدرة على نقل الأكسجين. توافقنا في ذلك مع دراسة Rahman M et al[24] ومع Mir A et al[8].
ومن جهة أخرى، فيما يتعلق بقدرة اختبارات CBC المجراة روتينياً على التنبؤ بتطور عوز الحديد، وجدنا ارتفاعاً في تعداد كريات الدم الحمراء ومستويات الهيموغلوبين ونسبة الهيماتوكريت لدى الأطفال المصابين بأدواء قلب خلقيّة مزرّقة مقارنةً بالأطفال الشواهد وكان هذا الفرق ذا دلالة إحصائية. قد يعزى ذلك إلى أن نقص الأكسجة لدى هؤلاء المرضى يسبب زيادة في انتاج الاريثروبيوتين مما يحفز نقي العظم ويؤدي الى زيادة في تعداد كريات الدم الحمراء]25[.قد يقنع هذا التكيّف الفيزيولوجي لنقص الأكسجة حالة عوز الحديد، مما يساهم بارتفاع المراضة والوفيات ما لم يُشخّص ويُعالج بالشكل الملائم .توافقت دراستنا مع دراسة أجراها Soni S et al[16] ومع دراسة أجراها Mir A et al[8].
كانت مستويات MCV منخفضة لدى الأطفال المصابين بأدواء قلب خلقيّة ، سواء المزرّقة أو غير المزرّقة مقارنةً بالأطفال الشواهد. إلا أن هذا الفرق لم يكن ذا دلالة إحصائية. قد يعزى هذا الى تشتت احجام الخلايا المعبّر عنه بارتفاع RDW لدى هؤلاء الأطفال . لم تتوافق دراستنا بهذا الشأن مع دراستي Soni S et al[16] وMir A et al[8].
وعند إجراء اختبار الانحدار اللوجستي لتحديد المتغيرات المستقلة التي يمكنها التنبؤ بعوز الحديد، تبين أن MCV كمؤشر فردي لم يكن كافياً لهذا الغرض، قد يعود ذلك الى تأثر MCV بعوامل أخرى وعدم تغيره بشكل ملحوظ في بعض حالات عوز الحديد المبكر أو المعتدل، بالإضافة الى تقارب قيمه بين المرضى مما يحد من القدرة الإحصائية على كشف الفرق.
بالمقابل أظهرMentzer Index فرقاً ذا دلالة إحصائية بين ناقصي الحديد وغير ناقصي الحديد في مجموعة الأطفال المصابين بأدواء قلب خلقيّة مزرّقة . حيث أنه لدى هؤلاء الأطفال تؤدي الاستجابة لنقص الاكسجة الى ارتفاع تعداد كريات الدم الحمراء، مما يؤدي الى انخفاض قيمة مؤشر مينتزر الى ما دون 13 رغم وجود حالة عوز حديد. لذلك فإن انخفاض قيمته في هذه المجموعة لا يشير الى وجود تلاسيميا، بل يعكس تأثير نقص الاكسجة لديهم على تعداد الكريات. كما أظهر قدرة تنبؤية بعوز الحديد لديهم مما يدعم استخدامه كؤشر مساعد في هذه الفئة المرضية.
كما لاحظنا أن مستويات RDW كانت مرتفعة لدى الأطفال المصابين بأدواء قلب خلقيّة، سواء المزرّقة أوغير المزرّقة، مقارنةً بالأطفال الشواهد وكانت هذه الفروق ذات دلالة إحصائية. وتدعم هذه النتيجة ما ورد في دراسة Mir A et al[8].
وفي دراسة أجراها Miyamoto et alلاستكشاف العلاقة بين RDW والوفيات المرتبطة بأمراض القلب والأوعية الدموية، تم تقييم الروابط بين فقر الدم، الإنترلوكين-6 (IL-6)، و RDW لدى مرضى يعانون من أمراض القلب الخلقية غير المزرقة خلصت الدراسة إلى أن RDWعلى الرغم من كونه اختبارًا سريريًا بسيطًا وغير مكلف، يمثل مؤشرًا لسوء إنذار أمراض القلب والأوعية الدموية. ]26[
ويُعد الفيريتين المخزون الأساسي للحديد في الجسم، ونقصه يُمثل المرحلة الأولى من استنزاف الحديد قبل أن ينخفض مستوى الحديد في المصل. عندما يبدأ الفيريتين بالانخفاض، لا يتأثر حجم كريات الدم الحمراء فورًا، ولكن مع مرور الوقت، تبدأ الكريات الأحدث في التقلص نتيجة لنقص الحديد المتاح، مما يزيد من تباين الأحجام ويؤدي إلى ارتفاع RDW.بالتالي، يمكن لـ RDW أن يكون مؤشرًا على عوز الحديد]27[.
أظهرت دراستنا أيضاً أن RDW من المتغيرات المستقلة التي يمكنها التنبؤ بعوز الحديد لدى الأطفال المصابين بأدواء قلب خلقيّة مزرّقة فقط. يمكننا تفسير هذه النتيجة بأن مرضى الأدواء القلبية الخلقيّة المزرّقة يعانون من نقص أكسجة مزمن يؤدي الى تحفيز انتاج كريات الدم الحمراء الا أن هذا الإنتاج يكون غير فعال في حال تزامنه مع عوز الحديد إضافة لما قد يعانيه الأطفال من أعواز تغذوية أخرى، بينما لا تظهر الحالات غير المزرّقة نفس الدرجة من التحفيز المزمن لنقي العظم كما أن عوز الحديد لديهم أقل حدة كما بينت نتائجنا، ويتفق ذلك مع ما توصلت إليه دراسة Bandyopadhahy S et al[21].
من هنا يمكن اعتبار RDW مؤشراً داعماً مفيداً في التنبؤ بعوز الحديد خاصة في الحالات التي يصعب فيها اجراء تحاليل متقدمة.
الاستنتاجات Conclusions
بناءً على نتائج هذه الدراسة، يمكن الاستنتاج بأن الأطفال المصابين بأدواء قلب خلقيّة، لاسيما في الحالات المزرّقة، هم أكثر عرضة للإصابة بعوز الحديد، والذي يرتبط بدوره بزيادة تواتر نوب الزرقة، نقص الوزن واحتمال تفاقم المراضة. كما أظهرت الدراسة أن بعض المؤشرات الدموية مثل RDW وMentzer Index تساعد في التنبؤ بعوز الحديد لديهم.
التوصيات Recommendations
توصي الدراسة بضرورة التحري الدوري عن عوز الحديد لدى الأطفال المصابين بأمراض قلب خلقية عن طريق معايرة مستويات حديد المصل والفيريتين، إلى جانب دعم استخدام مؤشرات دموية بسيطة وغير مكلفة كـ RDW ومؤشر مينتزر لتوجيه القرار السريري خاصة في البيئات ذات الموارد المحدودة. كما يُنصح بإدراج مكملات الحديد في البروتوكولات العلاجية للمرضى ذوي الخطورة العالية، ومراقبة الحالة التغذوية لهؤلاء الأطفال بشكل دوري للحد من المضاعفات المحتملة وتحسين نوعية حياتهم ونموهم على المدى البعيد.
قائمة الاختصارات List of abbreviations
| الشرح باللغة الإنكليزية | الشرح باللغة العربية | اسم الاختصار |
| Complete blood count | التعداد الكامل للدم | CBC |
| Ethylenediaminetetraacetic acid | الايتيلين دي امين رباعي حمض الخل | EDTA |
| Unsaturated Iron Binding Capacity | السعة الرابطة للحديد غير المشبعة | UIBC |
| total iron binding capacity | السعة الكلية الرابطة للحديد | TIBC |
| transferrin saturation | نسبة اشباع الترانسفرين | TSAT% |
| Chemiluminescent Immunoassay | مقايسة باللمعان الكيميائي المناعي | CLIA |
| red blood cells | خلايا الدم الحمراء | RBCs |
| hemoglobin | الهيموغلوبين | HGB |
| Hematocrit | الهيماتوكريت | HCT |
| mean corpuscular volume | متوسط حجم خلايا الدم الحمراء | MCV |
| mean corpuscular hemoglobin | متوسط كمية الهيموغلوبين في خلايا الدم الحمراء | MCH |
| mean corpuscular hemoglobin Concentration | متوسط تركيز الهيموغلوبين في خلايا الدم الحمراء | MCHC |
| red cell distribution width | عرض توزيع الكريات الحمراء | RDW |
| Statistical Package for the Social Sciences | الحزمة الإحصائية للعلوم الاجتماعية | SPSS |
| Confidence Interval | مجالات الثقة | CI |
الموافقة الأخلاقيّة Ethics approval
حصلت هذه الدّراسة على موافقة مجلس أخلاقيّات الأبحاث الطّبيّة الحيويّة في جامعة دمشق بتاريخ 29\1\2202 برقم PH-290122-29.
تضارب المصالح Conflict of interests
يقر جميع الباحثين المشاركين في هذا البحث بعدم وجود تضارب في المصالح فيما بينهم.
التمويل Funding
لم يتلقَ المؤلفون أي منحة محددة من أي جهة تمويلية من أجل البحث أو من أجل النشر.
مساهمات المؤلفين Author’s contributions
صممت الدكتورة رنوه السيّد البحث وقامت رشا الخليف بجمع البيانات والعيّنات وإجراء التحاليل المخبرية والتحليل الإحصائي، وقام كلٌّ من الدكتورة السيّد والخليف بتفسير النتائج وكتابة وصياغة مخطوطة البحث، وقاما بقراءة المخطوطة النهائية والموافقة عليها.
المراجع :- haled E, Abd El Moneim M, Riad N, Saber M. Iron deficiency and behavioral disorders in children with cyanotic congenital heart disease. Saudi J Med. 2021;6(7):198-205.
- Bernier PL, Stefanescu A, Samoukovic G, Tchervenkov CI. The challenge of congenital heart disease worldwide: epidemiologic and demographic facts. Semin Thorac Cardiovasc Surg Pediatr Card Surg Annu. 2010;13:26-34.
- Feng Y, Cai J, Tong X, Chen R, Zhu Y, Xu B, et al. Non-inheritable risk factors during pregnancy for congenital heart defects in offspring: a matched case-control study. Int J Cardiol. 2018;264:45-52.
- Gidding SS, Stockman 3rd JA. Erythropoietin in cyanotic heart disease. Am Heart J. 1988;116(July (1 Pt 1)):128–132
- Tempe DK, Virmani S. Coagulation abnormalities in patients with cyanotic congenital heart disease. J Cardiothorac Vasc Anesth. 2002;16:752-65.
- Broberg CS, Bax BE, Okonko DO, et al. Blood viscosity and its relationship to iron deficiency, symptoms and exercise capacity in adults with cyanotic congenital heart disease. J Am Coll Cardiol. 2006;48:356-65.
- Yip R, Mohandas N, Clark MR, Jain S, Shohet SB, Dallman PR.Red cell membrane stiffness in iron deficiency. Blood. 1983;62:99–106
- Mir AB, Shah JA, Mushtaq S, Jan M. Prevalence, profile of malnutrition and iron deficiency anemia in children with cyanotic congenital heart defects: a case-control observational study in tertiary care hospital in North India. Int J Contemp Pediatr. 2019;6(3):1303-8.
- Carson JA, Duff A, Poses RM, et al. Effect of anemia and cardiovascular disease on surgical mortality and morbidity. Lancet. 1996;348:1055-60.
- Olcay L, Ozer S, Gurgey A, et al. Parameters of iron deficiency in children with cyanotic congenital heart disease. Pediatr Cardiol. 1996;17:150-4.
- Roodpeyma S, Movssavi F, Kamali Z. Red blood cell indices in cyanotic congenital heart disease. Med J Iran Hosp. 2002;4:24-6.
- de Benoist B, McLean E, Egli I, et al. Worldwide prevalence of anaemia 1993–2005: WHO global database on anaemia. World Health Organization; 2008. ISBN 9789241596657.
- Wang W, Knovich MA, Coffman LG, Torti FM, Torti SV.Serum ferritin: past, present and future. Biochim Biophys Acta.2010;1800:760–769.
- Stanley FL. Reference, intervals for laboratory tests andProcedures. In: Kliegman RM, Stanton BF, St Geme JW, SchorNF, eds. Nelson Textbook of Pediatrics 20th ed. New Delhi:Elsevier; 2016:3471–3472.
- World Health Organization. WHO child growth standards: Length/height-for-age, weight-for-age, weight-for-length, weight-for-height and body mass index-for-age: Methods and development. World Health Organization;2006. Available from: https://www.who.int/publications/i/item/924154693X
- Soni S, Chaudhary P, Arya S, Thora S. To assess iron deficiency anaemia in patients with cyanotic heart disease compared to general population. Int J Pediatr Res. 2018;5(5):268-72. doi:10.17511/ijpr.2018.i05.05.
- Mukherjee S, Sharma M, Devgan A, Jatana SK. Iron deficiency anemia in children with cyanotic congenital heart disease and effect on cyanotic spells. Med J Armed Forces India. 2018;74(3):235-40.
- Gaiha M, Sethi HP, Sudha R, Arora R, Acharya NR. A clinichematological study of iron deficiency anaemia and its correlation with hyperviscosity symptoms in cyanotic congenital heart disease. Indian Heart J. 1993;45(January– February (1)):53–55.
- Binh TQ, Suong NTB, Dinh NH, Anh VT, Thanh VT, Khoi LM. Iron deficiency anemia in children with congenital heart disease and the usefulness of erythrocyte indexes as a screening tool. Arch Gen Intern Med. 2018;2(3):1-4.
- Itiola AY, Animasahun BA, Njokanma OF. Serum iron status of children with cyanotic congenital heart disease in Lagos, Nigeria. SQU Med J. 2019;19(4):346-51.
- Bandyopadhyay S, Bhuvaneswari A, Sridhar A. A study of iron status in children with cyanotic congenital heart disease. Int J Contemp Pediatr. 2023;10:1383-90.
- Saxena A, Relan J, Agarwal R, Awasthy N, Azad S, Chakrabarty M, et al. Indian guidelines for indications and timing of intervention for common congenital heart diseases: Revised and updated consensus statement of the Working Group on Management of Congenital Heart Diseases. Annals of Pediatric Cardiology. 2019;33(3):1-33. doi:10.4103/apc.APC_32_19.
- Yan F, Li K, Xing W, Dong M, Yi M, Zhang H. Role of iron-related oxidative stress and mitochondrial dysfunction in cardiovascular diseases. Oxidative Medicine and Cellular Longevity. 2022;2022:5124553. doi:10.1155/2022/5124553.
- Rahman M, Dipti DI, Ahmed MY. Iron deficiency Anemia among Children with Congenital Heart Disease: A Cross-Sectional Study. Sch J App Med Sci. 2025 Apr;13(4):908-13.
- Onur CB, Sipahi T, Tavil B, Karademir S, Yoney A. Diagnosing iron deficiency in cyanotic heart disease. Indian J Pediatr. 2003;70(1):29-31.
- Miyamoto K, Inai K, Takeuchi D, et al. Relationships among red cell distribution width, anemia, and interleukin-6 in adult congenital heart disease. Circ J. 2015;79:1100-6.
- Narchi H, Kulaylat N. Red cell distribution width in the diagnosis of iron deficiency anemia. J Pediatr. 1999;135(4): 546-547.