التعدد الشكلي وحيد النوكليوتيد rs6166 C/T في جين مستقبل الهرمون المنبّه للجريب لدى جمهرة من السّوريات المصابات بمتلازمة المبيض متعدد الكيسات في دراسة حالة-شاهد
2025-08-23 | المجلد السابع العدد السادس - المجلد السابع | مقالات بحثيةزينه عبد الحميد أبو شامي | مروان جميل الحلبي | لمى علي يوسف
الملخص
خلفيّة البحث: تعدُّ متلازمة المبيض متعدد الكيسات اضطراباً صمّاويّاً شائعاً لدى الإناث في سنّ الإنجاب وذات سببية إمراضيّة متعددة العوامل الجينيّة والبيئيّة. تتّسم المتلازمة بمظهر مبيض متعدد الكيسات (≥20 جريب بقطر 2-9 ملم في كل مبيض)، وقلة الإباضة أو انعدامها، وحالة فرط أندروجينيّة تتظاهر بالشّعرانية، إضافةً إلى العدّ/حَبّ الشَّباب والمقاومة للإنسولين. تشمل التأثيرات طويلة الأمد للمتلازمة كلاً من العقم والأمراض القلبية الوعائية والبدانة والسكري من النمط الثاني. تُعد التّعددات الشّكليّة في الجين المرمّزة لمستقبل الهرمون المنبه للجريبFollicle-Stimulating Hormone Receptor (FSHR) مرشحة محتملة للارتباط بالاستعداد للمرض.
الهدف: هدفت دراستنا إلى تحرّي علاقة التعدد الشّكليّ مفرد النكليوتيد rs6166 C/T في جين مستقبل الهرمون المنبّه للجريب باختطار الإصابة بمتلازمة المبيض متعدد الكيسات.
تصميم الدّراسة والطّرائق: اتّبعت الدراسة تصميماً رصدياً من نمط حالة-شاهد، وشملت 38 مريضة مؤكّدة التّشخيص بمتلازمة المبيض متعدد الكيسات وفقاً لمعايير روتردام المُعدّلة و46 أنثى سليمة نفيت لديهنّ المتلازمة وفق المعايير ذاتها في المجموعة الشاهدة. أُجري التنميط الجيني للتعدد الشّكليّ rs6166 C/T بطريقة تفاعل البوليميراز التّسلسلي Polmerase Chain Reaction (PCR) متبوعًا بتحليل تعدد أطوال شدف التقييد Restriction Fragment Length Polymorphism(RFLP) بأنزيم BsrI وخضعت 5% من العيّنات لسلسلة سانجر وجاءت النّتائج مطابقة لنتائج RFLP.
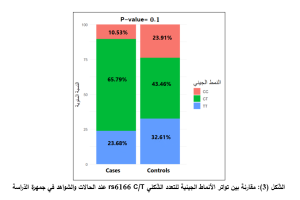
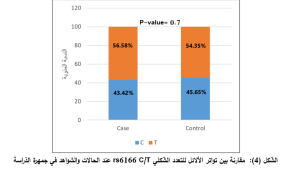
النّتائج: كانت تواترات الأليلين C وT للتعدد الشّكلي rs6166 C/T متماثلة بين المريضات والشّواهد (P= 0.7)، في حين تباينت تواترات الأنماط الجينيّة (CT وCC وTT) بين المجموعتين، حيث بلغت على التّرتيب 65.79 % و10.53% و23.68% في مجموعة الحالات مقابل 43.48% و23.91% و32.61% لدى مجموعة الشّواهد، لكن دون وجود فارق ذي دلالة إحصائيّة (P= 0.1).
الاستنتاجات: لا تدعم نتائج هذه الدراسة وجود ارتباط بين التعدد الشكليّ rs6166 C/T في جين مستقبل الهرمون المنبّه للجريب والإصابة بمتلازمة المبيض متعدد الكيسات في هذه المجموعة السكانية المدروسة.
كلمات مفتاحية : التّعدد الشّكلي وحيد النوكليوتيد، جين مستقبل الهرمون المنبّه للجريب، متلازمة المبيض متعدّد الكيسات، تفاعل البوليمراز التّسلسلي, Polycystic ovary syndrome, PCOS, FSHR, SNPs, Genotyping, PCOM, rs6165, rs6166
المقدمة Introduction
تُعَدّ متلازمةُ المبيض المتعدّد الكيسات (PCOS) Polycystic Ovary Syndrome حالةً هرمونيّةً شائعةً تصيبُ النّساء في سنّ الإنجاب بنسبة تتراوح بين 8%- 13% حسب إحصائيات منظمة الصحة العالمية الصادرة عام 2023 (1).
وتشيرُ الدّراسات العائلية إلى وجود أساس وراثي لهذه المتلازمة وذلك نظراً لارتفاع نسبة الإصابة بين الإناث اللواتي تربطهن صلات قربى (PCOS) (2)، ورغم انتشار المتلازمة، فلا تزال المسببات قيد الدراسة من الناحية الهرمونية والفيزيولوجية والوراثية بالإضافة لعوامل البيئة المحيطة وتأثيرها (3–5)، حيث يؤكّدُ التّغاير أو عدم التّجانس heterogeneity الإثني ethnic والجغرافي geographic لمتلازمة المبيض المتعدد الكيسات أنّ هذا الاضطراب مرتبط بعوامل بيئية، كما تقترح العديد من الدراسات تحرّي نمط الحياة لدى المريضات(6)، الفيزيولوجيا المرضية الخاصة بالمتلازمة معقّدة وتنطوي على سبلٍ وبروتينات متعددة (7)، واقترحت دراساتٌ الارتباط الواسع للمجين Genome-wide association studies (GWAS) وجودَ دلائلٍ قوية على أن العواملَ الجينيّة تلعب دوراً مهمّاً في إمراضية متلازمة المبيض متعدد الكيسات(3)، حيثُ تُشيرُ التّقديراتُ إلى أنّ العوامل الجينيّة تساهم بنسبة 79% في الإصابة بالمتلازمة، في حين أن العوامل البيئيّة وأسلوب الحياة يساهم بنسبة 21% في التعبير عن الاستعدادات الوراثية (8).
طُبّقت دراسات الارتباط الواسع للمجين لاستعراف الجينات المُؤَهِّبة للإصابة بالمتلازمة لدى النساء الآسيويات والأوروبيات، وتبيّن أنّ الجينات المشتبه بمساهمتها في إمراضية المبيض المتعدد الكيسات تشمل كلّاً من: مستقبل الهرمون المُنبّه للجريب Follicle Stimulating Hormone Receptor (FSHR)، مستقبل الإنسولين Insulin Receptor (INSR)، الهرمون المضاد لمولر Anti-Mullerian Hormone (AMH)، مُستَقبِل الهرمون المُلَوتِن/ مُوَجِّهَةُ الغُدَدِ التَّنَاسُلِيَّةِ المَشيمائِيَّة Luteinizing Hormone/Choriogonadotropin Receptor (LHCGR) (7,9).
تتصف المتلازمة بقلة/انعدام الإباضةoligo/anovulation وفرط الأندروجينيّة hyperandrogenism وتُعد زيادة الشعرانية hirsutism وحدها مؤشراً تنبؤيّاً لفرط الأندروجينيّة وعدم انتظام الدورة الشهرية menstrual irregularities (10)، بالإضافة إلى حَبُّ الشَّباب أو العدّ acne ومقاومة الإنسولين insulin resistance. أمّا التأثيرات طويلة الأمد لـ PCOS فتشمل كلاً من: العقم المُسَبّب بانعدام الإباضة anovulatory infertility (11)، والأمراض القلبية الوعائية cardiovascular diseases والبدانة obesity وداء السكري من النمط الثاني type2 diabetes (12).
يعد العقم أحد أهم وأبرز الآثار الصحية لمتلازمة المبيض متعدد الكيسات (11)، ويعدّ اضطراب الإباضة ovulation disorders أحد العوامل المُسببة وينجم عن اختلال توازن الهرمونات، حيث أنّ للهرمونات الجنسية ومستقبلاتها دوراً أساسياً في تكوّن الجريبات folliculogenesis (13)، وتؤثر زيادة مستويات الأندروجينات وانخفاض مستويات الإستروجين سلباً في عملية الإباضة، بالإضافة إلى مقاومة الإنسولين المرتبطة بالمتلازمة التي يمكن أن تسهم في اضطراب الإباضة (14).
يرتبط الهرمون المنبه للجريب بمستقبله ليُحَرِّض نمو البويضات في المبيض، وتطوّر الجُريبات عند الإناث، وله دور حاسم في تنظيم النمو والتطور الجنسي وعمليات التكاثر لدى الذكور والإناث (15,16). يتوضّع التعدد الشّكلي rs6166 C/T, Ser680Asn ضمن الإكسون العاشر من جين FSHR ويؤدي وجود النيكليوتيد C في موقع التّعدد الشّكلي إلى ترميز الحمض الأميني سيرين Serine، والنيكليوتيد T يرمّز للحمض الأميني أسبارجين Asparagine في الموقع 680 في مستقبل الهرمون المنبه للجريب قرب النّهاية الكربوكسيلية في المجال داخل الخلوي، مما قد يكون له أثر في نقل الشارة الخلوية (17).
الموادّ والطرائق Materials and methods
صممت هذه الدراسة على أن تكون دراسة رصدية من نمط حالة-شاهد observational case-control study، مشتملة على مجموعة من السيدات البالغات ممن لم يتجاوزن سن الإياس.
صنفت المشاركات ضمن ذراعين؛ ذراع الحالة case يشمل 38 مريضة، وكانت معايير الاشتمال: التّشخيص بمتلازمة المبيض متعدد الكيسات حسب معايير روتردام، ومعايير الاستبعاد: جميع أنواع الأورام المتعلقة بجهاز التكاثر الأنثوي، فرط تنسج الكظر، أمراض الغدة الدرقية النشطة، متلازمة كوشينغ، جميع عمليات الاستئصال التي تتضمن أجزاء من جهاز التكاثر الانثوي. بالإضافة إلى بعض المعايير التي تتضمن النساء الشواهد مثل الخضوع لعلاج يؤثر في استقلاب الكربوهيدرات، أو إفراز الغدد الصم، موانع حمل فموية، الأدوية الخافضة للشحوم، (يجب أن تكون مثل هذه العلاجات قد أُوقفَت قبل ثلاثة أشهر من إجراء الدراسة)، وأمراض السكري وفرط كوليسترول الدم.
ذراع الشاهد control يضم 46 سيدة ذات دورة شهرية منتظمة، مع مستويات طبيعية من الأندروجين وليس لديهم أي تاريخ عائلي للشعرانية. المجموعة الشاهدة مماثلة لمجموعة الحالات المريضات من حيث الفئة العمرية (18-45 سنة).
وحظيت الدّراسة بموافقة لجنة أخلاقيات البحث العلمي في كليّة الصّيدلة في جامعة دمشق، بالإضافة إلى الحصول على موافقة أفراد الدراسة المستنيرة Informed consent قبل انخراطهم فيها، وذلك بعد تقديم الشروحات الوافية عن هدف الدراسة والفوائد المرجوة منها والمخاطر المحتملة.
شملت هذه الدّراسة زوّار إحدى عيادات دمشق للإخصاب المساعَد، وجرت مراحل الدّراسة المخبريّة في مركز أبحاث العلاجات الحيوية وكليّة الصيدلة في جامعة دمشق.
بُزِلت عيّنات دم وريديّ محيطي بحجم 2.5 مل وجُمعت في أنابيب اختبار حاوية على مضاد تخثّر (EDTA) تمّ استخلاص الدنا المجيني من العينات المحفوظة بعد فكّ تجميدها، حسب الإرشادات المرفقة مع عتيدة استخلاص الدنا Blood DNA Preparation-Solution Kit من شركة Jenabioscience الألمانية. تمّ اختيار زوج من المشارع Primers من أحد الأدبيّات (18)، بهدف تضخيم الشدفة من الدنا الحاوية على التّعدد الشّكلي rs6166 C/T بواسطة PCR، تمّ التحقّق من نوعيّتهما عبر أداتيّ MFE Primer وGenome Data Viewer/NCBI.
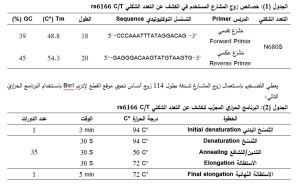
أُظهرت النواتج بالترحيل على هلامة آغاروز 1.7%.
تم التّقصي عن التعدد الشكلي بواسطة أنزيم التقييد BsrI من شركة New England Biolabs وحُضّر تفاعل القطع الأنزيمي بحجم نهائي 20 ميكروليتر حيث تمّت إضافة 4-8 ميكروليتر من منتج الـPCR حسب تركيز المنتج، و2 ميكروليتر من الوقاء المرفق مع الأنزيم، و1ميكروليتر من الأنزيم وتتمة الحجم بماء خالٍ من النكلياز.
حُضنت العينات مدة 180 دقيقة في حمّام مائي بدرجة65 C° ثمّ رُحّلَت منتجات القطع للحجم كاملاً مع صبغة التحميل 6X بنسبة 5:1 على هلامة أغاروز بتركيز 4%، بفولتيّة 50 ولمدة 30 دقيقة.
أُجريَ التحليل الإحصائي للأنماط الجينية باستخدام برنامج R الإحصائي وبرنامج GraphPad Prism (version 8.0.1) تمت مقارنة توزع الأنماط الجينية والألائل بين مجموعتي الدراسة باستخدام اختبار Chi-square لمعرفة فيما إذا كانت الفروقات الملاحظة يُعتد بها إحصائياً (P-value< 0.05) أو أن هذه الفروقات ناتجة عن المصادفة (P-value> 0.05).
النتائج Results
ظهرت بنتيجة تفاعل البوليمراز التّسلسلي شدفة وحيدة بطول يقارب 114 زوج أساس، ويمكن رؤية مثال لترحيل منتجات تفاعل الPCR لستّ عينات (الشكل 1).
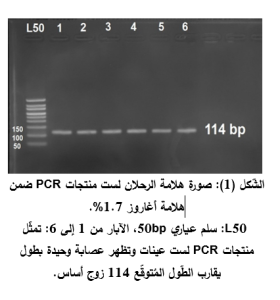
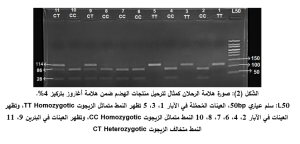
يظهر لدى تطبيق تفاعل الهضم الأنزيمي بأنزيم BsrI على منتج PCR عصابتان بأطوال 86 و28 زوج أساس، نظراً لاحتواء الشدفة لموقع قطع واحد فقط في حال وجود الأساس C في موقع التّعدد الشّكلي. في حالة تماثل الزيجوت Homozygotic CC فتكون نتيجة القطع ظهور عصابتين بأطوال 86 و 28 زوج أساس، وعصابة واحدة بطول منتج الـPCR 114 زوج أساس في حال وجود الأساس T في موقع التّعدد الشّكلي في الأليلين حيث يغيب موقع القطع (حالة تماثل الزيجوت Homozygotic TT)، أما في النمط متخالف الزيجوت Heterozygotic CT فتكون نتيجة القطع ظهور ثلاث شدف بأطوال 114، 86 و28 زوج أساس ويمكن رؤية مثال لترحيل منتجات تفاعل الهضم لإحدى عشرة عينة (الشكل 2).
تُبيّن نتيجة التّنميط الجيني لمجموعة المرضى أنّ النّمط الجيني متغاير الزيجوت CT الأكثر تواتراً بنسبة 65.79 % وقابلتها في مجموعة الشّواهد نسبة 43.48%، بينما كانت نسبة الأنماط متماثلة الزيجوت CC وTT عند المرضى 10.53 و23.68 على التّرتيب، وعند الشّواهد 23.91 و32.61 على التّرتيب، دون وجود فارق معتدّ به إحصائيّاً في توزّع النّمط الجيني بين الحالات والشواهد (P=0.1). بلغ تواتر الأليل C 43.42% في مجموعة الحالات و45.65% في مجموعة الشّواهد، أمّا الأليل T فقد بلغ تواتره 56.58% في مجموعة الحالات و54.35% في مجموعة الشّواهد بدون وجود فارق يُعتدّ به إحصائياً (P=0.7)، كما يوضّح الجدول (3).
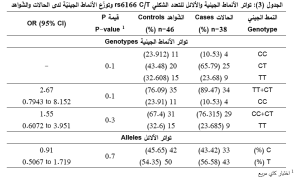
المناقشة Discussion
تبدي التّغايرات الجينية تباينات شديدة بين الأعراق والإثنيات المختلفة وتُعدّ دراسة تواتر التعددات الشّكلية وعلاقتها بالأمراض بين الأثنيات المختلفة ضرورة للتنبّؤ بحدوث الأمراض وإمكانيّة تدبيرها بالشّكل المناسب لكل جمهرة سكانيّة.
تُبيّن نتيجة التّنميط الجيني لمجموعة المرضى أنّ النّمط الجيني الأكثر تواتراً هو النمط متغاير الزيجوت CT دون وجود فارق معتدّ به إحصائيّاً في توزّع النّمط الجيني بين الحالات والشواهد (P=0.1). اتّفقت نتائجنا مع دراسة في البرتغال حيثُ لم يوجد فارق يُعتدّ به إحصائيّاً للأنماط الجينية بين مجموعتي الحالات والشّواهد وبلغ عدد العينات 80 حالة و80 شاهد (19). واتفقت نتائجنا أيضاً مع دراسة في السعودية حيثُ لم يوجد فارق يُعتدّ به إحصائيّاً للأنماط الجينية بين مجموعتي الحالات والشّواهد وبلغ عدد العينات 96 حالة 96 شاهد (20). واختلفت مع دراسة في كوريا الجنوبية حيثُ كان الفارق ذو دلالة إحصائية (P=0.035) وبلغ عدد العينات 377 مريضة PCOS و388 شاهد (21).
لم يُلاحظ وجود فارق يُعتدّ به إحصائياً في توزع الأليل بين مجموعتي الحالات والشّواهد (P=0.7)، حيثُ بلغ تواتر الأليل C 43.42% في مجموعة الحالات و45.65% في مجموعة الشّواهد، أمّا الأليل T فقد بلغ تواتره 56.58% في مجموعة الحالات و54.35% في مجموعة الشّواهد. اتفقت نتائجنا مع دراسة في الصين الشّمالية (15)، ومع دراسة في تركيا (18)، واختلفت مع دراسة الهندية (13).
الاستنتاجات Conclusions
لا تدعم نتائج هذه الدراسة وجود ارتباط بين التعدد الشكليّ rs6166 C/T في جين مستقبل الهرمون المنبّه للجريب والإصابة بمتلازمة المبيض متعدد الكيسات في هذه المجموعة السكانية المدروسة.
المحدوديّات Limitation: تعذّر الحصول على بيانات المريضات من الطول والوزن، بالإضافة إلى صغر حجم العينة بسبب تكلفة الاختبارات الجينيّة.
التوصيات Recommendation: دراسة علاقة التعدد الشّكلي rs6166 C/T بكل معيار من معايير تشخيص المبيض المتعدد الكيسات، وعلاقة أنماطه الجينيّة مع هرمون المنبّه الجريب للجريب.
قائمة الاختصارات List of abbreviations:
| Follicle-stimulating hormone receptor | FSHR |
| Polymerase chain reaction | PCR |
| Polycystic ovary syndrome | PCOS |
| Restriction fragment length polymorphism | RFLP |
| Genome-wide association studies | GWAS |
| Anti-Müllerian Hormone | AMH |
| Luteinizing Hormone/Choriogonadotropin Receptor | LHCGR |
| Insulin Receptor | INSR |
الموافقة الأخلاقية والموافقة على المشاركة Ethics approval and consent to participate
حصلت هذه الدراسة على موافقة لجنة أخلاقيات البحث العلميّ في جامعة دمشق بتاريخ 24/2/2025، وبرقم 919.
تضارب المصالح Conflict of interests
يقر المؤلفون بعدم وجود مصالح متضاربة.
التمويل Funding
تم تمويل هذا البحث من قِبَل جامعة دمشق.
مساهمات المؤلفين contributions’Authors
زينه أبو شامي: الباحث الأساسي، القيام بالجزء العملي من البحث والكتابة النظرية للأطروحة والمقالة.
مروان الحلبي: المشرف المشارك، الإشراف الأساسي على جمع العينات والإشراف على الجانب السريري المتعلق بالمريضات.
لمى يوسف: المشرف الأساسي للبحث، الإشراف على جميع تفاصيل البحث من تصميم خطة البحث والتوجيهات في الجانب العملي وتدقيق الكتابة النظرية.
المراجع :- WHO [Internet]. 2023 [cited 2025 Jan 2]. Polycystic ovary syndrome. Available from: https://www.who.int/news-room/fact-sheets/detail/polycystic-ovary-syndrome
- Subhi Ramadhan R. Molecular analysis of FSH receptor gene in Iraqi women with PCOS syndrome. Middle East Fertil Soc J. 2018 Dec 1;23(4):404–8.
- Lidaka L, Bekere L, Rota A, Isakova J, Lazdane G, Kivite-Urtane A, et al. Role of single nucleotide variants in fshr, gnrhr, esr2 and lhcgr genes in adolescents with polycystic ovary syndrome. Diagnostics. 2021 Dec 1;11(12).
- Elting MW, Korsen TJM. Women with polycystic ovary syndrome gain regular menstrual cycles when ageing. Vol. 15, Human Reproduction. 2000.
- Hahn S, Tan S, Elsenbruch S, Quadbeck B, Herrmann BL, Mann K, et al. Clinical and Biochemical Characterization of Women with Polycystic Ovary Syndrome in North Rhine−Westphalia PCOS´Infertility´Hirsutism´Obesity´HyperandrogenismÉthPCOS´PCOS´InfertilityPCOS´Infertility´PCOS´Infertility´HirsutismPCOS´Infertility´Hirsutism´PCOS´Infertility´Hirsutism´ObesityPCOS´Infertility´Hirsutism´Obesity´PCOS´Infertility´Hirsutism´Obesity´HyperandrogenismPCOS´Infertility´Hirsutism´Obesity´HyperandrogenismÉth− nic diversity.
- De Melo AS, Dias SV, De Carvalho Cavalli R, Cardoso VC, Bettiol H, Barbieri MA, et al. Pathogenesis of polycystic ovary syndrome: Multifactorial assessment from the foetal stage to menopause. Vol. 150, Reproduction. BioScientifica Ltd.; 2015. p. R11–24.
- Khan MJ, Ullah A, Basit S. Genetic basis of polycystic ovary syndrome (PCOS): Current perspectives. Vol. 12, Application of Clinical Genetics. Dove Medical Press Ltd.; 2019. p. 249–60.
- Ali RM, Shkurat TP, Alexandrova AA, Bugrimova ES, Lomteva S V., Ammar MN. Association of CYP17 gene polymorphism (rs743572) with polycystic ovary syndrome. Vol. 31, Meta Gene. Elsevier B.V.; 2022.
- Wan P, Meng L, Chao Huang &, Dai B, Jin Y, Chai L, et al. Replication study and meta-analysis of selected genetic variants and polycystic ovary syndrome susceptibility in Asian population. Available from: https://doi.org/10.1007/s10815-021-02291-1
- Hiam D, Moreno-Asso A, Teede HJ, Laven JSE, Stepto NK, Moran LJ, et al. The genetics of polycystic ovary syndrome: An overview of candidate gene systematic reviews and genome-wide association studies. Vol. 8, Journal of Clinical Medicine. MDPI; 2019.
- Costello MF, Misso ML, Wong J, Hart R, Rombauts L, Melder A, et al. The treatment of infertility in polycystic ovary syndrome: A brief update. Australian and New Zealand Journal of Obstetrics and Gynaecology. 2012 Aug;52(4):400–3.
- Ajmal N, Khan SZ, Shaikh R. Polycystic ovary syndrome (PCOS) and genetic predisposition: A review article. Vol. 3, European Journal of Obstetrics and Gynecology and Reproductive Biology: X. Elsevier Ireland Ltd; 2019.
- Sujatha T, Jayashankar E, Addepally U, Vijayalakshmi K, Hasan Q. Association of follicle-stimulating hormone receptor gene ser680 asn (rs6166) polymorphism with polycystic ovarian syndrome. Int J Reprod Contracept Obstet Gynecol. 2016;3126–32.
- Marinelli S, Napoletano G, Straccamore M, Basile G. Female obesity and infertility: outcomes and regulatory guidance. Vol. 93, Acta Biomedica. Mattioli 1885; 2022.
- Wu XQ, Xu SM, Liu JF, Bi XY, Wu YX, Liu J. Association between FSHR polymorphisms and polycystic ovary syndrome among Chinese women in north China. J Assist Reprod Genet. 2014;31(3):371–7.
- Sindiani AM, Batiha O, Al-zoubi E, Khadrawi S, Alsoukhni G, Alkofahi A, et al. Association of single-nucleotide polymorphisms in the ESR2 and FSHR genes with poor ovarian response in infertile Jordanian women. Clin Exp Reprod Med. 2021;48(1):69–79.
- Santi D, Potì F, Simoni M, Casarini L. Pharmacogenetics of G-protein-coupled receptors variants: FSH receptor and infertility treatment. Vol. 32, Best Practice and Research: Clinical Endocrinology and Metabolism. Bailliere Tindall Ltd; 2018. p. 189–200.
- Unsal T, Konac E, Yesilkaya E, Yilmaz A, Bideci A, Ilke Onen H, et al. Genetic polymorphisms of FSHR, CYP17, CYP1A1, CAPN10, INSR, SERPINE1 genes in adolescent girls with polycystic ovary syndrome. J Assist Reprod Genet. 2009 Apr;26(4):205–16.
- Vieira IH, Carvalho AF, Almeida Reis S, Carreira AL, Dias C, Fernandes S, et al. Association Between Follicle-Stimulating Hormone Receptor (FSHR) rs6166 and Estrogen Receptor 1 (ESR1) rs2234693 Polymorphisms and Polycystic Ovary Syndrome Risk, Phenotype, and Reproductive Outcomes in an Infertile Portuguese Population. Cureus. 2023 Mar 2;
- Alshammary AF, Alsobaie SF, Alageel AA, Aldakheel FM, Ansar S, Alrashoudi R, et al. Molecular Role of Asn680Ser and Asp37Glu Missense Variants in Saudi Women with Female Infertility and Polycystic Ovarian Syndrome. Curr Issues Mol Biol. 2023 Jul 1;45(7):5494–514.
- Kim JJ, Choi YM, Hong MA, Chae SJ, Hwang K, Yoon SH, et al. FSH receptor gene p. Thr307Ala and p. Asn680Ser polymorphisms are associated with the risk of polycystic ovary syndrome. J Assist Reprod Genet. 2017 Aug 1;34(8):1087–93.