المستويات البلازمية للحديد لدى مرضى سرطان بروستات سوريين حديثي التشخيص تبعاً لمرحلة الورم ودرجته
2026-03-15 | المجلد السابع العدد السابع - المجلد السابع | مقالات بحثيةراما عاصم قندقجي | رنوة محمود السيد
الملخص
الخلفية وهدف البحث: يعد سرطان البروستات من أكثر أنواع السرطانات شيوعاً بين الرجال، وتزداد نسبة حدوثه مع التقدم في العمر، رغم من عدم القدرة على تحديد عوامل بيئية مسؤولة عن الإصابة به بشكل قاطع؛ إلا أن نمط الحياة والتعرض المزمن لبعض المؤثرات البيئية قد يلعب دوراً في الإصابة بالمرض. تعد المستويات العالية من الحديد ذات علاقة وثيقة بنمو الخلايا السرطانية، إذ إن التدفق المتزايد للحديد داخل الخلايا يعدّ ضرورياً لانقسامها وبقائها. هذا الارتباط يجعل من الحديد عامل اختطار محتملاً في سياق تطور الأورام، ومن جانب آخر قد يؤثر اضطراب توازنه داجل جسم المريض على سير المعالجة ونتائجها؛ حيث يرتبط نقص الحديد بارتفاع معدلات المراضة والوفيات لدى مرضى السرطان، نتيجة تأثيره السلبي على المناعة والوظائف الحيوية الأساسية.
وبناءً على ما سبق؛ هدفت الدراسة إلى تقصي مستويات الحديد البلازمية لدى مرضى سرطان بروستات سوريين حديثي التشخيص ومقارنتها مع مجموعة شاهدة ودراسة ارتباط هذه المستويات مع مرحلة الورم ودرجته لدى المرضى.
مواد البحث وطرائقه: شملت الدراسة 80 رجلاً سورياً قُسموا إلى مجموعتين: مجموعة مرضى مصابين بسرطان البروستات ومشخصين حديثاً عن طريق الخزعة (n=40) ومجموعة شاهدة شملت مرضى مشخصين بفرط تنسج البروستات (n=20) وأشخاصاً سليمين ظاهرياً (n=20)، تم قياس التراكيز البلازمية للحديد بطريقة المقايسة اللونية.
النتائج : أظهرت النتائج تبايناً في المستويات البلازمية للحديد بين مجموعة مرضى سرطان البروستات والمجموعة الشّاهدة بجزئيها (السليمين ظاهرياً والمشخصين بفرط تنسج البروستات)، تمَّت دراسة توزُّع عينات الدراسة من حيث التَّراكيز البلازمية للحديد حيث كانت التَّراكيز البلازمية للحديد لدى الشّاهد أعلى من التَّراكيز البلازمية للحديد لدى المرضى بدلالة إحصائية P-Value = 0.000165 < 0.05
وُجِدَت علاقة ارتباط عكسيًّة ضعيفة ρ = -0.350 يعتدُّ بها إحصائياُّ P-Value = 0.02 < 0.05 بين مرحلة الورم ((Stage وتراكيز الحديد البلازمية، في حين لم تكن تلك العلاقة موجودة مع درجة الورم (Grade) ρ = -0.036 لا يُعتدّ بها إحصائياً P-Value = 0.82 > 0.05
الاستنتاجات: تشير الدراسة الحالية إلى تغاير المستويات البلازمية للحديد بشكل مثير للاهتمام لدى مرضى سرطان البروستات تبعاً لمرحلة الورم stage، وبالتالي من الممكن أن تكون تلك المستويات مؤشراً لتقدم المرحلة وسوء الإنذار لدى المرضى.
كلمات مفتاحية : سرطان البروستات، الحديد، مرحلة الورم ,Prostate cancer, Iron, Stage
المقدمة Introduction
يعد سرطان البروستات Prostate Cancer (PC) من الأورام الخبيثة التي تصيب الرجال، ويعد من الأسباب التي تؤدي إلى ارتفاع معدل معدلات الوفيات بين الرجال على مستوى العالم. (1)
في كل عام يتم تشخيص 1.6 مليون إصابة و 366000 حالة وفاة بسبب سرطان البروستات، حيث يأتي هذا السرطان عالمياً كخامس مسبب للوفيات من السرطانات عند الرجال، كما أنه يحتل المرتبة الثانية من ناحية ارتفاع معدلات الإصابة به كل عام. (2)
الحديد عنصر حيوي بالغ الأهمية يشارك في عمليات نقل الأوكسيجين وتكوين العديد من الأنزيمات المهمة للاستقلاب الخلوي، حيث يشارك في عمليات حيوية مثل نقل الأوكسيجين وتكوين الأنزيمات وتنظيم الاستقلاب الخلوي، ومع ذلك فإن تراكمه المفرط داخل الجسم يعد ساماً؛ نظراً لقدرته على تحفيز إنتاج الجذور الحرة عبر تفاعلات أكسدة إرجاع (نقل الالكترونات بين نوعين كيميائيين)، وهذا يمكنه من المشاركة في التفاعلات الضارة وغير المرغوب بها مثل توليد أنواع الأوكسيجين التفاعلية Reactive Oxygen Species (ROS)، ولهذا فإن عملية استقلاب الحديد تخضع لتنظيم محكم للغاية. حتى السنوات الأخيرة، كان تركيز قطاع الصحة العامة فيما يتعلق بمدخول الحديد منصباً على نقصه، حيث لا يزال يمثل النتيجة الأكبر لحالات نقص التغذية شيوعاً في العالم. ومن جهة أخرى اكتسب فرط الحديد أهمية متزايدة في الأبحاث الحديثة المتعلقة بالأمراض المزمنة كالسرطان (3)
تفاعل فنتون Fenton reaction هو تفاعل كيميائي بين الحديد وبيروكسيد الهيدروجين ينتج عنه جذر هيدروكسيل.
يرتبط توليد أنواع الأوكسيجين التفاعلية ارتباطاً وثيقاً بالتسرطن من خلال إحداث تلف في المكونات الخلوية بما في ذلك الدهون والبروتينات والحمض النووي بشكل أساسي. (4)
تظهر الخلايا السرطانية قدرةً على إعادة تشكيل مسارات استقلاب الحديد داخل الخلية بطرق تفضي إلى تراكمه، وذلك من خلال تعزيز التقامه وتخزينه، أو تقليل تصديره، أو كلا الأمرين معاً.(4) ، هذا التعديل الاستقلابي يرتبط بزيادة حاجة الخلايا السرطانية للحديد، حيث يسهم توفر الحديد بكميات عالية في دعم نموها وتكاثرها، بينما يؤدي حرمانها منه إلى تثبيط النمو. (5)
تشير البيانات السريرية إلى أن خلايا سرطان البروستات تحتجز الحديد بمستويات أعلى مقارنة بالخلايا الطبيعية المجاورة، والتي تظهر تراكيز منخفضة من الحديد. (6)
لم يعد دور الحديد يقتصر على تعزيز نمو الورم فحسب، بل ثبت أيضًا أنه يؤثر في القدرة على الانتشار والنقائل (5)
فقر الدم هو من المضاعفات الشائعة المصاحبة للأورام الخبيثة في مختلف مراحلها، وينجم غالباً عن عوامل متعددة تشمل الالتهابات المزمنة، انحلال الدم وارتشاح نقي العظم. وتقدر نسبة انتشاره المبلغ عنها بين 20% و60% في الأورام الصلبة.
في سياق سرطان البروستات، يمكن أن يكون فقر الدم ناجماً عن البيلة الدموية الناتجة عن غزو الورم للإحليل، أو نتيجة للنقائل العظمية المنتشرة التي تؤثر على وظيفة نقي العظم. (7)
يتجاوز تأثير فقر الدم في سرطان البروستات مجرد الأعراض المتعلقة بجودة الحياة. فقد خلُص تحليل تلوي meta analysis لـ 15 دراسة استعادية واستباقية retrospective and prospective إلى ارتباط فقر الدم بانخفاض معدل البقاء الإجمالي Overall Survival (OS) وكذلك انخفاض فترة البقاء دون تقدم المرض Progression-free survival. (7)
انطلاقاً ممّا سبق، فقد هدفت هذه الدّراسة إلى تقييم حالة الحديد لدى مرضى سرطان البروستات قبل بدء العلاج، وذلك بغرض مواءمة الخطة العلاجية وفقاً لوضع الحديد الفردي لكل مريض، وتدبير فقر الدم إن وجد بطريقة فعالة، مع تجنب التزويد غير الضروري بالحديد الذي قد يسهم في تعزيز نمو الخلايا السرطانية.
المواد والطرائق Materials and Methods
تصميم الدراسة وجمع العيّنات:
اشتملت الدّراسة التي كانت من نمط حالة – شاهد case-control study على 80 رجلاً سوريّاً قُسِّموا إلى مجموعتين؛ مجموعة الدراسة (case group) تضمَّنت 40 مريضاً شُخِّص لديهم سرطان البروستات حديثاً عن طريق إجراء خزعة، ولم يخضعوا لأي علاج. جُمِعَت عيّنات هذه المجموعة من مستشفى البيروني الجامعي في الفترة الواقعة بين شهر أيار من عام 2024 وشهر كانون الثاني من عام 2025.
مجموعة الشاهد (control group) تضمَّنت 40 رجلاً قسموا لمجموعتين: مجموعة تضمنت 20 رجلاً لديهم فرط تنسج بروستات حميد حيث كانت قيم Prostate Specific Antigen (PSA) لديهم (PSA<10 ng/ml) ومجموعة أخرى تضمنت 20 رجلاً سليماً ظاهرياً حيث كانت مستويات الـ PSA لديهم ضمن المجال الطبيعي(PSA = 0-4 ng/ml) ، جُمِعَت عيّنات مجموعة الشاهد من المخابر الخاصة في مدينتي دمشق وحمص في الفترة الواقعة بين شهر أيلول 2024 وشهر كانون الثاني من العام 2025.
شملت معايير اشتمال المرضى: مرضى مشخصون بواسطة الخزعة بسرطان البروستات وقبل البدء بالمعالجة أو الخضوع للعمل الجراحي، لا يوجد تاريخ لأورام أخرى.
بينما شملت معايير اشتمال الشواهد: أشخاصاً أصحاء ظاهرياً، مرضى مشخصون بفرط تنسج بروستات حميد، لا يوجد تاريخ لأي أورام.
استبعد المشارك من الدراسة عند تشخيص سرطان آخر غير سرطان البروستات، تلقي العلاج قبل جمع العينات لمرضى سرطان البروستات، إجراء الاستئصال الجراحي، تناول مكملات الحديد، وجود أمراض كبدية أو كلوية أو أمراض مزمنة أخرى، وجود تاريخ من نقل الدم.
وبالنسبة لجميع المتطوّعين استُخدِمَت استبانات شاملة لجمع المعلومات الطبيّة والحصول على التاريخ الكامل بما في ذلك نمط الحياة، والتّاريخ الطبّي، إضافةً إلى التّاريخ العائلي لسرطان البروستات وأنواع السّرطان الأخرى.
بالنسبة لمجموعة المرضى استُكمِلَت المعلومات حول حالة المريض من خلال الرّجوع إلى ملفّه الطبّي في المستشفى.
أُبلغ جميع المتطوّعين الذين شاركوا في هذه الدّراسة بأهداف الدّراسة وقاموا بتوقيع نموذج لموافقة خطيّة مستنيرة. حصلت هذه الدّراسة على موافقة مجلس أخلاقيّات الأبحاث الطّبيّة الحيويّة في جامعة دمشق بتاريخ 21\2\2024 برقم 1428\ص.
أخذ عيّنات الدّم والمقايسات الكيميائيّة الحيويّة:
جُمِعَ قُرابة 5 مل من الدم الوريدي من كل رجل، ووُضِعَت في أنبوب يحتوي على مضاد التخثر الهيبارين وثُفّلَت العيّنة بقوّة تثفيل نسبيّة تعادل 1000xg لمدّة 10 دقائق، بعدها تمّ فصل العيّنة والاحتفاظ بالبلازما في أنابيب ابندورف بدرجة حرارة -80 درجة مئويّة لحين إجراء المعايرة.
تمت معايرة مستويات الحديد البلازمية بطريقة المقايسة اللونيّة colorimetric assay باستخدام كيت من شركة Medichem المصنع في سوريا بامتياز ألماني وفق تعليمات الشّركة المُصنِّعة. تم إجراء الاختبارات في مختبر الكيمياء الحيوية والأحياء الدقيقة في جامعة دمشق؛ وشملت الأجهزة المُستَخدمة ما يلي: جهاز مقياس الطيف الضوئي Spectrophotometer نصف آلي من شركة JENWAY البريطانية، وحمام مائي.
الدراسة الإحصائية:
استُخدِم برنامج الحزمة الإحصائيّة SPSS الإصدار 26 لإنجاز كامل الدّراسة الإحصائيّة، وعبّرنا عن القيم باستخدام (المتوسّط الحسابيّ والانحراف المعياريّ)، وقورِنَت القيم بين مجموعتي الدراسة باستخدام اختبارMann-Whitney، أمّا اختبار ANOVA Test متبوعاً باختبار Tukey HSD Test فقد استُخدِم لدراسة الفروقات بين متوسطات المجموعات. بينما دُرِسَت علاقة الارتباط باستخدام اختبار سبيرمان، واعتُمِدَت قيمة P-value < 0.05 للاختبارات كقيمةٍ يُعتَدّ بها إحصائيّاً.
النتائج Results
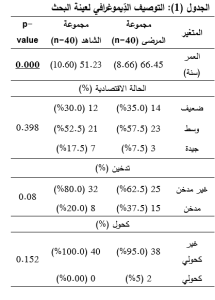
يبين الجدول 1 التوصيف الديموغرافي لعينة البحث حيث كانت الفئات العمرية التي يشاهد بها المرض مرتفعة بوسطي 66.45 عاماً، فيما بلغ وسطي العمر عند مجموعة فرط التنسج 59.1 سنة بينما متوسط عمر السليمين ظاهرياً 51.23 سنة.
تماثلت المجموعتان من حيث التدخين (p-value 0.08) لا يعتد به إحصائياً، إذ إنّ معظم المتطوعين غير مدخنين، وكانت الحالة الاقتصاديّة (تبعاً لإفادة المرضى والشواهد) متوافقة بين المجموعتين p-value =0.398)) لا يعتد به إحصائياً، وتكمن أهمية ذلك في إلغاء تأثير تفاوت الظروف المعيشية بين المتطوعين والتي تنعكس على الوارد الغذائي من الحديد وعلى مستويات الحديد في الدم لديهم.
تمَّ التَّعبير عن القيم باستخدام التكرار (النسبة المئوية) وذلك على مستوى جميع المتغيرِّات المدروسة باستثناء العمر حيث تمَّ التَّعبير عنه باستخدام (المتوسِّط الحسابيّ ± الانحراف المعياريّ)، تمَّ اختبار الاختلافات بين متوسِّطات المتغيِّرات باستخدام اختبار Mann-Whitney بعد التَّأكد من كونها لا تخضع للتَّوزيع الطبيعي بالاستعانة باختبار Kolmogorov-Smirnov، وتمَّ استخدام اختبار Chi-square لمقارنة المتغيِّرات الفئويَّة، واعتبرت P-value < 0.05 قيمة يعتد بها إحصائياً.
تم تصنيف الحالة الاقتصادية (حسب إفادة المشاركين بعد سؤالهم) اعتماداً على وجود دخل شهري ثابت: حيث اعتبر الدخل أقل من 500000 ليرة سورية شهرياً ضمن الفئة الضعيفة، ومن 500000 إلى 2000000 ليرة سورية ضمن الفئة المتوسطة، وفوق 2000000 ليرة سورية ضمن الفئة الجيدة.
تم تحديد حالة التدخين بناءً على إجابة المشاركين على السؤال المتعلق بذلك ضمن الاستبيان بـ نعم\لا
كما تم تحديد حالة تناول الكحول بناءً على إجابة المشاركين على السؤال المتعلق بذلك ضمن الاستبيان بـ نعم\لا.
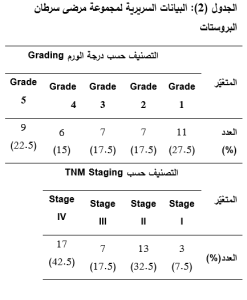
شملت الدّراسة 40 مصاباً بسرطان البروستات المُشخَّص حديثاً عبر إجراء خزعة نسيجيّة، توزعوا وفقاً لدرجة الورمTumor grade إلى والتّصنيف حسب TNM Staging كما يبيّن الجدول 2 علماً أن 95% من المرضى كانوا يعانون من سرطان البروستات من نمط الكارسينوما الغدية (Adenocarcinoma).
لدى دراسة الفرق في متوسطات التراكيز البلازمية للحديد بين المجموعتين (الحالة والشاهد) باستخدام اختبار مان ويتني Mann-Whitney U test، تبين أن التراكيز البلازمية للحديد لدى الشاهد أعلى من التراكيز البلازمية للحديد لدى المرضى P-value=0.000165<0.05 وهي قيمة يعتد بها إحصائياً كما هو مُوضَّح في الشكل 1.
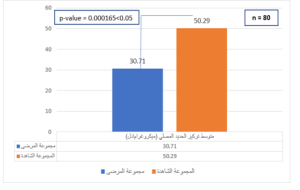
الشكل (1): فرق متوسط تراكيز الحديد البلازمية بين مجموعة مرضى سرطان البروستات والمجموعة الشاهدة
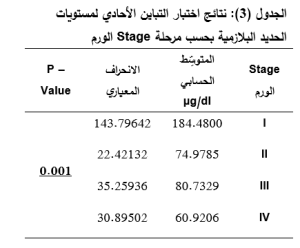
نستنتج من الجدول السابق بأنه توجد فروق ذات دلالة إحصائية في مستويات الحديد البلازمية بحسب Stage الورم حيث أن P-Value =0.001 وهي أصغر من 0.05 فهي بذلك ذات قيمة يعتد بها إحصائياً مما يشير إلى وجود علاقة ارتباط بين مستويات الحديد والمرحلة stage حيث أنه عند التمييز بين high\low) stage) بلغت قيمة P-Value عند high stage (stage4) P-Value =0.107 وعند low stage (stage 1,2,3) P-Value =0.072 حيث يمكننا أن نشير إلى وجود نزعة للفارق الإحصائي قد يعود ذلك لكون حجم العينة صغير.
يلاحظ من الجدول التالي وجود فرق دال إحصائيًّا في مستويات الحديد البلازمية بين مرحلة Stage الورم I مقارنة مع المرحلة الأخرى حيث يزيد متوسِّط مستويات الحديد البلازمية في الـ Stage I بمقدار 109.50±28.26 بالمقارنة مع مستويات الحديد البلازمية في الـ Stage II بصورةٍ دالَّةٍ إحصائيًّا (P-Value = 0.002 < 0.05) ويزيد متوسِّط مستويات الحديد البلازمية في الـStage I بمقدار 103.74±30.45 بالمقارنة مع مستويات الحديد البلازمية في الـ Stage III بصورةٍ دالَّةٍ إحصائيًّا (P-Value = 0.008 < 0.05) ويزيد متوسِّط مستويات الحديد البلازمية في الـ Stage I بمقدار 123.55±27.63 بالمقارنة مع مستويات الحديد البلازمية في الـ Stage IV بصورةٍ دالَّةٍ إحصائيًّا (P-Value = 0.000 < 0.05)، بينما لم يتم ملاحظة فروق يعتدُّ بها إحصائيًا في تراكيز الحديد البلازمية على مستوى الـمراحل Stages الأخرى.
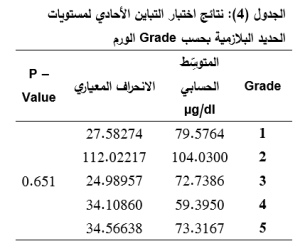
يظهر الجدول 4 أنه لا توجد فروق ذات دلالة إحصائية في مستويات الحديد المصلية بحسب Grade الورم حيث كانت قيمة P-Value =0.651 وهي أكبر من 0.05 وبالتالي غير دالَّةٍ احصائيًا.
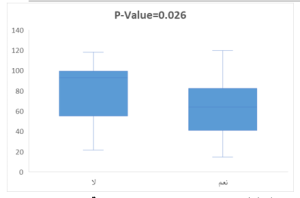
الشكل (2): اختلاف مستويات الحديد البلازمية بحسب وجود وغياب النقائل
يوضح الشكل التوزيع الإحصائي لتركيز الحديد في الدم لدى مرضى سرطان البروستات، حيث تظهر المجموعة المصابة بالنقائل نمطاً مختلفاً في التشتت والانحراف مقارنة بالمجموعة غير النقائلية.
المناقشة Discussion
أظهرت هذه الدراسة انخفاضاً إحصائياً في تركيز الحديد في الدم لدى مرضى سرطان البروستات مقارنةً بالشواهد، ويزداد هذا الانخفاض مع تقدم المرحلة السريرية للمرض stage ووجود النقائل، إذ أن اضطراب تنظيم الحديد داخل الخلايا قد يؤدي إلى نمو غير طبيعي وتحفيز تطور السرطان بما في ذلك النقائل، كما أنه لم يظهر لدينا ارتباط ذو دلالة إحصائية بين مستويات الحديد ودرجة الورم grade، مما يوحي بأن انخفاض الحديد يرتبط بشكل أكبر بمرحلة المرض السريرية stage وليس بدرجته النسيجية grade ، علماً أن الأنماط النسيجية كانت متشابهة لدى مرضى سرطان البروستات من نمط الكارسينوما الغدية (Adenocarcinoma).
يشير انخفاض الحديد الملاحظ لدى المرضى إلى احتمال وجود خلل استقلابي وظيفي في الحديد لا يصنف ضمن فقر الدم التقليدي، وهو ما يتماشى مع ما ورد في دراسة أجراها Yuce وزملائه التي بيّنت انخفاضاً في الحديد لدى المرضى، مما يشير إلى اضطراب وظيفي في استقلاب الحديد. (8)
كشفت نتائج الدراسة الحالية عن وجود فرق واضح في تركيز الحديد في الدم بين مرضى المرحلة الأولى (Stage I) والرابعة (Stage IV) من سرطان البروستات، إذ كان الحديد أعلى في المرحلة الأولى.
يمكن تفسير ذلك من خلال الآلية المرضية المعروفة بـ نقص الحديد الوظيفي (Functional Iron Deficiency) المرافق لفقر الدم المرتبط بالسرطان (Cancer-Related Anemia, CRA)، والتي تنتج عن اضطراب في معالجة الحديد داخل الجسم (Iron Handling Dysfunction) خلال تقدم المرض.
وفقاً لما ورد في دراسة Natalucci وزملائها فإن فقر الدم المرتبط بالسرطان لا ينتج عن نقص حقيقي في الحديد، بل نتيجة ارتفاع العوامل الالتهابية المزمنة (Chronic Inflammatory Cytokines)، لا سيما Interleukin-6 (IL-6)، التي تحفّز إنتاج الهيبسيدين (Hepcidin)؛ وهو البروتين المسؤول عن تنظيم استقلاب الحديد (Iron Metabolism Regulator).
يعمل الهيبسيدين على تثبيط تصدير الحديد من الخلايا البالعة (Macrophages) والكبد (Liver) عبر تقليل نشاط بروتين الفيروبورتين (Ferroportin, FPN)، مما يؤدي إلى احتجازه داخل الخلايا وانخفاض تركيزه في الدم، وهو نمط يعرف سريرياً بـ “نقص الحديد الوظيفي” ويميز المراحل المتقدمة من السرطان. (9)
وتدعم هذه الآلية ملاحظات سريرية منشورة عن سرطان البروستات تحديداً؛ فقد أوضحت دراسة Vela أن خلايا سرطان البروستات تُظهر خللاً في التعبير الجيني لبروتينات الحديد، حيث يُلاحظ زيادة في التقام الحديد عبر مستقبلات الترانسفيرين (Transferrin Receptor 1, TFR1) وتنظيم مفرط للبروتينات الداخلية المنظمة للحديد (Iron Regulatory Protein 2, IRP2) مع انخفاض واضح في تصديره عبر FPN. (10)
هذا النمط يؤدي إلى احتجاز الحديد داخل الخلايا السرطانية ويُسهِم في ظهور فقر الدم في المراحل المتقدمة، بما ينسجم مع النتائج الإحصائية الحالية التي تُظهر انخفاض الحديد في المرحلة الرابعة وارتفاعه في المرحلة الأولى قبل نشوء اضطراب الاستقلاب. (10)
حيث أن فقر الدم ونقص الحديد شائعان في المراحل المتقدمة من سرطان البروستات إذ يرتبط فقر الدم بشكل واسع بالمراحل المتقدمة منه. (7)
يمكن تفسير انخفاض الحديد لدى مرضى المرحلة المتقدمة من سرطان البروستات بوجود آليات مرضية متعددة تسهم في تطور فقر الدم المزمن التي من أبرزها البيلة الدموية Hematuria كنمط من أنماط النزف البطيء غير الظاهر سريرياً(11) ، حيث تتراوح نسبة انتشار فقر الدم بين مرضى سرطان البروستات بين 13% و78% (7)، فمع تقدم الورم قد يغزو الورم الإحليل أو جدار المثانة مما يؤدي إلى نزيف بولي مزمن يؤدي تدريجياً إلى استنزاف الحديد من الجسم، في دراسة أجراها Nalesnik وزملائه ذكر أن البيلة الدموية ومصادر النزف البطيء الأخرى تعتبر من العوامل المهمة في حدوث فقر الدم عند مرضى سرطان البروستات المتقدم، وأوضحوا أن النزف ينجم غالباً عن النمو الداخلي للورم في الإحليل أو نقائله داخل المثانة. (11)
في المقابل خالفت نتائجنا نتائج دراسة Saleh وزملائه، إذ أظهرت نتائجها ارتفاعاً في مستويات الحديد لدى المرضى قبل بدء العلاج. يعزى هذا التباين إلى اختلاف التباينات الوراثية ونمط التغذية بين المشاركين. (12)
للدراسة الحاليّة بعض المحددات منها أن عدد العينات في المراحل المبكرة قليل.
الاستنتاجات Conclusions
يشير ارتباط المرحلة الأقل من الورم مع المستويات البلازمية الأعلى للحديد عند المرضى المُشخصين حديثاً إلى دور مُحتَمل للحديد لدى هذه المجموعة المرضيّة ممّا يستدعي أخذ ذلك بعين الاعتبار لتحديد حالة الحديد لدى المرضى لمواءمة خطة العلاج وتدبير فقر الدم بالشكل الأمثل إن وجد وتجنب الإضافات غير الضرورية للحديد لدى هؤلاء المرضى.
لا بدّ من إجراء دراسات على أعداد أكبر من المرضى لفهم أعمق للعلاقة المُعقّدة بين الحديد والخليّة السرطانيّة، بالإضافة إلى ضرورة مُتابعة المرضى ومراقبة مستويات الحديد لديهم وعلاج حالة فقر الدم في المراحل المتقدمة من الورم.
قائمة الاختصارات List of abbreviations
CAR: Cancer-Related Anemia
FPN: Ferroportin
IRP2: Iron Regulatory Protein 2
M: distant metastasis
N: the regional lymph nodes status
OS: overall survival
PC: Prostate Cancer
ROS: reactive oxygen species
T: Tumor size
TFR1: Transferrin Receptor 1
تضارب المصالح Conflict of interests
يُقِرّ جميع الباحثين المشاركين في هذا البحث بعدم وجود تضاربٍ في المصالح فيما بينهم.
التمويل Funding
موّلت جامعة دمشق البحث جزئياً.
مساهمات المؤلفين Author’s contributions
راما قندقجي: تصميم الدراسة، تجنيد المشاركين بالدراسة، جمع العينات، تحليل البيانات، كتابة المقالة.
رنوة السيد: تصميم الدراسة، تحليل البيانات، تدقيق المقالة.
الشكر والتقدير Acknowledgements
نود أن نشكر الطاقم الطبّي في مستشفى البيروني الجامعي في دمشق.
المراجع :- Sekhoacha M, Riet K, Motloung P, Gumenku L, Adegoke A, Mashele S. Prostate Cancer Review: Genetics, Diagnosis, Treatment Options, and Alternative Approaches. Vol. 27, Molecules. MDPI; 2022.
- Prostate Source: Globocan 2020 Number of new cases in 2020, both sexes, all ages [Internet]. 2020. Available from: https://gco.iarc.fr/today
- Fonseca-Nunes A, Jakszyn P, Agudo A. Iron and cancer risk-a systematic review and meta-analysis of the epidemiological evidence. Vol. 23, Cancer Epidemiology Biomarkers and Prevention. 2014. p. 12–31.
- Torti S V., Manz DH, Paul BT, Blanchette-Farra N, Torti FM. Iron and cancer. Vol. 38, Annual Review of Nutrition. Annual Reviews Inc.; 2018. p. 97–125.
- Torti S V., Torti FM. Iron and cancer: 2020 vision. Vol. 80, Cancer Research. American Association for Cancer Research Inc.; 2020. p. 5435–48.
- Vela D. Iron metabolism in prostate cancer; from basic science to new therapeutic strategies. Vol. 8, Frontiers in Oncology. Frontiers Media S.A.; 2018.
- Wong CHM, Ko ICH, Leung DKW, Chan HC, Li KM, Chan YS, et al. Anaemia and iron deficiency in advanced prostate cancer: revisiting a common morbidity. Hong Kong Med J. 2025 Apr 1;31(2):154–8.
- Yuce A, Benli E, Cirakoglu A, Keles M, Yazici I, Acet A. Comparison of serum iron, hemoglobin, ferritin and crp levels in prostate cancer patients with a control group Running title: Serum iron levels in prostate cancer. Ann Med Res. 2023;30(5):1.
- Natalucci V, Virgili E, Calcagnoli F, Valli G, Agostini D, Zeppa SD, et al. Cancer related anemia: An integrated multitarget approach and lifestyle interventions. Vol. 13, Nutrients. MDPI AG; 2021. p. 1–37.
- Vela D. Iron metabolism in prostate cancer; from basic science to new therapeutic strategies. Vol. 8, Frontiers in Oncology. Frontiers Media S.A.; 2018.
- Nalesnik JG, Mysliwiec AG, Canby-Hagino E. Anemia in Men With Advanced Prostate Cancer: Incidence, Etiology, and Treatment. Vol. 6, REVIEWS IN UROLOGY 1 [Rev Urol. 2004.
- Saleh SAK, Adly HM, Abdelkhaliq AA, Nassir AM. Serum levels of selenium, zinc, copper, manganese, and iron in prostate cancer patients. Curr Urol. 2020 Mar 1;14(1):44–9.