تأثير التّعدد الشّكلي مفرد النكليوتيد Taq-I (rs731236) في جين مستقبل فيتامين D في اختطار الإصابة بالتهاب المفاصل الرثياني وشدة المرض لدى مرضى سوريين
2026-03-15 | المجلد السابع العدد السابع - المجلد السابع | مقالات بحثيةزينب سعيد شحادة | لمى علي يوسف | ميسون أحمد قدسي | إبراهيم وليد حنفي | رهام سمير أنطاكي
الملخص
الخلفية وهدف البحث: يُعدّ التهاب المفاصل الرثياني (RA) مرضاً مناعياً ذاتياً مزمناً، يتميّز بالتهاب مفصلِي مزمن، ومضاعفاتٍ جهازيّةٍ، وارتفاعٍ في معدلات الوفيّات. تؤدي مستقبلات فيتامين D (VDR) دوراً تنظيمياً في الجهاز المناعي، ويُعتقد أنّ التغايرات الجينية في الجين المرمزة لها قد تؤثّر في القابلية للإصابة بـ RA. هدفت هذه الدّراسة إلى تحرّي العلاقة بين التّعدد الشّكلي مفرد النكليوتيد(rs731236) Taq-I في الجين المرمز لمستقبل فيتامين D واختطار الإصابة بالتهاب المفاصل الرثياني، إضافةً إلى تقييم تأثير هذا التغاير في فعاليّة المرض والتراكيز المصليّة لفيتامين D لدى جمهرة من السّوريين.
مواد البحث وطرائقه: صمّمت الدراسة الحاليّة لتكون من نمط حالات-شواهد وأُجريت في مستشفيي المواساة والوطني الجامعيين في دمشق في الفترة الممتدة من آذار حتى حزيران 2023، وشملت 100 مريضٍ RA و100 شخصٍ سليمٍ مماثلٍ من حيث العمر والجنس. قيست التراكيز المصليّة للكالسيفيرول (25(OH)D) بتقنيّة المقايسة المناعية بالتألّق الكيميائي الكهربائي، وقُيّمت فعاليّة المرض باستخدام حرز DAS28-CRP، واستعرفت الأنماط الجينيّة للتغاير Taq-I باستخدام تقنية تفاعل البوليميراز المتسلسل (PCR) المتبوع بالسلسلة وفق طريقة سانغر لمنطقة الـDNA المستهدفة. أجريت التحليلات الإحصائية باستخدام برنامج SPSS الإصدار 26.
النتائج : أبدى مرضى الـ RA قيماً أخفض لمتوسط التراكيز المصليّة لفيتامين D مقارنةً بالشواهد (22.38 ±15.80 مقابل 27.56 ± 13.04 نانوغرام/مل، (p=0.036، مع تواترٍ أعلى لعدم كفاية/عوز فيتامين D %50) مقابل 35%). تبيّن وجود اختلافٍ دالٍّ إحصائيّاً في تواتر ألائل التّعدّد الشّكلي Taq-I بين المرضى والشواهد(p=0.001) ، وارتبط الأليل G بزيادة اختطار الإصابة بـ RA حيث بلغ منسب الأرجحيّة الضّعف OR=2.00)،P=0.001 ). كذلك، لوحظ ارتباط النّمط متماثل الزيجوت AA بشدةٍ مرضيةٍ أعلى (DAS28 ≥ 5.1).
الاستنتاجات: يرتبط التغاير(rs731236) Taq-I في الجين المرمز لـ VDR بزيادة اختطار الإصابة بالتهاب المفاصل الرثياني وشدّته لدى العيّنة السورية المدروسة. تقترح النتائج إجراء دراساتٍ مستقبليةٍ موسّعةٍ لتأكيد هذه العلاقة وتوضيح آلياتها
كلمات مفتاحية : التهاب المفاصل الرثياني، 25(OH)D، مستقبل فيتامين D، Taq-I (rs731236)، SNP، DAS28CRP، سوريون, Rheumatoid arthritis, 25(OH)D, Vitamin D receptor, Taq-I-I (rs731236), SNP, DAS28-CRP, Syrians.
المقدمة Introduction
يُعدّ التهاب المفاصل الرثياني Rheumatoid arthritis (RA) مرضاً مناعياً ذاتياً شائعاً ومزمناً، يصيب الغشاء الزليلي في المفاصل ويؤدي إلى تآكل العظام وتشوهاتٍ مفصليةٍ مع مرور الوقت (1). وعلى الرغم من التقدم في وسائل التشخيص والعلاج، لا تزال الآلية الإمراضية الدقيقة للمرض غير مفهومةٍ تماماً (2). تشير المعطيات الحديثة على نحو متزايد إلى أنّ لفيتامين D دوراً يتجاوز استقلاب الكالسيوم والعظام، ليشمل تنظيم الاستجابات المناعية الفطرية والمكتسبة. يُعبَّر عن مستقبل فيتامين D (VDR) في العديد من الخلايا المناعية، بما في ذلك الخلايا التائية والبائية، والأرومات الليفية (3). وقد أظهرت بعض الدراسات أن التغايرات الجينية في الجين المُرمِّز لمستقبل فيتامين D (VDR)قد تؤثر في مستويات التعبير الجيني على مستوى الانتساخ أو في بنية البروتين أو وظيفته، مما قد يسهم في زيادة القابلية للإصابة بأمراض مناعية مثل التهاب المفاصل الرثياني (RA) (4، 5).
يُعدّ التّعدد الشّكلي مفرد النكليوتيد Taq-I ذو الرقم التعريفي (rs731236)، والذي يقع في الإكسون التاسع للجين المرمّز لمستقبل فيتامين D (VDR)، أحد التّعددات الشّكليّة الشائعةِ في جين الـVDR ، ويُعتقد أنه يؤثر في ثباتيّة المنتسخات. وبالرغم من أن هذا التغاير لا يُحدِث تغييراً في تسلسل الأحماض الأمينية، إلا أن ارتباطه بأمراض مناعية متعددة يشير إلى أهميته التنظيمية (6، 7).
هدفت هذه الدراسة إلى تحرّي العلاقة بين التّعدد الشّكلي Taq-1 واختطار الإصابة بالتهاب المفاصل الرثياني في جمهرةٍ سوريةٍ، مع دراسة علاقته بشدة المرض والتراكيز المصليّة لفيتامين D.
المواد والطرائق Materials and Methods
تصميم الدراسة والمشاركون
صُمّمت دراستنا الحاليّة لتكون رصديّة من نمط حالات-شواهد case-control study، وحازت الموافقة الأخلاقية ذات الرقم التعريفي MD-210-125-21-h23 الممنوحة من قبل لجنة الأخلاقيّات الحيوية في جامعة دمشق، وأجريت في مستشفيي المواساة والوطني الجامعيين في دمشق بين شهري آذار وحزيران من عام 2023.
شملت الدراسة 100 مريضٍ بالغ ٍمشخّصٍ بالتهاب المفاصل الرثياني (RA) وفقاً لمعايير التصنيف الصادرة عن الكلية الأمريكية لأمراض الروماتيزم American College of Rheumatology/الرابطة الأوروبية لمكافحة الروماتيزم European Alliance of Associations for Rheumatology لعام 2010(ACR/EULAR 2010) ، بالإضافة إلى 100 شخصٍ سليمين ظاهرياً في مجموعة الشّواهد ومماثلين للمرضى من حيث العمر والجنس. قدّم جميع المشاركين موافقاتهم الخطية المستنيرة قبل انخراطهم في الدراسة. تضمنت معايير الأهلية/التّضمين أن يكون عمر المشاركين ≥18 سنة، مع تعرّض منتظم لأشعة الشمس (≥3 ساعات/أسبوع)، وعدم وجود حالاتٍ مرضيّةٍ أو دوائيّةٍ معروفةٍ بتأثيرها في التراكيز المصلية لفيتامين D.
مقايسة وتصنيف حالة فيتامين D
قيست التراكيز المصليّة البدئيّة لـ 25 هيدروكسي فيتامينD المُعبر عنها بالكالسيفرول أو [25 (OH) D] باستخدام المقايسة المناعية بالتألّق الكيميائي الكهربائي (عتيدةElecsys® Vitamin D Total G3 ، من شركة Roche Diagnostics، ألمانيا)، وجرى تصنيف حالة فيتامين D لدى المشاركين بحسب التّراكيز المصليّة لفيتامين D وفق إرشادات معهد الطب Institute of Medicine (IOM) إلى الفئات التالية: حالة كفاية Sufficiency فيتامين D (التراكيز الأعلى من 20 نانوغرام/مل)، حال عدم كفاية Insufficiency فيتامين D (التراكيز بين 12-20 نانوغرام/مل)، حالة عوز Deficiency فيتامين D (التراكيز المصلية الأقل من 12 نانوغرام/مل).
تقييم فعالية المرض Disease Activity Score-C Reactive Protein DAS28-CRP))
تم تقييم فعالية التهاب المفاصل الرثياني RAلدى المرضى باستخدام مقياس فعّالية/نشاط المرض في 28 مفصلًا مع قيمة البروتين الارتكاسي C (DAS28-CRP). قيست تراكيز CRP في المصل باستخدام عتيدة Tina-quant C-Reactive Protein IV باستعمال جهاز COBAS INTEGRA/COBAS، من شركة Roche Diagnostics، ألمانيا. عُدّت تراكيز0.5> CRP مغ/دل ضمن الحدود الطبيعيّة، وقد فُسّرت نتائج DAS28-CRP وقُيّم المرضى بموجبها على النّحو التّالي:
- نشاط مرضي مرتفع لقيم 1< DAS
- نشاط متوسط لقيم DAS تقع في المجال من 3.2 وحتى 5.1.
- نشاط منخفض لقيم DAS ≤2.
استعراف الألائل والتّنميط الجيني Genotyping
بُزلت عيناتُ دم ٍوريديٍّ محيطيٍّ بحجم 3 مل على أنبوب يحتوي على مضادٍ التخثر ايتيلن ثنائي الأمين رباعي الخلات Ethylenediamine Tetraacetic Acid (EDTA)، وحُفظت العينات مُعنونة ومُجمّدة بدرجة حرارة -20 درجة مئوية في مخبر التقانة الحيويّة الصّيدلانيّة والمناعية في الهيئة العامة للتّقانة الحيوية لحين استخلاص الحمض النّووي الرّيبوزي منقوص الأوكسجين Deoxyribonucleic Acid (DNA). أُذيبت العيّنات الدمويّة المجمّدة ومن ثم استُخلص الـ DNA باستخدام عتيدة تنقية الحمض النووي الجينومي من Jena Bioscience، ألمانيا، من حجم دم قدره 300 مكل وفقاً للتعليمات المرفقة بعتيدة العزل من الشّركة المصنّعة. وقيست تراكيزه باستخدام جهاز التحليل الطيفيMaestro-Nano® Pro MaestroGen®، تايوان. واعتُمدت الـقيم الـتي تتراوح من 1.7 الـى 4.0 منسباً جيداً للنقاوة وبلغ المتوسط الحسابي (A260/280 ~1.86).
التفاعل التّسلسُليّ للبوليميراز Polymerase Chain Reaction (PCR) والسلسلة Sequencing
قمنا أولاً بالبحث عن التعدد الشكلي Taq-I في الجين المرمز لمستقبل فيتامين D في قاعدة بيانات المركز الوطني لمعلومات التقانة الحيويةNational Institute for Biotechnology Information (NCBI) الخاصّة بالتّعددات الشكليّة باستخدام رقم التعريف rs731236 الخاص بالتعدد الشكلي المدروس. وحدّد موضع التعدد الشّكلي في الجينوم البشري، قمنا بتصميم المرئسين التّقدّمي والعكسي التّاليين:
- التسلسل 5`-AGGTCGGCTAGCTTCTGGAT-3` كمشرع تقدمي Forward Primer
- التّسلسل 5`-CAGTGGTATCACCGGTCAGC-3` كمشرع عكسيReverse Primer
وتم التّأكد من نوعية هذين المشرعين باستعمال أداة MFEprimer وجرت أمثلة in silico لشروط تفاعل البوليميراز التّسلسُليّ PCR والتي أفضت إلى منتجٍ نوعيٍّ بالطول المتوقّع ~292 زوجِ أساسٍ.
أجريت تفاعلات الـ PCR لتضخيم منطقة الـ DNA المتضمنة لـ SNP المستهدف، حيث بلغ حجم التفاعل الكلّي 20 مكل، واحتوى مزيج التفاعل على ما يلي: 200 نانوغرام من الحمض النووي الجينومي، 1 ميكروليتر من كل مرئس (بتركيز 10 بيكومول)، 10 ميكروليتر من مزيج GeneDireX® One PCR™ Master Mix يحتوي على إنزيمTaq Polymerase ، ومحلول التفاعل، وصبغة الهلام، وصبغة فلورية، وأُكمل الحجم النهائي إلى 20 ميكروليتر باستخدام ماء منزوع الأيونات وعقيم. أُجري تفاعل PCR في جهاز المدور الحراري Senso-Quest باستخدام الشروط الموضّحة في الجدول 1.
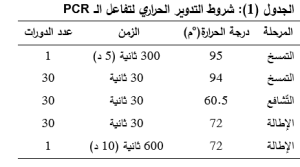
تم تظهير منتجات PCR بترحيلها كهربائيّاً في هلام الأغاروز بعد تعريضها للأشعة فوق البنفسجيّة، ثم نُقّيت المنتجات لإجراء السلسلة ثنائية الاتجاه بطريقة سانغر في شركةMacrogen الكوريّة الجنوبيّة، وقرئت المخططات الاستشرابية chromatograms باستخدام برمجيّة SnapGene®.
التحليلات الإحصائية
تم إجراء التحليلات الإحصائية باستخدام برنامج SPSS الإصدار 26. قورنت المتغيرات الفئوية باستخدام اختبار كاي تربيع (Chi-square)، وعُرضت النتائج على شكل تكرارات ونسب مئوية. أما المتغيرات المستمرة فقد تم تحليلها باستخدام اختباري مان–ويتني Mann–Whitney U وكروسكال–واليس Kruskal–Wallis، حسب الاقتضاء. تم اختبار توزع الأنماط الجينية للتوازن الوراثي وفق قانون هاردي–واينبرغ باستخدام اختبار كاي تربيع. كما حُسبت نسب الأرجحية (ORs) Odds Ratios مع فواصل الثقة 95% (%95(CIs لتقدير العلاقة بين التعدد الشّكلي المدروس وخطر الإصابة بالتهاب المفاصل الرثياني (RA).
النتائج Results
السمات الديموغرافية والسريرية والمتثبتات المخبرية للمشاركين
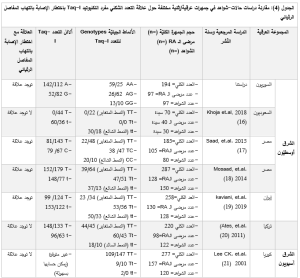
كان متوسط أعمار مرضى التهاب المفاصل الرثياني (RA) والمجموعة الشّاهدة متقارباً (46.03 ±11.29 مقابل 45.68 ±11.23 عاماً)، (p= 0.826). وكان توزّع الفئات العمرية شبه متطابق (p= 0.985). كما كان توزع المرضى والشّواهد بين الجنسين متوازناً، مع غلبة للإناث في كلتا المجموعتين (85% مقابل 83%)(p= 0.700) . كان المتوسط الحسابي لمنسب كتلة الجسم (BMI) متماثلاً لدى مرضى الـ RA مقارنةً مع الأصحاء (24.67 ±3.76 مقابل 24.96 ±3.24 كغ/م²) .(p= 0.564)
لم يسجل فرقٌ يُذكر بين المجموعتين في تواتر اللباس المحافظ، الذي قد يؤثّر في التعرض لأشعة الشمس، حيث بلغت نسبة السيّدات المرتديات للحجاب 84.5% في مجموعة الـ RA مقابل 75.9% في المجموعة الشّاهدة؛p= 0.162) ). كذلك، كان استخدام واقيات الشمس نادراً ومتقارباً بين المجموعتين (5% مقابل 11%؛p= 0.118 ). كان متوسط حرز التعرض لأشعة الشمس أسبوعيّاً أعلى قليلًا لدى المرضى (5.45± 15.80) مقابل 15.26±5.30 ساعة؛p= 0.478) ). لوحظ وجود فارق جليٍّ في معدلات التدخين بين مجموعتي الدّراسة، إذ كانت نسبة المدخنين أقل بشكلٍ ملحوظٍ بين مرضى الـ (22%) RA مقارنةً بالمجموعة الشّاهدة (67%)، .(p= 0.001)
لدى تقييم فعّالية المرض في مجموعة الحالات (مرضى الـ (RA، تبيّن أنّ 15% من المرضى يعانون من فعّاليةٍ/نشاطٍ مرتفعٍ للمرض (DAS28-CRP > 5.1)، وأفادت نسبةٌ تناهز النّصف 51% منهم بتشخيص مبكر للمرض قبل سن الأربعين. كان الميثوتركسات جزءاً من الخطة العلاجية لدى 67% من المرضى.
تخطت نسبة تناول متممات فيتامين D الفمويّة لدى المرضى قبل انخراطهم في الدّراسة 41% مقارنة بنسبةٍ لم تتجاوز 18% لدى الشواهد، p= 0.001)). وكان المرضى أكثر تناولاً لجرعات مرتفعة من متممات فيتامين D (10,000 وحدة/أسبوع أو 20,000–50,000 وحدة/أسبوع)، p= 0.006)). وأظهر المرضى الذين كانوا يتناولون متممات فمويّة من فيتامين D قبل الانخراط في الدّراسة تراكيز مصليّة أعلى من 25(OH)D مقارنةً بأقرانهم ممن لم يتلقوا متممات فيتامين D، وكان الفارق ذا دلالةٍ إحصائيّةٍ كبيرةٍ (p= 0.004). غير أنّ نسب الإصابة بعوز أو نقص فيتامين D كانت أعلى بشكلٍ عام لدى مجمل مرضى RA مقارنة بالشواهد (50% مقابل 35%)؛(p= 0.005) ، كما أبدى المرضى تراكيز مصلية أقل بشكل ملحوظ من 25(OH)D 22.38) 15.80±نانوغرام/مل) مقارنةً بالشّواهد (27.56 ±13.04 نانوغرام/مل)، .(p= 0.036)
نتائج التنميط الجيني
نجحنا في التّنميط الجيني لـ 97 مريضاً و97 شاهداً. يبيّن الشكل 1 أمثلةً عن المنتجات تضخيم قطعة الـDNA المستهدفة مرحلةً على هلامة الأغاروز (الشّكل 1. A)، ويُظهر الأنماط الجينية الثلاثة للتعدد الشكلي Taq-I (الشّكل 1. A،B ،C ). لدى مقارنة نسب انتشار الأنماط الجينيّة للتعدد الشّكلي Taq-I بين المرضى والأصحاء، لوحظ تباينٌ في نسب الانتشار؛ حيث بلغ تواتر النّمط الشّائع متماثل الزيجوت ((AA لدى المرضى 25.8% مقابل 59.8% لدى الشواهد، في حين بلغ تواتر النمط متخالف الزيجوت ((AG نسبة 63.9% لدى المرضى واقتصر على 26.8% من الشواهد، أما النمط متماثل الزيجوت للأليل الطافر (GG) فكان تواتره متقارباً في كلتا مجموعتي المرضى (10.3%) والشواهد (13.4%)، وكانت الفروقات الملاحظة في توزع الأنماط الجينيّة الثلاثة معتدّاً بها إحصائياً (0.0001p=).
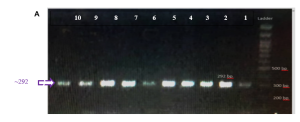
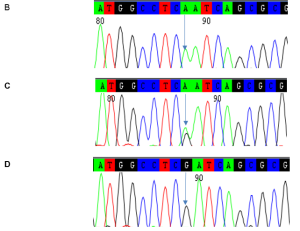
الشكل (1): صورة ممثلة لترحيل منتجات تفاعل البوليميراز المتسلسل (PCR) على هلامة أغاروز (تركيز 1.5%) (A)، حيث تظهر عصابة وحيدة بالطول المتوقّع 292 زوج أساس بالمقارنة مع سلم عياريّات (100 زوج أساس) للحمض النووي منقوص الأكسجين الـDNA. المخططات الاستشرابية Chromatograms لتسلسل الـDNA في منطقة التعدد الشكلي مفرد النكليوتيد Taq-I (rs731236) في الجين المرمزة لمستقبل فيتامين D، حيث يمثل المخطط B مثالاً عن النّمط الجينيّ متماثل الزيجوت للأليل الشّائع (AA)، ويمثّل المخطط C مثالاً للنمط الجيني متخالف الزيجوت (ِAG)، في حين يبيّن المخطط D مثالاً للنمط الجيني متماثل الزيجوت للأليل المتغاير (GG).
قُورنت تواترات أليلي التعدد الشكلي مفرد النكليوتيد Taq-I في جمهرة الدراسة، وبرز تباين واضح في نسب تواترهما، حيث بلغت نسبة تواتر الأليل A 57.7% لدى المرضى مقابل 73.2% لدى الشواهد، وبالمقابل كانت نسبة تواتر الأليل G (المرضى 42.3%/الشواهد 26.8%). وكان الفارق في تواتر الأليلين ذا دلالةٍ إحصائيةٍ (p= 0.001) اعتماداً على اختبارPearson Chi-Square .
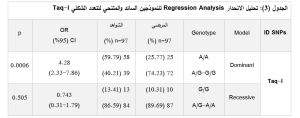
بلغت قيمة منسب الأرجحية(OR) للأليل A OR= 0.50))، أي أن وجود الأليل A (السائد) يرتبط بانخفاض احتمالية وقوع المرض بنسبة 50%، وبلغت قيمة منسب الأرجحيّة 2 للأليل G (OR= 2)، أي أن وجود الأليل G (المتغاير) يزيد من احتمالية الإصابة بالمرض بمقدار الضعف، يُبين الجدول 2 توزع الأنماط الجينية وتواتر أليلي التعدد الشكلي الـTaq-I
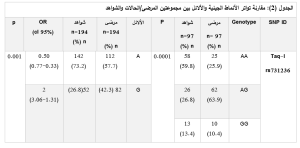
أجري تحليل الانحدار وفق نموذجي الوراثة السائد والمتنحي لأليلي التعدد الشكلي ـTaq-I، وبينت النتائج وجود اختلاف في توزّع الأنماط الجينية بشكل ملحوظ بين مجموعتي المرضى والشّواهد، مما يُشير الى ارتباط هذا الـ SNP بالمرض. وأشارت النتائج الى أنّ وجود الأليل G يرتبط بزيادة خطر الإصابة بالــRA بمقدار الضعف مقارنةً بالأليل A. كما أظهر التحليل أن وجود أليل G واحد على الأقل (أي النّمطين سواءً GG أم GA) يزيد من خطر الإصابة بـالـ RA بمقدار 4.28 مرة مقارنةً بالنّمط الجيني AA، مما يدل على وجود تأثيرٍ سائدٍ قويٍّ للأليل G ممّا يرجّح دوره كعامل خطورة حتى لدى امتلاك الفرد له بنسخة واحدة فحسب. يُلخّص الجدول 3 هذه النتائج.
لم يُظهر التعدد الشكلي Taq-I (سواءً في توزع الأنماط الجينية أو الألائل) ارتباطاً مع التراكيز المصلية لفيتامين D (p=0.149)، لكن، كان جديراً بالملاحظة ارتباط النّمط الجيني AA باحتماليّة أعلى لارتفاع قيمة حرز فعالية المرض DAS28-CRP بمقدار 16 ضعفاً وبدلالةٍ هامةٍ إحصائياً (p=0.022). ومن جهة أخرى، لم يكن لكلّ من القصة العائلية للسكري أو عمر تشخيص المرض، أو استخدام الميثوتركسات ضمن الخطة العلاجية، تأثيرٌ يذكرٌ على المحصلات السريرية في مجموعة المرضى.
المناقشة Discussion
أجريت هذه الدراسة الرّصدية من نمط (حالة- شاهد) والتي شملت 100 مريضٍ مشخصين بالتهاب المفاصل الرثياني وفق معايير ACR/Eular 2010، تم اختيارهم بناءً على معايير تضمينٍ دقيقةٍ أهمها نفي وجود أمراضٍ تؤثر في التراكيز المصلية لفيتامين D واستتباب الكالسيوم والفسفور. تمت مقايسة التراكيز المصليّة لفيتامين D معبراً عنه بالكالسيفرول أو 25(OH)D في جمهرة الدراسة بطريقة الاختبار المناعي بالتألق الكيميائي الكهربائي، واعتمدنا في تصنيف أفراد مجموعتي المرضى والشّواهد بناءً على حالة التراكيز المصلية لفيتامين D على توصيات معهد الطب الأمريكي IOMالصادرة في عام 2012 (8)، ودعمت نتائجنا وجود فارق دالٍّ إحصائياً بين المرضى والشواهد في التراكيز المصلية لفيتامين D، حيث أنّ وجود نقص شائع في فيتامين D بين المرضى يدعم الفرضية القائلة بأن نقص أو عوز هذا الفيتامين ليس مجرد نتيجة ثانوية للمرض، بل قد يكون عاملًا ممهِّدًا أو مساهمًا في تطوره (9)، وتشابهت بهذا نتائجنا مع دراساتٍ مشابهة في كلٍّ من السعودية وباكستان والصين (10-12).
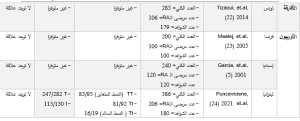
توفّر نتائج هذه الدراسة دعماً إضافياً لفرضية الدور المحتمل للتعدد الشّكليTaq-I (rs731236) للجين المرمزة لمستقبل فيتامين D (VDR)في الاستعداد للإصابة بالتهاب المفاصل الرثياني(RA) ، فقد أظهر توزّع الأنماط الجينية والألائل في العينة السورية المدروسة اختلافاً دالاً إحصائيّاً بين المرضى والأفراد الأصحاء. ودعمت نتائج الدّراسة الحاليّة ارتباط الأليل G للتعدد الشكلي Taq-I، حتى بنسخة أليل واحدة (وفق نموذج سائد Dominant Model)، باختطار تطّور الإصابة بـ RA بما يقارب الضعف (OR= 2.00, P= 0.001)، وهو ما يشير إلى تأثيرٍ جينيٍّ واضحٍ في إمراضية المرض، حيث يُعد الـ Taq-I من التعددات الشكلية مفردة النكليوتيد التي تقع في المنطقة المرمّزة coding region Polymorphism، وعلى وجه التّحديد في الإكسون التّاسع بالقرب من النّهاية ´3، ويُصنّف ضمن ما تُسمى بـالتعددات المرادفة Synonymous SNP، فهو لا يُغير الأحماض الأمينية في بروتين مستقبل فيتامين D. إلا أنّ دراسات جينومية سابقة اقترحت أنّ هذا التّعدد الشّكلي قد يؤثر في ثباتية الرنا المرسال mRNA stability أو الكفاءة في الترجمة البروتينية، مما يُعد آلية محتملة لتأثيره السلبي في التعبير الجيني عن مستقبل فيتامين D (VDR) (13)، من الناحية الوظيفية، قد يؤدي ذلك لتغيير في التعبير عن بروتين مستقبل فيتامين D مما قد يؤثر بالمحصلة في دوره المناعي المضاد للالتهاب، وخاصة كبح إنتاج السيتوكينات مثل IL-2 وIFN-γ من الخلايا T، ما يُسهم في تحفيز ردود الفعل المناعيّة الذاتيّة (7). يُبين الجدول (4) مقارنةً لدراسات الحالات-شواهد الدراسات case-control studies المشابهة لدراستنا في مجموعات عرقية/إثنية مختلفة تشمل جمهرات شرق أوسطية والمنشورة في الدوريات العالمية، حيث برهنت معظم الدراسات في جمهرات شرق أوسطية وشمال إفريقيّة (مصر) على وجود علاقة بين التعدد الشكلي مفرد النكليوتيد Taq-I والاستعداد للإصابة بالتهاب المفاصل الرثياني، في حين غابت البيّنة على وجود مثل هذه العلاقة في الجمهرات الشرق آسيوية والأوروبيّة والإفريقيّة. وقد يُعزى سبب التباين مع دراستنا الى الطريقة المعتمدة في التّنميط الجيني للجمهرات المدروسة، حيث اعتمدت دراستنا على تقنية سلسلة قطعة الدنا الجينومي المضخّمة بتفاعل البوليميراز التسلسلي (PCR)، وهي طريقة عالية الدقة وتُعدّ معياريّة للكشف عن الأنماط الجينية في قطعة الدنا المستخلصة بعد تضخيمها بتفاعل الـPCR، في حين اعتمدت دراسات أخرى على تقنية تحري تعدد الأشكال في الجزء محدد الطول Restriction Fragment Length Polymorphism (RFLP)، والتي قد تكون أقل دقةً مقارنةً بطريقة السلسلة المباشرة (14، 15).
لوحظ حسب نتائجنا ارتباط النمط الجينيAA بزيادة في شدة المرض، مما يعكس دوراً مغايراً لكل من النمط الجيني والأليل في مراحل مختلفة من سير المرض. ويتماشى هذا التمايز مع ما أشارت إليه دراساتٌ سابقةٌ بأن العوامل الجينية المسؤولة عن الاستعداد الوراثي للإصابة لا ترتبط بالضرورة بـشدة المرض أو فعاليته السريرية، ففي دراسة Scottوزملاؤه (2019)، لم تلاحظ علاقة بين المتغايرات الجينية المرتبطة بالاستعداد للإصابة بـ RA وقيمة حرز فعالية المرض DAS28 بين المرضى (25). وبالمقابل وُجد في دراسة أخرى أجراها Johnsen وزملاؤه (2008) أن التعددات الشكلية في بعض الجينات الالتهابية، مثل تلك المرمزة لـIL-1، والتي تلعب دوراً في تطور التآكلات المفصلية لدى المرضى المصابين بالـRA لم تكن مرتبطة باختطار الإصابة بالمرض ذاته (26). بناءً عليه، يُحتمل أنّ الأليل G يؤدي دوراً في تحريض الاستجابة المناعية الأولية التي تمهد لظهور المرض، بينما يرتبط النمط AA بالفعالية وشدة المرض لدى المرضى المصابين، ربما من خلال تأثيره في التعبير عن الـ VDR أو استجابته الوظيفية للفيتامين D، مما يقلل من التأثير التثبيطي للفيتامين D على السيتوكينات الالتهابية مثل TNF-α وIL-17، وIL-2 التي تنتجها الخلايا التائية T-cells، وبالتالي تحفيز ردود الفعل المناعيّة الذاتيّة وزيادة شدة المرض (27).
الاستنتاجات Conclusions
تدعم هذه الدراسة فرضيّة وجود علاقةٍ ذاتِ دلالة ٍإحصائيةٍ بين التغاير الجيني Taq-I (rs731236) في الجين المرمّز لمستقبل فيتامين D واختطار الإصابة بالتهاب المفاصل الرثياني، بالإضافة إلى ارتباطه بشدة المرض، كما تُعزز النتائج إمكانية اعتبار هذا التغاير واصماً جينياً مفيداً في التنبؤ بقابلية الإصابة وفعاليّة المرض، مما قد يُسهم في تطوير استراتيجيات للوقاية الشخصية والتدبير العلاجي المبكر.
ومع ذلك، تُوصى بإجراء دراساتٍ مستقبلية ٍعلى عينات أكبر ومن أعراقٍ أو إثنيات مختلفةٍ، تتضمّن تعددات شكليّة أخرى في جين VDR ودراسة التداخل مع العوامل البيئية والغذائية، وذلك لتعميق الفهم حول الدور الجزيئي لهذه التغايرات في الفيزيولوجيا المرضية لـ RA والعلاج الشّخصاني.
قائمة الاختصارات List of abbreviations
| ACR | American College of Rheumatology | الكليّة الأمريكيّة للأمراض الرثيانيّة |
| BMI | Body Mass Index | منسب كتلة الجسم |
| CRP | C-Reactive Protein | البروتين المتفاعل C |
| DAS28-CRP | Disease Activity Score in 28 Joints with C-Reactive Protein Level | حرز فعاليّة المرض في 28 مفصل مع قيمة البروتين المتفاعل C |
| DNA | Deoxyribonucleic Acid | الحمض النووي الريبي منقوص الأكسجين |
| EDTA | Ethylenediamine Tetraacetic Acid | ايتيلن ثنائي الأمين رباعي الخلات |
| EULAR | European Alliance of Association for Rheumatology | التحالف الأوروبي لرابطة طب الأمراض الرثيانية |
| IU | International Unit | وحدة دولية |
| PCR | Polymerase Chain Reaction | التفاعل السلسلي للبوليميراز |
| ORs | Ratios Odds | نسب الأرجحية |
| RA | Rheumatoid Arthritis | التهاب المفاصل الرثياني أو الداء الروماتويدي |
| SNPs | Single Nucleotide Polymorphisms | التعددات الشكلية مفردة النكليوتيد |
| VDR | Vitamin D Receptor | مستقبل الفيتامين D |
| (OH)VD3 25 | 25 hydroxy Vitamin D3 | 25 هيدروكسي فيتامين D3 |
الموافقة الأخلاقية والموافقة على المشاركة Ethics approval and consent to participate
تتوافق هذه الدراسة مع إعلان هلنسكي وتمّ إجراؤها وفقاً لموافقة لجنة الأخلاقيات في جامعة دمشق رقم
MD-210125-21-H23
تضارب المصالح Conflict of interests
يُقرّ المؤلفون بعدم وجود مصالح مُتضاربة.
التمويل Funding
مُوِّل هذا البحث من قبل جامعة دمشق.
مساهمات المؤلفين Author’s contributions
قامت زينب سعيد شحادة بتجنيد المرضى والشواهد، وإجراء المقابلات السريرية، والتحقق من استيفاء معايير التضمين والاستبعاد، كما ساهمت في العمل الجزيئي والتنميط الجيني وإجراء المقايسات المخبرية، وشاركت في إعداد المسودة الأولى للمخطوط. قامت لمى علي يوسف بتصميم الدراسة ووضع إطارها المفاهيمي، والإشراف على تنفيذها ومتابعة سير العمل، كما شاركت في تفسير النتائج وإعداد المسودة الأولى للمخطوط وتولّت مراجعته العلمية بصيغته النهائية. شاركت ميسون أحمد قدسي في الإشراف الأكاديمي والعلمي على الدراسة ومراجعة محتواها. تولّى إبراهيم وليد حنفي إجراء التحليلات الإحصائية وتفسير نتائجها. ساهمت رهام سمير أنطاكي في العمل الجزيئي والتنميط الجيني والمراحل التقنية المرتبطة به. اطّلع جميع المؤلفين على النسخة النهائية من المخطوط ووافقوا عليها.
المراجع :- Almutairi KB. Nossent JC. Preen DB. Keen HI. Inderjeeth CA. The Prevalence of Rheumatoid Arthritis: A Systematic Review of PoPulation-based Studies. J Rheumatol. 2021 May;48(5):669-676. doi: 10.3899/jrheum.200367. EPub 2020 Oct 15. PMID: 33060323.
- Q.. Y. Wang. D. Xu. J. Nossent. N. J. Pavlos and J. Xu (2018). “Rheumatoid arthritis: Pathological mechanisms and modern Pharmacologic theraPies.” Bone Res 6: 15
- Aranow C. Vitamin D and the immune system. J Investig Med. 2011 Aug;59(6):881-6. doi: 10.2310/JIM.0b013e31821b8755. PMID: 21527855; PMCID: PMC3166406.
- L.; Penna. G. Control of autoimmune diseases by the vitamin D endocrine system. Nat. Clin. Pract.Rheumatol. 2008. 4. 404–412.
- Garcia-Lozano JR. Gonzalez-Escribano MF. Valenzuela A. et al. Association of vitamin D genotyPes with early onset rheumatoid arthritis. Eur J Immunogenet. 2001; 28:89–93. doi: 10.1046/j.1365-2370.2001.00233.x.
- N.A.. et al.. 1994. Prediction of bone density from vitamin D recePtor alleles. Nature 367 (6460). 284–287 .
- Ao T, Kikuta J, Ishii M. The Effects of Vitamin D on Immune System and Inflammatory Diseases. Biomolecules. 2021 Nov 3;11(11):1624. doi: 10.3390/biom11111624. PMID: 34827621; PMCID: PMC8615708.
- Rosen CJ, Abrams SA, Aloia JF, et.al, IOM committee members resPond to Endocrine Society vitamin D guideline. J Clin Endocrinol Metab. 2012 APr;97(4):1146-52. doi: 10.1210/jc.2011-2218. EPub 2012 Mar 22. PMID: 22442278; PMCID: PMC5393439.
- Lee YH, Bae SC. Vitamin D level in rheumatoid arthritis and its correlation with the disease activity: a meta-analysis. Clin ExP Rheumatol. 2016 SeP-Oct;34(5):827-833. EPub 2016 APr 6. PMID: 27049238.
- Atwa MA, Balata MG, Hussein AM, Abdelrahman NI, Elminshawy HH. Serum 25-hydroxyvitamin D concentration in Patients with Psoriasis and rheumatoid arthritis and its association with disease activity and serum tumor necrosis factor-alPha. Saudi Med J. 2013 Aug;34(8):806-13. PMID: 23974451.
- Sukharani N, Dev K, Rahul F, Bai P, Ali A, Avinash F, Kammawal Y, Kumar N, Rizwan A. Association Between Rheumatoid Arthritis and Serum Vitamin D Levels. Cureus. 2021 SeP 24;13(9):e18255. doi: 10.7759/cureus.18255. PMID: 34712532; PMCID: PMC8542394.
- Wen HY, Luo J, Li XF. Vitamin D Levels and Associations With Disease Activity in Chinese Han Patients With Early Rheumatoid Arthritis. J Clin Rheumatol. 2015 Aug;21(5):276-7. doi: 10.1097/RHU.0000000000000268. PMID: 26203837.
- N.A.. et al.. 1994. Prediction of bone density from vitamin D recePtor alleles. Nature 367 (6460). 284–287 .
- Mardis ER. Next-generation DNA sequencing methods. Annu Rev Genomics Hum Genet. 2008;9:387-402. doi: 10.1146/annurev.genom.9.081307.164359. PMID: 18576944.
- Kratochwil CF, Kautt AF, Rometsch SJ, Meyer A. Benefits and limitations of a new genome-based PCR-RFLP genotyPing assay (GB-RFLP): A SNP-based detection method for identification of sPecies in extremely young adaPtive radiations. Ecol Evol. 2022 Mar 23;12(3):e8751. doi: 10.1002/ece3.8751. PMID: 35356554; PMCID: PMC8941502.
- Khoja, S.O., Al-Jehani, R.F., Bahlas, S.M., Algamdi, S.A. and Attar, S., 2018. Evaluation of RelationshiP Between Vitamin D RecePtor Gene PolymorPhisms and Rheumatoid Arthritis in Saudi PoPulation. PharmacoPhore. 2018; 9: 85, 94.
- Saad MN, Mabrouk MS, Eldeib AM, Shaker OG. Genetic Case-Control Study for Eight PolymorPhisms Associated with Rheumatoid Arthritis. PLoS One. 2015 Jul 6;10(7):e0131960. doi: 10.1371/journal.Pone.0131960. PMID: 26147289; PMCID: PMC4492599.
- Mosaad YM, Hammad EM, Fawzy Z, Abdal Aal IA, Youssef HM, ElSaid TO, Monir R, El-Deek BS. Vitamin D recePtor gene PolymorPhism as Possible risk factor in rheumatoid arthritis and rheumatoid related osteoPorosis. Hum Immunol. 2014 May;75(5):452-61. doi: 10.1016/j.humimm.2014.02.009. EPub 2014 Feb 12. PMID: 24530824.
- Bazzazi, H. (2019). The Association of Vitamin D RecePtor PolymorPhisms of FokI and TaqI with Rheumatoid Arthritis in North-East of Iran. Jorjani Biomedicine Journal , 7 (4), 20-29.
- Ates Ö, Dolek B, Dalyan L, ToPal-Sarikaya A. Vitamin D recePtor gene PolymorPhisms in rheumatoid arthritis. Turk J Rheumatol. 2011;26(2): 145–149.
- Lee CK. Hong JS. Cho YS. et al. Lack of relationshiP between vitamin D recePtor PolymorPhism and bone erosion in rheumatoid arthritis. J Korean Med Sci. 2001; 16:188–92. doi: 10.3346/jkms.2001.16.2.188
- Tizaoui K, Kaabachi W, Ouled Salah M, Ben Amor A, Hamzaoui A, Hamzaoui K. Vitamin D recePtor Taq-I and APa-I PolymorPhisms: a comParative study in Patients with Behçet’s disease and Rheumatoid arthritis in Tunisian PoPulation. Cell Immunol. 2014 Jul;290(1):66-71. doi: 10.1016/j.cellimm.2014.05.002. EPub 2014 May 17. PMID: 24880677.
- Maalej A, Petit-Teixeira E, Michou L, Rebai A, Cornelis F, Ayadi H. Association study of VDR gene with rheumatoid arthritis in the French PoPulation. Genes Immun. 2005 Dec;6(8):707-11. doi: 10.1038/sj.gene.6364260. PMID: 16151416.
- Punceviciene E, Gaizevska J, Sabaliauskaite R, et.al, Vitamin D and VDR Gene PolymorPhisms’ Association with Rheumatoid Arthritis in Lithuanian PoPulation. Medicina (Kaunas). 2021 APr 3;57(4):346. doi: 10.3390/medicina57040346. PMID: 33916688; PMCID: PMC8065838.
- Scott IC, Rijsdijk F, Walker J, et,al. Do Genetic SuscePtibility Variants Associate with Disease Severity in Early Active Rheumatoid Arthritis? J Rheumatol. 2015 Jul;42(7):1131-40. doi: 10.3899/jrheum.141211. EPub 2015 May 15. PMID: 25979711; PMCID: PMC6714044.
- Johnsen AK, Plenge RM, Butty V, et, al. A broad analysis of IL1 PolymorPhism and rheumatoid arthritis. Arthritis Rheum. 2008 Jul;58(7):1947-57. doi: 10.1002/art.23592. PMID: 18576312; PMCID: PMC2533126.
- Mohammadi A, Azarnezhad A, Khanbabaei H, IzadPanah E, Abdollahzadeh R, Barreto GE, Sahebkar A. Vitamin D recePtor genetic PolymorPhisms and the risk of multiPle sclerosis: A systematic review and meta-analysis. Steroids. 2020 Jun;158:108615. doi: 10.1016/j.steroids.2020.108615. EPub 2020 Feb 22. PMID: 32097613.